Mekanisme Molekul Peraturan Progenitor Renal: Berapa Banyak Kepingan dalam Teka-teki?
Feb 24, 2022
Abstrak: buah pinggangtikus, tikus dan manusia mempunyai nenek moyang yang mengekalkan homeostasis harian dan mengambil bahagian dalam proses penjanaan semula endogen selepas kecederaan, kerana keupayaan mereka untuk membiak dan membezakan. Dalam petak glomerular dan tiub nefron, kajian yang konsisten menunjukkan bahawa populasi sel progenitor yang dicirikan dengan baik dan berbeza, disetempat dalam epitelium parietal kapsul Bowman dan bertaburan di tubul proksimal dan distal, boleh menjana sel khusus segmen dalam keadaan fisiologi. dan kecederaan tisu berikutan. Walau bagaimanapun, tindak balas penjanaan semula yang rosak atau tidak normal dari progenitor ini boleh menyumbang kepada keadaan patologi. Ciri-ciri molekul bagibuah pinggangprogenitor telah dikaji secara meluas, mendedahkan bahawa banyak laluan klasik dan terpelihara secara evolusi, seperti Notch atau Wnt/ -catenin, memainkan peranan utama dalam pengawalan sel. Lain-lain, seperti asid retinoik, sistem renin-angiotensin-aldosteron, TLR2 (Toll-like receptor 2) dan leptin, juga penting dalam proses ini. Dalam ulasan ini, kami meringkaskan kebanyakan mekanisme molekul mengarahkanbuah pinggangtindak balas progenitor semasa homeostasis dan berikutkecederaan buah pinggang.Akhir sekali, kami akan meneroka bagaimana penjujukan RNA sel tunggal boleh membawa pencirianbuah pinggangnenek moyang ke peringkat seterusnya, sambil mengetahui tandatangan molekul mereka semakin relevan di klinik.
Kata kunci:nenek moyang buah pinggang; mekanisme molekul; kecederaan buah pinggang; penjujukan RNA sel tunggal; tandatangan molekul

CISTANCHE AKAN MEMPERBAIKI PENYAKIT BUAH PINGGANG/PINGGANG
pengenalan Mekanisme penjanaan semula dan pembaikan endogen telah dicadangkan untuk beberapa organ mamalia [1]. Organ regeneratif klasik, seperti saluran gastrousus dan kulit, telah dikaji secara meluas selama bertahun-tahun dan telah menunjukkan peranan utama leluhur endogen [2]. Di dalam usus, sel stem usus mengekalkan homeostasis harian, manakala sel stem/progenitor yang berbeza bertanggungjawab ke atas proses pembaikan pantas selepas kecederaan [2]. Begitu juga, sel stem epidermis membentuk kumpulan sel stem heterogen yang mengambil bahagian dalam homeostasis epidermis, serta pembaikan tisu, selepas kecederaan [3]. Yang dewasabuah pinggangadalah organ dengan perolehan selular yang rendah dan dikurniakan nenek moyang yang mampu membiak dan membezakan [4,5]. Harta berharga ini membolehkan para penyelidik dan pakar klinik memikirkan cara terapeutik baharu untuk dipulihkanfungsi buah pinggangselepas kecederaan. Di sini, kami mencadangkan gambaran keseluruhan mekanisme molekul yang berlaku dalam glomerular dan tiubbuah pinggangnenek moyang dalam keadaan fisiologi dan patologi (Rajah 1) dan bagaimana disregulasi laluan ini boleh berlaku pada asalpenyakit buah pinggang. Kami juga akan mengkaji bagaimanabuah pinggangnenek moyang boleh dicirikan lagi menggunakan teknologi penjujukan RNA sel tunggal (scRNAseq) dan kaitan klinikal tandatangan molekul sel-sel ini.


Nenek moyang buah pinggang
Nenek moyang buah pinggang telah ditemui oleh Sagrinati et al. pada manusiabuah pinggang, berdasarkan ekspresi penanda sel stem CD133 dan CD24, dalam ketiadaan atau ekspresi rendah penanda pembezaan [6,7]. Sel CD133 plus CD24 plus disetempat di kutub kencing kapsul Bowman, serta bertaburan di sepanjang petak tiub nefron di antara sel tiub yang berbeza [6]. Beberapabuah pinggangprogenitor, termasuk yang dilokalkan dalam kapsul Bowman dan subset daripada yang terkumpul di sepanjang tubul, juga menyatakan CD106 (juga dipanggil molekul lekatan sel vaskular 1, VCAM1), manakala majoriti progenitor yang disetempat di sepanjang tubul tidak [6, 8]. Perbezaan dC fenotip ini mencerminkan kapasiti fungsian yang pelbagai; sesungguhnya, sel CD133 tambah CD24 tambah CD106- yang bertaburan di sepanjang tubulus memaparkan ciri fungsi progenitor tiub, manakala CD133 tambah CD24 tambah CD106 serta belut epitelium parietal (PEC) adalah berbilang potensi [6]. Di samping itu, subset CD1 33 tambah CD24 tambah CD1 06 serta progenitor yang disetempatkan berhampiran kutub distal kapsul Bowman dan podocalyxin yang mengekspresikan hanya mampu menjana podosit [6]. Secara keseluruhannya, pemerhatian ini mengkonfigurasi garis keturunan hierarkibuah pinggangnenek moyang dalambuah pinggangyang mengingatkan sistem hemopoietik [9]. PEC dengan ciri progenitor yang sama dan penyetempatan anatomi juga dikenal pasti dalam tetikus dan tikusbuah pinggang[4,10,11]. Penandaan genetik PEC dalam garis tetikus yang boleh diinduksi transgenik menunjukkan bahawa PEC berhijrah ke jumbai glomerular dan membezakan menjadi podosit dalam tikus iklan [11]. Lagipun, Pax2 telah dikenal pasti sebagai penanda untuk tetikusbuah pinggangnenek moyang, dan penciptaan modol tetikus yang boleh diinduksi untuk pengesanan keturunan bagi populasi sel Pax2 ditambah yang dibenarkan untuk menafikan pembezaanbuah pinggangprogenitor disetempat di kalangan PEC ke dalam podosit semasa pertumbuhan glomerular selepas bersalin [4]. Kajian lanjut menunjukkan bahawa juxtamedullary dan corticol glomeruli mempunyai bilangan Pax2 plus progenitor yang berbeza, dengan kortikal dikurniakan dua kali lebih banyak Pax2 plus progenitor pee kiraan podosit glomerular dalam keadaan sihat [12]. Pada tikus dewasabuah pinggang, sel tidak matang yang menyatakan molekul lekatan sel saraf (NCAM) dan penanda sel progenitor CD24 telah diterangkan di antara sel epitelium yang melapisi kapsul Bowman tikus [10].
Penandaan genetik Pax2 plus progenitor kapsul Bowman tikus dibenarkan untuk menunjukkan bahawa progenitor ini membezakan menjadi podosit dalam model glomerulosclerosis segmental fokus (FSGS), dan tindak balas mereka terhadap kecederaan menentukan hasil gangguan glomerular, seterusnya menyokong peranan mereka sebagai podosit. nenek moyang [4,12]. Baru-baru ini, menggunakan model tetikus transgenik di mana podosit dilabelkan dengan GFP (protein pendarfluor hijau) dan PEC secara serentak dilabelkan dengan tdTomato, Kaverina dan rakan sekerja juga memberikan bukti kukuh bahawa PEC berfungsi sebagai sumber podosit baru dalam tikus dewasa apabila kecederaan. Sel-sel ini bersama-sama menyatakan dua label pendarfluor, memperoleh penanda podosit dan menunjukkan proses kaki primer, sekunder dan tertier [13]. Tindak balas progenitor yang tidak normal terhadap kecederaan juga boleh menyumbang kepada perintah dis glomerular [4,10,14,15]. Malah, dalam keadaan tertentu, pada manusia, tikus dan tikus, penghijrahan huru-hara dan percambahan sel progenitor kapsul Bowman telah ditunjukkan untuk menyumbang kepada pembentukan bulan sabit dan parut glomerular [4,10,14]. Kajian tentang manusiabuah pinggangbiopsi adalah konsisten dengan konsep bahawa progenitor yang membiak menghasilkan lesi hiperplastik dalam glomerulopati bulan sabit dan runtuh [14], dan keputusan yang sama telah diperolehi pada tikus [10]. Pada tikus, pengesanan keturunan PEC menunjukkan bahawa percambahan mereka membawa kepada peningkatan ketara dalam bilangan sel dalam bulan sabit nefritis serum nefrotoksik murine dan glomerulopati yang runtuh [16] dan pembentukan lesi sklerotik dan pemendapan matriks ekstraselular dalam FSGS [15]. Baru-baru ini, pengesanan genetik khusus nenek moyang di kalangan PEC menunjukkan penglibatan mereka dalam penjanaan lesi glomerular hiperplastik yang boleh dibayangkan sebagai kegagalan untuk menjana semula podosit berikutan kecederaan [4]. Daripada semua kajian ini, kini jelas bahawabuah pinggangnenek moyang yang disetempatkan di kalangan PEC bertindak balas terhadap kecederaan podocyte, mencetuskan program penjanaan semula, tetapi tindak balas yang tidak cekap atau berlebihan boleh menyebabkan tisu berfungsi menjadi tisu seperti parut yang terdiri daripada sel dan matriks ekstraselular yang tidak teratur. Oleh itu, mengetahui mekanisme yang mendorong tindak balas proliferatif dan pembezaan yang betulbuah pinggangprogenitor semasa homeostasis dan kecederaan berikutan adalah sangat penting dan mungkin membenarkan pengenalpastian modulator putatif untuk meningkatkan potensi penjanaan semulabuah pinggangnenek moyang.
Pengawal selia Fisiologi Progenitor Glomerular: Apabila Orkestra Melantunkan Melodi
Laluan isyarat manakah yang mengawal senyap progenitor glomerular, percambahan dan pembezaan ke arah podosit dalam sihatbuah pinggang? Kajian mengenai nefrogenesis menunjukkan bahawa pengaktifan isyarat -catenin/Wnt mewakili langkah penting yang memacu pembezaan PEC ke dalam podosit semasa pembangunan [17,18]. Sesungguhnya, pemadaman Ctnnb1 ( -catenin 1) dalam PEC dalam tetikus kalah mati bersyarat pada peringkat badan berbentuk S lewat menyebabkan anomali glomerular dan penggantian PEC dalam kapsul Bowman dengan podosit yang dibezakan dengan baik. Mengesan nefrogenesis dalam tikus kalah mati bersyarat-catenin bersyarat embrio mendedahkan bahawa "podosit parietal" ini berasal daripada sel prekursor dalam lapisan parietal badan berbentuk S melalui suis keturunan langsung. Findings ini menunjukkan bahawa isyarat -catenin/Wnt diperlukan untuk pembezaan dan pematangan PEC yang betul kepada podosit [17]. WT1, pengawal selia utama proses ini [19], juga merupakan perencat kuat laluan isyarat -catenin/Wnt [18]. Kajian yang dilakukan dalam PEC senyap menunjukkan bahawa ekspresi WT1 ditindas oleh tahap tinggi Pax2 dan oleh ekspresi tahap tinggi mikroRNA-193a (miR-193a) [20]. Apabila PEC mengecilkan ekspresi miR-193a, ini membenarkan pengawalseliaan WT1, yang menyekat isyarat -catenin/Wnt dan mendorong pembezaan PEC menjadi podosit. Keputusan in vitro terkini menunjukkan bahawa apolipoprotein L1 (APOL1) juga mengawal fenotip molekul PEC melalui modulasi ekspresi miR193a dan APOL1 dan miR193a berkongsi hubungan maklum balas timbal balik [21]. Malah, dalam sistem kultur, pembezaan PEC kepada podosit telah disertai dengan penurunan dalam miR-193ungkapan. Begitu juga, penindasan miR-193a mempertingkatkan ungkapan APOL1 [21]. Kerja masa hadapan harus menangani sama ada paksi APOL1–miR-193ini berfungsi dengan cara yang sama dalam vivo seperti yang dilakukan secara in vitro dalam model tetikus transgenik yang berkaitan dan dalam manusiabuah pinggang. Menariknya, APOL1 adalah gen kerentanan, dengan varian genetik yang meningkatkan kemungkinan untuk membangunkan podocytopathies [22].
Kawalan keputusan nasib sel dan percambahan sel dalam banyak sistem yang berbeza dikendalikan melalui isyarat bersepadu laluan isyarat Wnt dan Notch [23]. Lasagni et al. melaporkan bahawa, dalambuah pinggangprogenitor yang dilokalkan dalam kapsul Bowman, pengaktifan Notch menggalakkan kemasukan ke fasa-S kitaran sel dan mitosis seterusnya sehingga mereka berada dalam keadaan yang tidak dibezakan [24]. Walau bagaimanapun, penurunan kawal selia laluan Notch semasabuah pinggangpembezaan progenitor mendorong penjanaan podosit dengan kandungan DNA yang tidak normal dan kematian berikutan oleh malapetaka mitosis [24,25]. Keputusan terkini menunjukkan bahawa CXCL12 yang berasal dari podocyte (ligan chemokine motif CXC 12) menghalang isyarat Notch, dengan itu mengekalkan ketenangan leluhur podocyte [12]. Notch downregulation mengaitkan dengan upregulation perencat kitaran sel p21, p27 dan p57 dan downregulation bagi cyclin D1 [24], memberikan podosit ciri-ciri sel postmitotic, nonproliferative. Mekanisme maklum balas progenitor podosit-renal CXCL{13}}pengantara juga mengehadkan penjanaan semula podosit selepas kecederaan glomerular [12]. Memang menggunakan pengesanan keturunan Pax2 plusbuah pinggangnenek moyang pada tikus dengan nefropati yang disebabkan oleh Adriamycin, para penyelidik menunjukkan bahawa sekatan CXCL12 menggalakkan pembentukan podocyte de novo dan melemahkan glomerulosclerosis [12].

CISTANCHE AKAN MENINGKATKAN FUNGSI BUAH PINGGANG/BUAH PINGGANG
Sebagai penambahbaikan daripadabuah pinggangpembezaan progenitor kepada podosit mungkin mewakili strategi terapeutik yang menarik untuk menggalakkan pengampunan gangguan glomerular, beberapa kajian telah dilakukan untuk mengenal pasti sebatian yang membezakan. Asid retinoik (RA) adalah derivatif vitamin A dengan faedah yang telah ditetapkan dalam rawatan pelbagai jenis kanser [26]. RA juga telah ditunjukkan untuk melindungi daripadakecederaan buah pinggangdalam pelbagai model eksperimenpenyakit buah pinggang,termasuk penyakit perubahan minimum, nefropati membran, FSGS, human immunodefificiency virus (HIV)-associated nephropathy (HIVAN) dan lupus nephritis [27]. Banyak kajian telah menggariskan peranan RA dalam pembezaan podocyte in vitro [28,29], dan kami menggunakan RA dalam media kultur sel untuk mempromosikanbuah pinggangpembezaan progenitor ke arah keturunan podosit [7]. Menariknya, pendedahan kepada albumin, yang mengikat RA dengan pertalian tinggi, semasa kultur in vitro boleh menghalangbuah pinggangpembezaan progenitor ke arah podosit dengan mengasingkan RA. Dalam vivo, kami melaporkan bahawa RA telah dikeluarkan dalam ruang Bowman berikutan kecederaan glomerular dan menghentikan sintesis RA endogen dalam model glomerulosklerosis segmental fokus memburukkan lagi albuminuria, kecederaan glomerular dan kematian [30]. Pentadbiran eksogen RA, meneutralkan aktiviti pengasingan albumin, membenarkan tindak balas penjanaan semulabuah pinggangnenek moyang, mewujudkan peningkatan dalam bilangan podosit dan peningkatanfungsi buah pinggang[30]. Keputusan terkini daripada Lasagni et al. [4] menyokong hipotesis bahawa pendekatan farmakologi yang meningkatkan tindak balas podosit kepada isyarat RA akan mengurangkan perkembangan eksperimen.kecederaan buah pinggang. Sesungguhnya, rawatan in vitrobuah pinggangprogenitor dengan RA dengan kehadiran 6-bromo-indirubin-30 -oxime (BIO), perencat glikogen synthase kinase 3 (GSK3), mendorong pembezaan yang kuat bagi manusiabuah pinggangprogenitor ke arah podosit melalui pengaktifan aktiviti transkripsi unsur tindak balas RA (RARE), iaitu, meningkatkan sensitiviti progenitor buah pinggang terhadap kesan pembezaan RA endogen. Peningkatan pembezaan progenitor buah pinggang ke dalam podosit dengan menggunakan BIO dalam model murine FSGS menghasilkan kesan penting pada penyakit itu, meningkatkan remisi penyakit dalam tikus yang dirawat. Dalam model tetikus peringkat progresif diabetes jenis 2 yang berkaitan dengan obesiti, BIO sebagai tambahan kepada perencatan dwi sistem renin-angiotensin (RAS)/pengangkut natrium-glukosa (SGLT)-2 dengan metformin, ramipril dan empagliflflozin melemahkan penurunan kadar penapisan glomerular (GFR) dengan mengurangkan lagi glomerulosklerosis, meningkatkan bilangan podosit melalui pengkhususan yang mengekalkan, serta mendorong pembezaan de novo daripada progenitor podosit dan meningkatkan ketumpatan celah fifiltrasi [31].
Endlich et al. menunjukkan peranan Dach1 (Dachshund homolog 1) dalam penentuan nasib sel PEC ke dalam podosit dan untuk fungsi podosit yang betul. Podocytes menyatakan tahap Dach1 yang tinggi dalam vivo dan in vitro, manakala PEC menyatakan tahap Dach1 yang sangat rendah. Penulis mendapati bahawa induksi ekspresi Dach1 dalam PEC secara signifikan mengimbangi synaptopodin dan WT1 protein khusus podocyte. Menariknya, Dach1 adalah sebahagian daripada rangkaian pengawalseliaan Eya-Six-Hox-Pax, dan pengawalseliaan ekspresi synaptopodin disertai dengan penurunan peraturan ekspresi Pax2 yang serentak [32].
Guhr et al. dianalisis oleh mekanisme yang manabuah pinggangnenek moyang mengekalkan potensi untuk mengekspresikan protein podosit di bawah keadaan patofisiologi dan menunjukkan bahawa ia mengandungi sistem ubiquitin-proteasome (UPS) yang diaktifkan yang membawa kepada degradasi pesat protein spesifik podosit yang baru disintesis [33]. Sebaliknya, UPS mengekalkan identiti podocyte dengan mengawal selia tahap protein khusus podocyte, seperti protein pengikat aktin -actinin 4 (ACTN4) dan synaptopodin (SYNPO), faktor transkripsi tumor Wilms 1 (WT1), podocin ahli keluarga stomatin, nefrin protein diafragma celah, protein penyesuai NCK1 dan protein kinase Cλ (PKCλ) diaktifkan [33]. Oleh itu, aktiviti UPS adalah penentu penting fenotip sel glomerular dan status pembezaan.Adalah diketahui umum bahawa, dalambuah pinggang,persekitaran mekanikal tertakluk kepada pengubahsuaian dalam model penyakit glomerular yang telah ditetapkan dan boleh menjejaskan keadaan dibezakan pelbagai jenis sel, termasuk podosit [34]. Kami baru-baru ini menganalisis kesan kekakuan substrat padabuah pinggangtingkah laku nenek moyang, menunjukkan bahawa, sekurang-kurangnya secara in vitro, fenotip manusiabuah pinggangprogenitor sangat bergantung pada modulus Young substrat, yang merupakan ukuran kekakuan bahan yang ditakrifkan sebagai nisbah tegasan kepada terikan, dengan substrat yang lebih keras menggalakkan percambahan dan penghijrahan progenitor buah pinggang. Kekakuan substrat memodulasi juga kapasitibuah pinggangprogenitor untuk membezakan ke arah podosit, dengan modulus Young 12 kPa menjadi optimum di kalangan yang dianalisis. Menggunakan perencat kimia dan genetik, kami menunjukkan bahawa aktiviti Rho kinase (ROCK) diperlukan untuk menengahi kesan kekakuan padabuah pinggangpercambahan progenitor, penghijrahan dan pembezaan [35]. Kekakuan glomerular yang berkurangan adalah ciri umum dari banyak bentuk kecederaan glomerular, termasuk FSGS [34,36], mencadangkan peranan penting untuk ROCK juga dalampenyakit buah pinggang.
Inhibitor sistem Renin angiotensin aldosteron (RAAS-I) adalah ubat yang berkesan dalam melambatkan perkembanganpenyakit buah pinggangmelalui pelbagai tindakan. Mekanisme yang bertanggungjawab untuk kesan terapeutik ubat-ubatan ini, serta merekabuah pinggangsasaran selular, telah banyak dikaji dalam beberapa model haiwan manusiapenyakit buah pinggang. Data terkini menunjukkan bahawa mereka juga mungkin menggunakan kesan berfaedah mereka dengan mempromosikanbuah pinggangpembezaan progenitor kepada podosit. Malah, dalam model tikus kecederaan glomerular, rawatan dengan ACE-I menyebabkan pengurangan proliferasi progenitor, pengurangan pembentukan bulan sabit dan mengelakkan perkembangan ke arah glomerulosklerosis [10]. Oleh itu, penyederhanaan pengaktifan sel progenitor oleh ubat memulihkan seni bina glomerular normal [10]. Menariknya, ekspresi reseptor angiotensin (Ang) II, AT1, terhad kepada CD24 ditambah PEC yang jarang berlaku pada manusia biasa.buah pinggangtetapi telah dikawal dalam lesi hiperplastik [37], mencadangkan sumbangan laluan reseptor Ang II/AT1 dalam mempromosikan abnormalbuah pinggangpenghijrahan progenitor dan percambahan dalam penyakit proliferatif [37]. Selaras, dalam pesakit yang terjejas oleh CGN (glomerulonefritis sabit), terapi ACE-I yang dikaitkan dengan regresi lesi hiperplastik dan menormalkan ekspresi reseptor AT1 padabuah pinggangnenek moyang. Keputusan ini memberikan penjelasan lain kepada kesan berfaedah yang diperhatikan selepas rawatan penyekat reseptor angiotensin II (ARB). Begitu juga, rawatan ARB meningkatkan hasil dalam model tikus glomerulonefritis proliferatif mesangial, mendorong peningkatan bilangan PEC yang menyatakan penanda sel stem [38].
Kecederaan pada podosit dianggap sebagai penyumbang penting kepada diabetespenyakit buah pinggangkemajuan ke peringkat akhirpenyakit buah pinggang[39–41]. Suganami et al. melaporkan pencegahan dan pembalikankecederaan buah pinggangoleh pentadbiran leptin dalam model haiwan nefropati diabetik [39]. Baru-baru ini, Pichaiwong et al. menunjukkan bahawa menggantikan leptin boleh membalikkan parameter struktur dan fungsi nefropati diabetes lanjutan dalam tetikus ob/ob BTBR kekurangan leptin [41]. Khususnya, rawatan leptin, tetapi bukan RAAS-I, menghasilkan peningkatan yang ketara dalam ketumpatan dan bilangan podosit dan peningkatan WT1-positif PEC yang membiak. Mekanisme yang mendasari proses ini dihuraikan lebih lanjut dalam kertas susulan, di mana ia menunjukkan bahawa rawatan dwi tikus ob/ob kekurangan leptin dengan antagonis terpilih reseptor jenis A (ETAR) endothelin-1 dalam kombinasi dengan perencatan RAAS membawa kepada fenotip yang lebih baik [40], dicirikan oleh pengaktifan PEC dan peningkatan bilangan podosit. Keputusan ini memberikan bukti tidak langsung bahawa PEC mungkin merupakan takungan yang berpotensi untuk memulihkan podosit yang hilang dan bahawa kapasiti pembezaan PEC mungkin merupakan elemen utama untuk regresi nefropati diabetik yang mungkin dimodulasi secara farmakologi.
Pengawal selia Glomerular Progenitors dalam Patologi: Apabila Orkestra Tidak Sesuaimanakalabuah pinggangnenek moyang boleh memacu penjanaan semula podosit berikutan kecederaan [4], mereka juga boleh menghasilkan lesi proliferatif extracapillary atau bulan sabit yang merupakan ciri kedua-dua penyakit glomerular inflamasi dan bukan radang [42]. Malah, bukti dalam model eksperimen [15] dan dalam biopsi manusia menunjukkan bahawa bulan sabit terdiri daripadabuah pinggangnenek moyang [14] yang secara tidak normal mengalihkan tindak balas mereka daripada reparatif kepada mencederakan. Ia tidak difahami sepenuhnya faktor mana yang bertanggungjawab untuk menyengetkan imbangan. CGN adalah penyakit berciri terbaik di manabuah pinggangnenek moyang adalah penyebab utama. Bulan sabit selular ialah perubahan morfologi biasa yang diperhatikan dalam CGN. Ia ditakrifkan sebagai pengumpulan berbilang lapisanbuah pinggangprogenitor dan jenis sel lain dalam ruang Bowman. Akibatnya, ia menutup saluran keluar kencing dan aliran air kencing primer, dan kemudiannya, nefron yang terlibat terjejas. Pecah kapilari glomerular dalam penyakit bulan sabit membawa kepada pendedahanrenal nenek moyang kepada kepekatan plasma yang tinggi yang secara mendadak meningkatkan pembiakan manusiabuah pinggangnenek moyang dalam budaya [43]. Beberapa komponen plasma boleh menyumbang kepada pembentukan bulan sabit, tetapi, pada masa ini, terdapat data yang konsisten hanya untuk pengaktifan fifibrinogen, ahli lata koagulasi yang diaktifkan semasa kecederaan vaskular. Kekurangan fifibrinogen atau fifibrinolisis menghalang pembentukan bulan sabit dalam beberapa model tikus [43,44].

Nefropati dan pseudoccrescent yang runtuh juga berasal daribuah pinggangnenek moyang [14]. Pada perbezaan dengan bulan sabit, adalah dicadangkan bahawa pseudoccrescents berasal daribuah pinggangprogenitor sebagai tindak balas yang tidak terkawal terhadap detasmen podosit yang besar dan cepat yang berlaku dalam keadaan tertentu kecederaan podosit langsung (seperti pendedahan kepada ubat tertentu, gangguan pengantara imun atau jangkitan yang menyasarkan secara langsung podosit) yang berlaku tanpa ketiadaan komponen keradangan dan membawa kepada keruntuhan kapilari [22,45]. Lesi ini juga kerap diperhatikan dalam glomerulopati virus, seperti HIV- dan parvovirus-nefropati [22]. Dalam glomerulopati virus ini, interferon (IFN-)- dan IFN- bukan sahaja mencetuskan keradangan tempatan di dalam glomerulus tetapi, juga, bertindak ke atas PEC dan podosit, dengan IFN- menghalang penghijrahan PEC dan kedua-duanya menekanbuah pinggangpembezaan progenitor kepada podosit secara in vitro [46]. Dalam vivo, dalam model nefropati Adriamycin, suntikan sama ada IFN- atau IFN- memburukkan proteinuria dan glomerulosklerosis [46]. Baru-baru ini, FSGS yang runtuh telah diterangkan pada pesakit keturunan Afrika baru-baru ini dengan genotip APOL1 berisiko tinggi dan dijangkiti sindrom pernafasan akut teruk coronavirus 2 (SARS-CoV-2) [47,48]. Telah dicadangkan bahawa SARS-CoV-2 boleh menjangkiti secara langsung podosit [49] dan/atau mencetuskan lata keradangan yang melibatkan pengaktifan laluan interferon-kemokin, yang seterusnya, berinteraksi dengan gen varian APOL1 [ 50]. Seperti yang dinyatakan di atas,buah pinggangpembezaan progenitor kepada podosit yang dikaitkan dengan ekspresi APOL1 dan oleh itu boleh terlibat dalam penyakit coronavirus 2019 (COVID{2}}) nefropati yang berkaitan.
Beberapa kajian baru-baru ini menyerlahkan peranan penting untuk ekspresi de novo CD9 dan, seterusnya, CD44 sebagai suis patogenik PEC daripada senyap kepada fenotip diaktifkan dalam CGN dan dalam FSGS [16,51,52], mengesahkan peranan patogenik. PEC dalam penyakit ini dan menawarkan sasaran molekul baharu untuk terapi penyakit glomerular. Bagi menyokong idea ini, Kaverina et al. menunjukkan bahawa PEC kehilangan ekspresi CD44 apabila membezakan menjadi podosit dalam glomeruli tikus tua yang cedera, menunjukkan bahawa peningkatan CD44 dalam PEC mewakili bukan regeneratif tetapi peralihan patologi [53]. Dalam FSGS, CD44 telah ditunjukkan mempunyai peranan penting dalam penghijrahan sel ke arah penghalang fifiltrasi yang cedera, di mana podosit yang cedera mengimbangi faktor perencatan migrasi (MIF) dan faktor terbitan sel stromal 1 (SDF1) yang merangsang ekspresi CD44 dan CD{{12} }pengantara penghijrahan [54]. Selain itu, PEC menghasilkan kedua-dua isoform protein matriks ekstraselular ekstraselular yang berasal dari PEC dan podosit dalam{16}}cara bergantungan CD [55]. Akhirnya, kajian pengesanan keturunan PEC mencadangkan bahawa CD44 tidak mengambil bahagianbuah pinggangpenjanaan semula melalui pembezaan ke dalam podosit dan hanya mengambil bahagian dalam laluan pro-fifibrotik [56].
Tubular Progenitors
buah pinggangprogenitor dari lapisan epitelium parietal kapsul Bowman berpotensi menjana semula sel epitelium tubular proksimal di persimpangan glomerulotubular [57]. Walau bagaimanapun, progenitor komited tiub yang bertaburan di tubul proksimal dan distal juga wujud pada manusia [6,58-60] dan pada tikus [5,61-63] dan meningkat apabila kecederaan tiub pada pesakit yang terjejas dengan kerosakan tiub akut atau kronik [6 ]. Kumar et al. melakukan pengesanan garis keturunan sel pengekspresi Sox9-yang jarang berlaku dalam tubul proksimal dan mengenal pasti mereka sebagai populasi progenitor tubular yang diduga terlibat dalam postacutekecederaan buah pinggang(AKI) pemulihan [64]. Sox9 ialah faktor transkripsi yang, dalambuah pinggangpembangunan, mengawal cawangan epitelium dan dinyatakan dalam prekursor nefron [64,65]. Menariknya, apabila Sox9 tersingkir dari segmen S1 dan S2, pemulihan fisiologi yang lebih perlahanfungsi buah pinggang, kecederaan tiub dipertingkatkan, serta meningkatbuah pinggangfifibrosis, berlaku [64]. Selepas nefrektomi separa, sel Sox9 plus membiak dan menjana sel epitelium tubul proksimal, gelung Henle, tubul distal, saluran pengumpul dan lapisan parietal glomerulus [66]. Baru-baru ini, Lazzeri et al. memberikan bukti bahawa progenitor tubular menjalani mitosis dan menggantikan kira-kira separuh daripada sel tubular yang hilang secara tidak dapat dipulihkan semasa AKI [5]. Menjalankan pengesanan garis keturunan sel Pax2 plus dalam model tetikus kecederaan tubular, mereka mengenal pasti progenitor tubular sebagai subpopulasi sel tubular yang berbeza yang tahan terhadap kematian dan menunjukkan aktiviti klonogenik yang tinggi, yang membawa kepada penjanaan segmen tubul panjang [5].
Pengatur Fisiologi Leluhur Tubular: Koir Polifonik
Manusiabuah pinggangprogenitor mengekspresikan limfoma B Mo-MLV (Moloney murine leukemia virus) kawasan sisipan 1 (Bmi-1) [57]. Bmi-1 ialah ahli keluarga policomb penindas transkrip. Ia terlibat dalam pengawalan kitaran sel dan penuaan sel stem endogen kepada pelbagai organ, seperti prostat, usus kecil dan paru-paru [67-70]. Di dalambuah pinggang, tahap BMI-1 meningkat dengan cepat berikutan kecederaan dalam model tetikus AKI [71]. Pertemuan ini menunjuk ke arah penglibatan Bmi-1 yang dinyatakan dalam progenitor tubular dalambuah pinggangpenjanaan semula. Sesungguhnya, Lv et al. menunjukkan bahawa nekrosis tubular akut membawa kepada peningkatan Bmi-1 dan mobilisasi progenitor tubular seterusnya dalam tikus jenis liar, manakala progenitor tiub tidak digerakkan dalam Bmi-1 tikus kalah mati [72]. Bmi-1 tikus kalah mati menunjukkan yang kuatbuah pinggangfenotip, termasuk fifibrosis interstisial, atrofi tiub dan terukbuah pinggangdisfungsi, dengan penurunan percambahan sel, peningkatan apoptosis dan penuaan sel dan infifiltrasi sel radang [72,73]. Dalam kajian baru-baru ini, Zhou et al. menjelaskan lagi peranan Bmi-1 dalambuah pinggangnenek moyang, menunjukkan bahawa Bmi-1 mengekalkan pembaharuan diri dan kekukuhanbuah pinggangprogenitor dengan mengekalkan keseimbangan redoks dan mencegah penangkapan kitaran sel, melalui perencatan spesies oksigen reaktif (ROS), p16 dan p53 [74].
Satu lagi molekul penting yang terlibat dalam pengawalan progenitor tiub ialah reseptor seperti Toll 2 (TLR2), atau CD282, protein membran terpelihara evolusi yang memainkan peranan penting dalam pengecaman patogen dan pengaktifan imuniti semula jadi. TLR2 bertindak sebagai penderia kecederaan tisu melalui pengesanan molekul corak molekul (DAMP) berkaitan kerosakan yang dikeluarkan oleh tisu yang rosak. Pengaktifan TLR2 membawa kepada pengaktifan faktor transkripsi hiliran yang mengawal ekspresi gen kemandirian atau sitokin dan kemokin proinflflammatory [75-77]. Sallustio et al. menunjukkan bahawa progenitor tiub mengekspresikan TLR2, yang rangsangannya oleh agonis yang meniru mediator inflamasi atau DAMP mendorong rembesan besar-besaran protein kemoattraktan monosit-1 (MCP-1), interleukin 6 (IL-6), interleukin 8 (IL-8) dan melengkapkan komponen C3 melalui pengaktifan NF-κB (faktor nuklear kappa-light-chain-enhancer sel B diaktifkan) [59]. Selain itu, rangsangan TLR2 memodulasi kadar percambahan dan kapasiti pembezaan progenitor tiub, mencadangkan peranan penting dalambuah pinggangpembaikan [59]. Kajian susulan oleh kumpulan yang sama mengenal pasti set miRNA yang berbeza yang dinyatakan secara khusus dalam progenitor tiub [78]. Antaranya, miR-1915 dan miR-1225-5p mengawal ekspresi CD133 dan PAX2, serta TLR2. Sallustio et al. kemudian membedah mekanisme pemulihan berikutan AKI dan mendapati peranan penting untuk TLR2 dalambuah pinggangpenjanaan semula [79]. Mereka menetapkan bahawa, selepas kecederaan, penderiaan kerosakan TLR2 membawa kepada rembesan inhibin-A dan decorin oleh progenitor tiub, yang seterusnya, menggalakkan pertumbuhan semula tiub melalui percambahan sel [79]. Kedua-dua sitokin ini tergolong dalam laluan isyarat TGF- (transforming growth factor-) dan terlibat dalam pengawalan kitaran sel, peningkatan percambahan sel dan perencatan apoptosis [80-84].
Ekspresi molekul dari laluan Wnt telah dilaporkan pada orang dewasabuah pinggangnenek moyang pada tikus [85] dan manusia [86]. Menggunakan model tetikus pengesanan keturunan, Rinkevich et al. menunjukkan bahawa, semasa homeostasis dan selepas kecederaan, mamalia dewasabuah pinggangmenjalani pengembangan klon khusus segmen daripada sel yang diperoleh daripada prekursor responsif WNT [63]. Mereka mencadangkan bahawa keupayaan untuk bertindak balas kepada isyarat WNT memilih untuk sel yang akhirnya akan menjalankan pengembangan klon yang mantap. Kajian dalam ENAM2 ditambah dengan air kencingbuah pinggangprogenitor menunjukkan bahawa pengaktifan laluan WNT oleh perencatan GSK3 mendorong pembezaanbuah pinggangnenek moyang ke dalam buah pinggangsel tubular proksimal epitelium [87]. Di samping itu, Wnt3 memberikan kesan pro-regeneratif dan dikawal selia dalam CD133 plusbuah pinggangprogenitor dalam model in vitro kecederaan cisplatin [88]. Dalam kajian ini, penulis mendedahkan peranan fungsi CD133 itu sendiri dalam pembaikan tiub buah pinggang melalui penyelenggaraan tindak balas proliferatif dan kawalan penuaan dengan bertindak sebagai faktor permisif untuk isyarat -catenin, menghalang degradasinya dalam sitoplasma [88]. Dalam ikan zebrafibuah pinggang,tubul yang rosak digantikan oleh nefron baru daripadabuah pinggangnenek moyang yang menyatakan reseptor Wnt frizzled9b dan faktor transkripsi lef1. Berikutan kecederaan, ekspresi ligan Wnt Wnt9a dan Wnt9b telah diinduksi dalam kecederaanbuah pinggangdi tapak di mana sel progenitor membentuk nefron baru [89]. Keputusan ini menunjukkan bahawa peranan penting laluan isyarat Wnt/frizzled dalambuah pinggangpenjanaan semula sangat terpelihara di kalangan spesies.

CISTANCHE AKAN MEMPERBAIKI PENYAKIT BUAH PINGGANG/PINGGANG
Seperti yang dinyatakan sebelum ini, isyarat Notch ialah laluan pemuliharaan evolusi yang mempunyai peranan penting dalamkecederaan buah pinggangdan pembaikan [24,90–93], terutamanya semasa AKI [94,95]. Kang et al. menunjukkan bahawa Sox9 plusbuah pinggangnenek moyang menyatakan tahap Notch yang tinggi, dan ekspresi berlebihan domain intraselular Notch1 (NICD1) dalam populasi Sox9 plus meningkatkanbuah pingganghistologi dalam model AKI yang disebabkan oleh asid folik [62]. Ma et al. melaporkan bahawa pengaktifan Sox9 plus progenitor buah pinggang, yang peranannya penting dalambuah pinggangpembaikan, telah dimediasi oleh laluan Notch, mengesahkan laporan sebelumnya bahawa tahap ekspresi Notch1-3, Jagged1/2, Dll4 dan Sox9 meningkat selepas kecederaan reperfusi iskemia (IRI) [66]. Malah, dalam organ lain seperti pankreas, pengaktifan Sox9 memodulasi laluan Notch dengan mengawal Hes1 untuk mengekalkan kumpulan sel progenitor [96]
Beberapa ubat telah ditunjukkan untuk bertambah baikbuah pinggangpenjanaan semula, dan, antaranya, perencat histon deacetylase (HDAC) (HDACis) mungkin merupakan pilihan terapeutik yang menjanjikan untuk rawatan AKI [97-102]. HDAC membentuk kumpulan enzim yang terlibat dalam pelbagai proses selular dengan mengeluarkan kumpulan asetil daripada protein histon atau bukan histon [103]. Marumo et al. melaporkan pengurangan dalam aktiviti HDAC5, peningkatan asetilasi histon dan pengaktifan semula protein morfogenetik tulang 7 (BMP-7) dalam sel tubular proksimal semasa fasa pemulihan berikutanbuah pinggangIRI [104]. Pemerhatian ini mencadangkan bahawa HDACis mungkin memberi kesan yang bermanfaat padabuah pinggangpemulihan melalui peningkatan ekspresi BMP-7, protein yang mengekalkan kumpulan progenitor buah pinggang dalam status tidak dibezakan semasabuah pinggangpembangunan [105]. Menariknya, rawatan dengan HDACis memperluaskanbuah pinggangpopulasi sel progenitor dalam zebrafifish [106]. Dalam model nefritis serum nefrotoksik bagiglomerulonephritis pada tikus, rawatan trichostatin A (TSA) diaktifkanbuah pinggangsel populasi sampingan (SD) [107]. Sel SD membentuk subset sel dengan potensi multilineage dan sifat renoprotektif yang diketahui yang melemahkan kronikpenyakit buah pinggang(CKD) melalui peningkatan ungkapan BMP-7 [107]. Menggunakan pendekatan pengesanan keturunan yang diterangkan di atas, Lazzeri et al. menunjukkan bahawa rawatan dengan dua HDAC yang digunakan secara meluas, TSA dan 4-fenilbutirat (4-PBA), membawa kepada pembiakan Pax2 ditambah progenitor, seterusnya mengelakkan perkembangan fifibrosis tisu dan CKD [5]. Pembangunan HDACis terpilih, dengan keberkesanan yang dipertingkatkan dan kurang ketoksikan, akan bertambah baikbuah pinggangpemulihan melalui percambahan progenitor tiub. Nota, HDAC telah menunjukkan kesan terapeutik yang bermanfaat dalam banyak model eksperimenpenyakit buah pinggangselain AKI, termasuk glomerulosklerosis, fifibrosis tubulointerstitial, keradangan glomerular dan tubulointerstitial, lupus nefritis, polikistikpenyakit buah pinggangdanbuah pinggangkarsinoma sel (RCC), seperti yang disemak dalam [108]. Beberapa HDAC sedang dalam ujian Fasa 1 atau 2 untuk rawatan RCC dan gangguan buah pinggang (clinicaltrial.org).
Pengawal selia Leluhur Tubular dalam Patologi: Koir Cacophonus
Ciri biologi dan molekulbuah pinggangkanser mencadangkan bahawabuah pinggangnenek moyang boleh menjadi asal usul pembangunan yang berbezabuah pinggangjenis tumor. Dalam kajian baru-baru ini, Peired et al. menunjukkan manusia itubuah pinggangnenek moyang yang mengekspresikan NICD1 secara berlebihan mempunyai kapasiti proliferatif yang meningkat dan membentuk mitosis yang menyimpang dalam budaya 2D dan boleh menghasilkan jisim seperti tumor dalam budaya 3D [8]. Begitu juga, Pax2 plusbuah pinggangprogenitor yang terlalu mengekspresikan NICD1 berikutan induksi transgen pada tikus dewasa atau mengikuti IRI adalah pada asal adenoma papillary dan RCC [8]. Dalam pengesahan fifinding ini, rawatan yang menyekat pengaktifan NOTCH1 yang disebabkan oleh AKI endogen membawa kepada perkembangan tumor yang lebih sedikit [8]. Baru-baru ini, dua kajian mencadangkan bahawa angiomyolipomas berasal dari pelbagai potensibuah pinggangsel epitelium disetempat di dalam tubul dan mengalami pengembangan klon sebagai tindak balas kepada penghapusan gen kompleks sklerosis tuberous (TSC) [109,110]. Kedua-dua kajian mencadangkan sel-sel ini bolehbuah pinggangnenek moyang dengan kapasiti pembezaan multilineage [109,110]. Menariknya, Cho et al. mendedahkan bahawa pengaktifan gelung kawal selia Rheb-Notch-Rheb yang tidak dilaporkan sebelum ini, di mana pengikatan kitaran Notch1 kepada elemen responsif Notch (NREs) pada promoter Rheb adalah peristiwa penting, merupakan mekanisme utama di sebalik penjanaan pelbagai keturunan hadir dalam angiomiolipoma [109]. Secara keseluruhan, keputusan ini menunjukkan bahawa penyahkawalseliaan laluan Notch masukbuah pinggangnenek moyang boleh membawa kepadabuah pinggangpatologi.
Wan et al. memerhatikan bahawa ekspresi SOX9 dikawal selia dalam pesakit RCC dan dikaitkan dengan gred patologi lanjutan [111]. Pesakit RCC dengan tahap SOX9 yang tinggi juga mempunyai kelangsungan hidup yang lebih pendek [111]. Data ini mengesahkan kajian terdahulu yang mengaitkan ekspresi SOX9 dengan penggredan RCC Fuhrman dan menunjukkan bahawa pesakit dengan SOX9 ( ) mempunyai tindak balas terapeutik yang lebih baik terhadap perencat tyrosine kinase berbanding mereka yang mempunyai SOX9 ( tambah ) [112]. Oleh itu, kita boleh membuat hipotesis bahawa peningkatan ekspresi SOX9 dalam SOX9 plusbuah pinggangnenek moyang boleh menyumbang kepada pembangunan RCC. Mekanisme yang sama diterangkan dalam kanser payudara seperti basal, di mana ekspresi SOX9 dalam sel stem / progenitor luminal boleh mengawal keplastikan keturunan untuk kanser melalui pengaktifan isyarat NF-κB [113].
Tinjauan tentang Masa Depan Leluhur Renal
Penjujukan RNA Sel Tunggal: Biarkan Kami Selaras dengan MasaPerkembangan pantas scRNAseq membuka perspektif baharu untuk membedah proses molekul yang terlibat dalambuah pinggangperaturan progenitor dalam keadaan fisiologi dan patologi. ScRNAseq terdiri daripada mendapatkan profiiling ekspresi gen pada resolusi sel tunggal, meletakkan bukti keadaan selular yang berbeza dan dinamik molekul walaupun subpopulasi yang lebih jarang. Teknologi baru ini telah berjaya digunakan dalam beberapa organ—contohnya, untuk mengkaji Prominin 1 plus progenitor hati [114], Dach1–downregulated limfoid progenitor [115] dan KTR5 plus lung progenitor dalam pesakit COVID-19 [116]. Dalam beberapa tahun kebelakangan ini, semakin banyak kumpulan penyelidikan telah menggunakan strategi ini untuk menentukan populasi selbuah pinggangpada tikus dan manusia [117–120]. Dalam kajian yang sangat baru-baru ini, Rudman-Melnick et al. mengenal pasti tandatangan transkrip semua populasi sel dalam model eksperimen AKI, menonjolkan kehadiran molekul berkaitan kecederaan yang tidak dijelaskan sebelum ini [119]. Pendekatan sedemikian berpotensi mendedahkan mekanisme baru yang diaktifkanbuah pinggangprogenitor yang mengikuti AKI, yang membawa kepada pengenalpastian sasaran molekul yang berpotensi. Dalam kertas mani mereka, Young et al. dapat memadankan sel jernih dan sel RCC papillary kepada subtipe sel tubular berbelit proksimal yang ditakrifkan oleh ungkapan SLC17A3 dan VCAM1 [117]. Seperti yang dinyatakan sebelum ini, ungkapan VCAM1 atau CD106 mencirikan, bersama-sama dengan CD133, populasi yang jarang ditemuibuah pinggangprogenitor tersebar kebanyakannya dalam tubul proksimal [6]. Analisis data scRNAseq mendedahkan bahawa transkriptom progenitor buah pinggang manusia menunjukkan persamaan dengan PT1, sel asal usul RCC papillary manusia [8]. Pemerhatian ini menyokong hipotesis kami bahawa RCC papillary berasal daripada transformasi dan percambahan pengantaraan Notch bagi populasi tubul proksimal progenitor buah pinggang [8].
Aplikasi Klinikal: The Clinic Calls the Tune
Terapi berasaskan nenek moyang buah pinggang mewakili sempadan baharu yang menjanjikan dalam rawatanpenyakit buah pinggang, kerana beberapa kajian mencadangkan bahawa mereka bertambah baikfungsi buah pinggangberikutan kecederaan [121]. Walau bagaimanapun, menyuntikbuah pinggangnenek moyang terus ke dalam model haiwan bagikecederaan buah pingganguntuk mendorong penjanaan semula tisu memberikan batasan penting yang telah didedahkan di tempat lain [121]. Kaveat ini boleh dielakkan berkat sifat yang baru dieksploitasibuah pinggangprogenitor, iaitu keupayaan mereka untuk merembeskan faktor trofik, sitokin atau kemokin yang secara cekap menjadi pengantara.buah pinggangpembaikan secara paracrine atau autokrin (Rajah 2). Kenji et al. melaporkan bahawa suntikan intraperitoneal supernatan kultur diperolehi daripada tikus dewasabuah pinggangnenek moyang secara signifikan menindas apoptosis sel tiub sisabuah pinggangsel, mengurangkan keradangan dan menggalakkan percambahan sel tidak matang dalam model IRI eksperimen melalui pembebasan HGF (faktor pertumbuhan hepatosit), EGF (faktor pertumbuhan epidermis), TGF- dan Epo (erythropoietin) [122]. Malah, penggunaan terapeutik pelbagai faktor pertumbuhan telah dilaporkan membaikkecederaan buah pinggang, seperti HGF, BMP7, EGF, TGF- dan VEGF (faktor pertumbuhan endothelial vaskular) [123-127]. Sallustio et al. melaporkan bahawa manusiabuah pinggangnenek moyang bukan sahaja secara signifikan membaiki sel-sel tubular yang rosak tetapi, juga, mempamerkan kesan antififibrotik melalui rembesan CXCL6 (ligan chemokine motif CXC 6), SAA2 (serum amiloid A2), SAA4 (serum amiloid A4) dan BPIFA2 (BPI (ketelapan bakteria). -meningkatkan) keluarga yang mengandungi lipatan Seorang ahli 2) melalui mekanisme paracrine [128]. Aggarwal et al. melaporkan bahawabuah pinggangrembesan progenitor had Epobuah pinggangfifibrosis selepas kecederaan tiub [129]. Sebagai tambahan kepada faktor larut, progenitor buah pinggang merembeskan vesikel ekstraselular (EV), zarah dibatasi dwilapisan lipid bersaiz nanometer yang membawa lipid bioaktif, protein dan RNA yang membolehkan komunikasi sel-tosel melalui tindakan paracrine. Jenis EV yang paling kecil dan paling diterangkan ialah eksosom, yang baru-baru ini telah disiasat untuk kesan perlindungannya terhadap AKI yang disebabkan oleh IRI [130,131]. Li et al. menunjukkan bahawa eksosom yang berasal dari progenitor buah pinggang boleh memulihkan struktur dan fungsi buah pinggang melalui kebolehan rangsangan imunomodulator, antiapoptosis dan proliferasi dalam model AKI. MikroRNA (miRNA) ialah komponen eksosom yang paling banyak, dan di antaranya, miR-146a dikenal pasti sebagai pemain utama dalam pengantaraan kesan sitoprotektif dengan merendahkan isyarat IRAK1 (interleukin 1 receptor related kinase 1)/NF-kB. [130]. Dalam model nefropati diabetik, eksosom yang dirembeskan nenek moyang kencing didapati mengurangkan apoptosis podosit dengan menyekat caspase-3 dan menggalakkan penjanaan semula vaskular, yang mungkin berkaitan dengan sitokin VEGF, TGF- 1, angiogenin dan BMP -7 terkandung dalam eksosom terbitan progenitor kencing [132]. Perencatan apoptosis podocyte juga berkaitan dengan ekspresi berlebihan miR-16-5p dalam eksosom yang dirembeskan progenitor kencing dengan menekan VEGF-A [133].
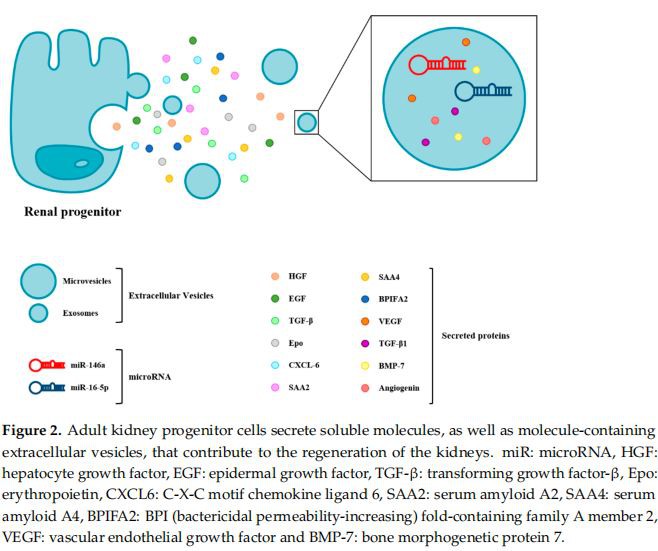
Molekul dan eksosom dirembeskan olehbuah pinggangnenek moyang menggalakkan pemulihan daripadapenyakit buah pinggangmelalui keupayaan mereka untuk menggunakan satu siri kesan renoprotektif dan penjanaan semula terima kasih kepada daya imuniti yang berkurangan dan risiko yang lebih rendah untuk maldifferentiation dan tumorigenesis berbanding terapi sel. Ciri-ciri luar biasa ini menjadikannya menarik untuk aplikasi klinikal. Satu lagi cabaran dalam pendekatan klinikal untukpenyakit buah pinggangialah penemuan alat baharu untuk mendiagnosis dan memantaupenyakit buah pinggangyang boleh diakses dengan mudah dengan prosedur bukan invasif. Dalam konteks ini, air kencing mewakili biobendalir yang berharga kerana kebolehcapaiannya, pensampelan yang cepat dan mudah serta pelbagai jenis protein, metabolit, sel dan kandungan selular yang dikeluarkan daripada saluran urogenital [134]. Kehadiran sel dalam air kencing yang memaparkan sifat sel stem pertama kali diterangkan oleh Zhang et al. pada tahun 2008 [135]. Pada tahun-tahun berikutnya, beberapa kumpulan telah membangunkan teknik untuk mengasingkan dan mencirikan progenitor yang diperoleh daripada air kencing daripada penderma yang sihat dan pesakit denganbuah pingganggangguan [136]. Belum ada konsensus rasmi yang dicapai mengenai penanda yang boleh digunakan untuk mentakrifkan progenitor terbitan air kencing. Kebanyakan kajian menunjukkan bahawa mereka mengekspresikan penanda sel stem mesenchymal (CD44, CD73 dan VIM) dan penanda sel stem (seperti POU5F1, SSEA4 dan TRA-1-81, serta CD117) tetapi tiada penanda yang berasal dari hematopoietik atau urothelium. garis keturunan sel dan tahap rendah penanda khusus tubular atau podocyte [136]. Mengenai asal-usul mereka, Bharadwaj et al. menunjukkan bahawa air kencing yang diperolehibuah pinggangnenek moyang membawa kromosom Y dalam lelaki ke perempuanpemindahan buah pinggangpenerima, menunjukkan bahawa mereka berasal daribuah pinggang[137]. Sel-sel ini mempunyai keupayaan untuk membezakan menjadi podosit [138] dan menyatakan penanda protein khusus podosit dan PEC [137,139], menunjukkan bahawa ia berasal daripada PEC. Analisis transkriptom perbandingan air kencing yang diperolehibuah pinggangnenek moyang danbuah pinggangberasal dari biopsibuah pinggangsel proksimal epitelium mengesahkan identiti progenitor buah pinggang progenitor yang berasal dari air kencing [87], menunjukkan bahawa mereka juga boleh berasal dari progenitor tubular yang bertaburan. Sel-sel ini boleh diprogramkan semula menjadi sel stem pluripotent teraruh (iPSC) dan digunakan untuk ubat regeneratif, pemodelan penyakit atau ujian farmakologi [140,141].
Baru-baru ini, telah dicadangkan bahawa ungkapan daripadabuah pinggangpenanda progenitor CD133 dalam EV kencing mewakili penanda yang baik untuk penilaian status fungsi petak tiub renal dan kehadiran sel dengan aktiviti proliferatif dan pembaikan dalam tubul selepas kecederaan. Malah, dua kajian melaporkan bahawa CD133 ditambah tahap EV kencing, meningkat dalam subjek yang sihat, bukan sahaja berkurangan pada pesakit dengan kerosakan tiub akut [142] tetapi, juga, dalam keadaan glomerular akut dan kronik [143]. Tambahan pula, kehadiran progenitor buah pinggang sendiri dalam air kencing mungkin mencerminkan status patofisiologibuah pinggangtisu. Khususnya, Manonelles et al. memberikan bukti bahawa pengasingan CD133 ditambah CD24 ditambah progenitor buah pinggang daripada air kencing penerima allograf yang stabil pada enam bulan boleh meramalkan hasil jangka panjang yang buruk daripada pemindahan pada dua tahun [144]. Proliferasi dan penghijrahan progenitor buah pinggang dari kapsul Bowman ke jumbai glomerular merentasi ruang kencing untuk menggantikan podosit yang terpisah boleh menjelaskan perkumuhan progenitor buah pinggang dan, jika dikekalkan dari masa ke masa, mungkin gagal untuk mengekalkan fungsi allograft, mengakibatkan penurunan GFR, albuminuria dan perkembangan lesi histologi glomerular kronik [144].
Bersumberkan air kencingbuah pinggangsel juga boleh menjadi alat diperibadikan yang berkuasa untuk kajian berfungsi pada varian calon dalam warisanpenyakit buah pinggang. Seperti yang diterangkan oleh Lazzeri et al., air kencing yang diperolehibuah pinggangprogenitor yang diperoleh daripada pesakit yang membawa mutasi patogen dalam pengekodan gen untuk protein podocyte berkembang dalam budaya tetapi membangunkan anomali dalam ekspresi atau penyetempatan protein podocyte berikutan pembezaan podocyte [138]. Selaras dengan bukti ini, teknik yang sama digunakan untuk menunjukkan patogenik varian gen NPHS1 yang tidak diketahui kepentingannya dalam pesakit dengan nefritis lupus refraktori [145]. Satu lagi kajian menggariskan kemungkinan untuk menggunakan sel epitelium buah pinggang yang berasal dari air kencing untuk menjalankan kajian RNA dan fungsi padabuah pinggang-gen spesifik, mengesahkan patogenik varian sinonim dalam PKHD1 (polikistikbuah pinggangdan penyakit hepatik 1) dan mengesahkan diagnosis genetik ARPKD (Autosomal Recessive PolycysticPenyakit buah pinggang) pada pesakit dengan CKD yang dikaitkan dengan polikistik atipikalbuah pinggang [146].
Kesimpulan
Sebilangan besar literatur menerangkan pelbagai mekanisme pengawalseliaanbuah pinggangprogenitor dalam glomerular dan dalam petak tiub, membolehkan kita mempunyai penglihatan global tentang kerumitan proses molekul yang berlaku dalam keadaan fisiologi dan patologi. Mengetahui tandatangan molekul bagibuah pinggangnenek moyang membuka pintu untuk mengenal pasti sasaran baharu untuk dikekalkan oleh ubatbuah pinggangpenjanaan semula atau biomarker untuk dipantaubuah pinggangkesihatan.
