Interaksi Sel-sel Penghuni Imun dan Buah Pinggang dalam Pembentukan Struktur Limfoid Tertiari dalam Lupus Nefritis
Mar 14, 2022
untuk maklumat lanjut:ali.ma@wecistanche.com
Simin Jamaly et al
ABSTRAK
buah pinggangpenglibatan memberikan morbiditi dan kematian yang ketara pada pesakit dengan sistemik lupus erythematosus (SLE). Patogenesis lupus nefritis (LN) melibatkan pelbagai mekanisme yang dicetuskan oleh unsur-unsur tindak balas autoimun yang mengubah biologibuah pinggangsel pemastautin. Proses dalam glomeruli dan interstitium boleh diteruskan secara bebas walaupun crosstalk antara kedua-duanya tidak dapat dielakkan. Podosit, sel mesangial, sel epitelium tiub,buah pinggangmakrofaj pemastautin, dan sel stroma dengan input daripada sitokin dan autoantibodi yang terdapat dalam peredaran mengubah ekspresi enzim, menghasilkan sitokin dan kemokin yang membawa kepada kecederaan dan kerosakanbuah pinggang. Beberapa molekul ini boleh disasarkan secara bebas untuk mencegah dan membalikkan kegagalan buah pinggang. Struktur limfoid tertier dengan pusat germinal sejati terdapat pada buah pinggang pesakit lupus nefritis dan semakin dikenali untuk dikaitkan dengan yang lebih miskin.buah pingganghasil. Sel stromal, sel epitelium tiub, salur endothelial tinggi, dan sel venula limfa menghasilkan kemokin yang membolehkan pembentukan struktur yang terdiri daripada zon kaya sel T dengan sel dendritik matang bersebelahan dengan folikel sel B dengan ciri-ciri pusat germinal. dikelilingi oleh sel plasma. Berikutan gambaran keseluruhan tentang interaksi sel imun dengan sel pemastautin buah pinggang, kami membincangkan peristiwa selular dan molekul yang membawa kepada pembentukan struktur limfoid tertier dalam interstitiumbuah pinggangtikus dan pesakit lupus nefritis. Secara selari, molekul dan proses yang boleh disasarkan secara terapeutik dibentangkan.

Klik untuk Cistanche DHT untuk penyakit buah pinggang
pengenalan
Systemic lupus erythematosus (SLE) adalah penyakit autoimun dengan kepelbagaian klinikal yang mengagumkan yang hadir dengan manifestasi daripada pelbagai organ. Banyak laluan patogenik telah dikenal pasti berpunca daripada faktor genetik, epigenetik, hormon, persekitaran, dan imunoregulasi dan semuanya berkumpul menyebabkan keradangan tisu dan kerosakan organ [1,2]. Setiap aspek tindak balas imun semula jadi dan adaptif telah dilaporkan terlibat dalam pesakit SLE dan ia menyumbang kepada ekspresi penyakit dalam subset pesakit yang berbeza. Kehadiran sejumlah besar autoantibodi telah mencirikan penyakit ini manakala pengeluaran yang ditujukan terhadap antigen nuklear, ribonukleoprotein nuklear kecil, DNA beruntai dua (dsDNA), dan nukleosom mewakili ciri penyakit [1,3]. Autoantibodi daripada kompleks imun larut (IC) dengan autoantigen (seperti nukleosom) yang dikeluarkan dengan banyak dalam peredaran pesakit SLE, boleh memendap pada membran basal pada pelbagai organ termasukbuah pinggang, dan memulakan keradangan. Autoantibodi boleh mengikat terus kepadabuah pinggangantigen dan membentuk IC in situ seperti yang ditunjukkan oleh antibodi anti-dsDNA kationik yang mengikat membran bawah tanah glomerular [4-6]. Secara selari, pengeluaran sitokin yang berlebihan termasuk interferon jenis I (IFN), interleukin (IL)-17 dan IL-23 memajukan lagi keabnormalan sel imun atau bertindak secara langsungbuah pinggangsel pemastautin menyebabkan kerosakan [7]. Akhir sekali, tetapi tidak kurang pentingnya, sel T autoreaktif menyusup ke dalambuah pinggangdi mana ia boleh membentuk struktur limfoid tertier (TLS) dan menyebabkan kerosakan organ.
Autoantibodi atau pemendapan IC dalambuah pinggang, bersama-sama dengan tindakan sitokin dan penyusupan sel imun menyumbang kepada perkembangan keradangan buah pinggang pada pesakit dengan SLE yang menjelma sebagai lupus nefritis (LN) dengan morbiditi dan kematian yang ketara [8,9]. Selepas kemas kini mengenai interaksi sel buah pinggang pemastautin dan imun, kami akan membincangkan secara terperinci pembentukan TLS dalambuah pingganginterstitium dan kesannya terhadap fungsi buah pinggang.
Sel pemastautin buah pinggang
2.1. Podosit
Podosit ialah sel khusus pada bahagian viseral kapsul Bowman yang mengelilingi kapilari glomerular. Ia adalah sebahagian daripada jentera penapisan glomerular dan penting untuk dikekalkanbuah pinggangfungsi [10]. Mereka mengekspresikan protein unik termasuk synaptopodin, nephrin [11], podocin [12], dan protein tumor Wilms [13], yang semuanya penting dalam penyelenggaraan struktur dan fungsi mereka [14]. Kecacatan genetik atau diperolehi dalam ekspresi molekul podosit utama selalu membawa kepada detasmen mereka dan perkembanganbuah pinggangkegagalan [15]. Kecederaan podocyte ketara pada orang dengan LN dan menyumbang kepada perkembangan proteinuria dan kerosakan glomerular [16,17].
Podosit diketahui menghasilkan dan menyatakan komponen laluan pelengkap yang bersama-sama dengan pemendapan dan pengaktifan pelengkap daripada peredaran menyumbang kepada kecederaan podosit. Perencatan laluan pelengkap telah dilayan dalam ujian klinikal untuk merawat orang dengan LN [18]. Selanjutnya, podosit mengekspresikan semua reseptor seperti Tol (TLR) dan protein reseptor seperti Nod-3 (NLRP3) dan caspase 1 [19]. Homocysteine mengaktifkan inflammasom NLRP3 dalam podosit tikus yang terdedah kepada lupus dan pesakit dengan LN [20] dan penindasannya mengurangkan proteinuria, histologi.buah pingganglesi, dan pembuangan proses kaki podosit [16] menunjukkan bahawa NLRP3 boleh disasarkan secara terapeutik.
Podosit daripada tikus yang terdedah kepada lupus dan orang yang mempunyai LN menyatakan peningkatan tahap molekul histokompatibiliti utama bersama-sama dengan molekul kostimulasi CD80 dan CD86 yang dianggap sebagai penanda kecederaan sel tetapi pada masa yang sama ia boleh mengaktifkan limfosit yang lewat dan menyumbang kepada pengumpulannya dalam yangbuah pinggangparenkim. Sebaliknya, pelanggaran dalam kapsul Bowman, dalam glomerulonefritis bulan sabit manusia boleh membenarkan sel T CD8 ditambah untuk mencapai jumbai glomerular dan podosit dan menyebabkan kemusnahannya [21].
Podosit mengekspresikan reseptor Fc neonatal (FcRn) yang membolehkan pemindahan IgG dari kapilari ke ruang air kencing. IgG daripada pesakit dengan LN memasuki podosit menggunakan FcRn dan menyebabkan peningkatan regulasi protein kinase IV (CaMK4) yang bergantung kepada kalsium/calmodulin yang memfosforilasi 14–3-3 , protein perancah synaptopodin, yang apabila dilepaskan akan terdegradasi. Synaptopodin adalah penting dalam penyelenggaraan struktur podocyte [22]. Secara selari, CaMK4 mengaktifkan NFkB yang menindas ekspresi nefrin, protein penting diafragma berpecah, dengan menggalakkan fungsi SNAIL penindas transkrip [23]. IgG daripada pesakit dengan LN aktif menyebabkan regulasi CaMK4 di bawah galaktosilasi [23]. Pemadaman global Camk4 dalam tikus rawan lupus MRLlpr secara berkesan menindas LN [24]. Lebih penting lagi, penghantaran yang disasarkan podocyte perencat CaMK4 menindas semua elemen LN dan mengelakkan pemendapan IC [22], menunjukkan bahawa penyelenggaraan struktur dan fungsi podosit dengan menekan aktiviti IC CaMK4 tidak didepositkan. Barisan maklumat ini menyatakan kepentingan faktor tempatan dalam perkembangan kerosakan organ dan nilai penghantaran ubat khusus sel/organ untuk mengehadkan kerosakan organ dalam autoimun.

Cistanche bagus untukbuah pinggang
2.2. Sel mesangial
Sel mesangial dan matriks mesangial membuatbuah pinggangkutub vaskular corpuscle dan penting dalam mengeluarkan protein terkumpul dan IC kecil dari membran bawah tanah [19]. Mereka terlibat dalam patogenesis LN kerana percambahan sel mesangial dan matriks mesangial hadir selalu dalam LN.buah pinggang[25]. Sel mesangial mengekspresikan reseptor seperti Tol (TLR) [25,26], dan apabila dirangsang dengan ligan TLR3 (dsRNA) ia menghasilkan jenis I IFN [25] – sitokin yang didakwa penting dalam patogenesis SLE [25]. ,27].
Antibodi kepada dsDNA mengikat sel mesangial dan mengaktifkan laluan keradangan dan fibrotik, terutamanya yang melibatkan laluan isyarat protein kinase diaktifkan mitogen (MAPK) dan protein kinase C (PKC), yang membawa kepada pengeluaran sitokin proinflamasi [27,28]. Sel mesangial merembeskan interleukin (IL)-6, yang dengan sendirinya boleh memacu perkembangan glomerulonephritis [29]. CaMK4 diperlukan untuk pembiakan sel mesangial dan pengeluaran sitokin. Khususnya, sel mesangial daripada tikus MRLlpr yang terdedah kepada lupus yang kekurangan CaMK4 secara genetik, tidak membiak sebagai tindak balas kepada faktor pertumbuhan yang diperoleh daripada platelet dan tidak menghasilkan IL-6 [30].
2.3. Sel epitelium tiub buah pinggang
buah pinggangsel epitelium tiub terlibat dalam patofisiologi LN. Mereka merembeskan sitokin patogenik, termasuk jenis I IFN [31] dan faktor pengaktifan sel B (BAFF) [32], kedua-duanya mempunyai peranan penting dalam pembangunan SLE (Rajah 1). Tambahan pula,buah pinggangsel epitelium tiub daripada pesakit LN mengekspresikan molekul kostimulasi B7-H4, menunjukkan bahawa mereka boleh mengaktifkan sel T. Penambahan antibodi anti-dsDNA kepada sel epitelium tubular renal dalam kultur membawa kepada regulasi berurutan faktor nekrosis tumor (TNF) , IL-1 dan IL-6 [33], yang mencadangkan sel menyumbang kepada proses keradangan dalam tubulointerstitium dalam LN [34].buah pinggangsel epitelium tiub mengekspresikan endonuklease apoptosis [35] yang nampaknya apabila diaktifkan melalui mekanisme yang belum diketahui, boleh menyebabkan kematian sel [36]. Baru-baru ini, telah ditunjukkan bahawa sel epitelium tiub boleh menghasilkan CXCL12 sebagai tindak balas kepada IL-23 untuk menggalakkan pemadaman interstisial dan genetiknya hanya dalam sel-sel ini mengehadkan glomerulonephritis dalam tikus yang terdedah kepada lupus [7].

BAFF, adalah faktor pertumbuhan dan pembezaan sel B yang mantap yang membantu sel B auto-reaktif untuk terus hidup dan melarikan diri dari toleransi periferi [37,38]. Sekatan BAFF dengan antibodi (Benlysta) telah diluluskan untuk merawat SLE [39] dan LN [40]. BAFF juga dinyatakan oleh sel epitelium tiub orang dengan LN proliferatif dan tahap ekspresi berkorelasi dengan indeks aktiviti yang ditentukan histopatologi [32]. BAFF boleh menggalakkan pembezaan lanjut sel B yang terdapat dalam ruang interstisialbuah pinggangdaripada pesakit dengan LN [41]. Selanjutnya, BAFF telah didakwa menggalakkan pembentukan TLS dalambuah pinggangdengan meningkatkan bilangan sel T yang diletakkan di dalam glomeruli dan meningkatkan keradangan pada tikus [42] yang mungkin menjelaskan kesan terapeutik Benlysta pada pesakit dengan LN [40]. Benlysta mensasarkan pematangan dan isyarat sel B dengan menghalang kemandirian sel B, dan mengurangkan pembezaan kepada sel plasma penghasil Ig pada pesakit dengan LN [43].
2.4. Sel stem mesenchymal
Sel stem mesenchymal (MSCs) adalah sel imunomodulator progenitor multipoten yang terdapat dalam semua tisu [44]. Mereka nampaknya mempunyai peranan dalam penindasan dendritik dan sel T [45]. Kajian terdahulu telah menunjukkan bahawa apabila kepekatan sitokin proinflamasi adalah rendah, MSC mungkin mempunyai potensi imunostimulasi [45,46]. MSC boleh dikesan dalam dinding pelvis dan TLS dalambuah pinggangdaripada tikus yang terdedah kepada lupus [47]. Rangsangan MSC dengan sitokin radang membawa kepada ekspresi TNF-, IL-1, CCL19 dan ICAM [47]. Walaupun tidak jelas, MSC nampaknya mempunyai peranan yang serupa dengan sel penganjur tisu limfoid (LTo) dan MSC khusus tisu pemastautin berfungsi seperti sel induser tisu limfoid (LTi). Mereka boleh memprogram semula dan memulakan lata keradangan awal dengan berinteraksi dengan sel T [47]. Pembezaan MSC dan pengumpulan sel imun menyebabkan pengembangan saluran limfa dan oleh itu pembentukan TLS [48].

Cistanche bagus untukbuah pinggang
2.5. Makrofaj
Makrofaj penduduk dibuah pinggangbiasanya dilihat dalam interstitium yang mengelilingi glomeruli [49]. Monosit periferal selepas kemasukan kebuah pinggangtisu dan pembezaan kepada makrofaj bertindak sebagai pemain utama dalam keradangan, kecederaan, dan fibrosis dalam gangguan buah pinggang akut dan kronik [50]. CD16 plus atau CD14 plus makrofaj direkrut untuk cederabuah pinggangdengan kehadiran sitokin dan kemokin [50]. Beberapa subtipe makrofaj (M1, M2a-c) [51] telah direkodkan hadir dalam tisu LN dengan asal dan fungsi yang tidak diketahui [49,50,52]. Secara umum, nampaknya jika makrofaj pemastautin terdedah kepada ligan TLR endosom dan molekul corak molekul (DAMP) yang berkaitan dengan kerosakan [53], mereka beralih daripada fasa resolusi kepada fasa keradangan. Semasa fasa keradangan, makrofaj menukar fenotip mereka kepada M1 dan mengekspresikan Ly6C/Gr1 dan sitokin pro-radang rahsia [54,55]. Sebaliknya, semasa fasa pembaikan atau resolusi, mereka berpolarisasi ke dalam fenotip M2 [56,57]. Oleh itu, nampaknya makrofaj mempunyai fungsi ganda dan memaparkan keplastikan yang tinggi semasa penyakit buah pinggang.
3. Struktur limfoid tertier
Istilah 'limfoid tertier' telah diperkenalkan oleh Picker dan Butcher [58] untuk menerangkan tapak limfoid tambahan dalam tisu bukan limfoid. TLS telah dirujuk dalam pelbagai cara, termasuk organ limfoid tertier, tisu limfoid tertier dan struktur limfoid ektopik. Pengumpulan limfosit dalam tisu bukan limfoid periferal, dan tahap di mana ia menjadi teratur, berbeza-beza mengikut jenis dan tempoh rangsangan keradangan antigenik [59]. Akibatnya, agregat limfoid terdiri daripada koleksi longgar, yang terdiri daripada beberapa sel T atau B, kepada tisu teratur yang memaparkan ciri-ciri TLS [60-63].
TLS terdiri daripada zon yang kaya dengan sel T dengan DC matang di sebelah folikel sel B dengan ciri-ciri pusat germinal yang dikelilingi oleh sel plasma. Atribut minimum yang diperlukan untuk membentuk TLS berfungsi tidak diketahui, tetapi TLS ditakrifkan sebagai agregat limfoid dengan komponen stroma tersusun yang terdiri daripada sel dendritik folikular (FDC) dan sel retikular fibroblastik (FRC), dan secara ciri, dengan venula endothelial tinggi (HEV) dan saluran limfa (LV) [64,65]. Definisi berdasarkan kriteria ini akan mengecualikan agregat sel B atau T sebagai tindak balas kepada keradangan yang tidak mempunyai petak stroma yang dibezakan (Kotak 1).
TLS berkembang dalam pelbagaibuah pinggangpatologi, termasuk nefropati IgA [66], peringkat awal IgG4-nefritis tubulointerstitial [67], akutbuah pinggangkecederaan [68,69], kanser [70], pyelonephritis [71], pemindahan dan LN [41,72,73]. Dalam tikus yang terdedah kepada lupus, TLS ditemui berhampiran dengan dinding pelvis, bersebelahan dengan arteri dan vena yang besar [74]. Dalam penyakit autoimun seperti rheumatoid arthritis, sindrom Sjogren, multiple sclerosis, diabetes, tiroiditis Hashimoto, kolangitis sclerosing primer dan sirosis hempedu primer, dan myasthenia gravis, TLS boleh membolehkan generasi in situ sel T dan B autoreaktif dan penghasilan autoantibodi yang mengekalkan proses patogenik [63,70,75,76].
3.1. Perbincangan silang sel imun buah pinggang dengan struktur limfoid tertier
Sel T mengekalkan homeostasis imun di bawah keadaan fisiologi dan menggalakkan toleransi terhadap antigen diri. Dalam autoimunbuah pingganggangguan gangguan toleransi sel T kepada autoantigen boleh menyebabkan penjanaan autoantibodi, keradangan, penyusupan sel imun, dan perkembangan pelbagai jenis nefritis [77,78].
Sel T boleh menyusup ke dalambuah pinggangtisu sama ada kerana ia telah diaktifkan di pinggir dan mengekspresikan molekul lekatan atau ia mungkin naif dan menjadi diaktifkan selepas ia memasukibuah pinggangparenkim oleh podosit atau sel epitelium tiub seperti yang dibincangkan di atas. Sel yang diaktifkan mengekspresikan molekul lekatan seperti CD44 yang, apabila dikaitkan dengan ESRIN/reka bentuk semula/moesin terfosforilasi [79], mengikat asid hyaluronik ligannya, yang sintesisnya meningkat dalam buah pinggang tikus rawan lupus [80]. Oleh kerana esrin/reka bentuk semula/moesin difosforilasi oleh Rho-kinase, perencatan aktivitinya mengehadkan kemasukan sel T ke dalambuah pinggang[81]. Begitu juga, perencatan sintesis asid hyaluronik mengurangkan kemasukan sel T ke dalam buah pinggang tikus yang terdedah kepada lupus [80] Menariknya, bilangan sel CD3 tambah CD44 tambah dalam darah periferi orang dengan SLE berkorelasi dengan aktiviti penyakit buah pinggang [82] .
Majoriti sel dalam TLS ialah sel T CD3 tambah [74] dan ia termasuk sel T CD8 tambah sitotoksik yang mengekspresikan granul dan sel T CD4 tambah yang memaparkan fenotip sel TH1 dan sel Treg CD4 tambah [83–86 ]. Diandaikan bahawa sel dendritik matang (DC) membentangkan antigen kepada CD4 ditambah sel T dalam zon sel T TLS [87], tetapi DC-LAMP ditambah DC juga telah dikesan di pusat germinal, menunjukkan bahawa mereka mempunyai peranan dalam pembentangan antigen kepada sel B [88]. Sel B tersusun menjadi pusat germinal dengan sel plasma. Kawasan sel B mengandungi CD21 tambah FDC manakala kawasan sel T mengandungi MIDC-8 tambah DC [74].
Sel T berganda-negatif (DN) ditakrifkan oleh kehadiran reseptor sel T (TCR) tambah dan ketiadaan molekul CD4 dan CD8. Mereka berkembang dalam darah periferi pesakit SLE, memberikan bantuan kepada sel B untuk menghasilkan autoantibodi [89], dan menghasilkan IL-17 [90]. Nampaknya ia berasal daripada sel T CD8 tambah [91,92] sebagai tindak balas kepada rangsangan dengan autoantigen dan kehadiran IL-23 [93]. Secara mekanikal, lokus CD8 dimatikan melalui pengubahsuaian epigenetik yang dikenakan oleh modulator elemen tindak balas cAMP penindas (CREM) [94]. Lebih menarik, sel T DN hadir dalambuah pinggangpesakit dengan LN dan mereka menghasilkan IL-17 [90] menunjuk kepada sumbangan langsung mereka kepadabuah pinggangkeradangan.
Subset TH17 sel T ditakrifkan oleh ungkapan keturunan yang menentukan faktor transkripsi ROR t. Mereka menggalakkan tindak balas autoimun pada manusia dan tikus dengan menghasilkan faktor perangsang koloni granulosit-makrofaj (GM-CSF), IFN, dan IL-17, - 21 dan - 22 [95,96]. Sel TH17 mengekspresikan C-C motif chemokine receptor type 6 (CCR6) dan direkrut kebuah pinggangoleh C–C motif chemokine 20 (CCL20), yang dihasilkan oleh sel mesangial selepas rangsangan oleh IL-17 (juga dihasilkan oleh neutrofil atau sel δT) [97] dan oleh TEC yang terdedah kepada IL-23 [ 7]. Sel TH17 yang terdapat dalambuah pinggangrahsia IL-17 dan menggalakkan keradangan dengan menghasilkan TLS [98], menggalakkan pengaktifan sel B dan kehilangan toleransi [99,100].
Sel T-helper folikular (TFH) ialah sel CD4 ditambah T yang menyatakan faktor transkripsi BCL6 dan reseptor chemokine motif CXC jenis 5 (CXCR5). Sel-sel ini berhijrah ke pusat germinal sebagai tindak balas kepada CXC motif chemokine 13 (CXCL13). Mereka juga mengekspresikan tiga reseptor permukaan, termasuk kostimulasi sel T yang boleh diinduksi, CD40L, PD-1 dan menghasilkan IL-21 untuk memajukan pengaktifan sel B dan pembezaan sel B ke dalam sel B memori dan plasmablas [ 101–103].
Tahap sel TFH yang beredar meningkat pada orang yang mempunyai penyakit autoimun termasuk SLE dan kajian pada tikus yang terdedah kepada lupus telah mengesahkan peranan patogen mereka [102]. Dalam pesakit SLE, kekerapan subset sel ini - sel TH ekstrafolikular - berkorelasi dengan tahap antibodi anti-dsDNA dan kuantiti sel B plasmablast. Sel TH folikel tambahan mentakrifkan subset CCR6 tambah, yang menyatakan CXCR5 tetapi bukan BCL6 dan boleh merembeskan IL-17 dan memudahkan pengeluaran imunoglobulin oleh sel B [103,104].
Sel Treg ialah sel TCR ditambah Foxp3 ditambah CD4 ditambah T yang berkembang di dalam timus atau pinggir. Mereka memaparkan aktiviti menindas dan mengawal kebanyakan tindak balas imun melalui pelbagai mekanisme [105]. Salah satu peranan mereka yang paling terkenal dalambuah pinggangialah rembesan sitokin anti-radang IL-10 [106]. Beberapa peristiwa molekul yang membawa kepada disfungsi sel Treg telah dijelaskan. Molekul yang terlibat termasuk protein phosphatase 2A (PP2A), sasaran mamalia kompleks rapamycin 1 (mTORC1), phosphatidylinositol 3,4,5-trisphosphate 3- phosphatase, dwi-spesifik protein phosphatase (PTEN) dan kalsium /calmodulin-dependent protein kinase IV (CaMK4). Penyasaran ini boleh menyelamatkan atau menyekat fungsi sel Treg dan memodulasibuah pinggangkeradangan [107].
Analisis klonotip sel T dari pelbagai tisu tikus LN, serta dari darah periferi ataubuah pinggangpesakit dengan SLE, telah mendedahkan pengembangan subset terhad repertoir TCR, menunjukkan tindak balas kepada bilangan autoantigen yang ditetapkan [93]. Repertoir ini kekal stabil selama beberapa bulan atau tahun [108,109]. Dalam pesakit SLE, klon dalam darah periferi adalah berbeza daripada yang di dalam buah pinggang [110], menunjukkan bahawa sel T naif diaktifkan secara bebas di pinggir danbuah pinggang.
Pengeluaran antibodi tempatan adalah kritikal dalam pembentukan TLS. Menariknya,buah pinggangProfil gen TLS berkaitan sistem imun dalam tikus rawan lupus adalah serupa dengan nodus limfa semasa peringkat aktif LN [74]. TLS menyediakan faktor survival sel T dan B IL-7 dan BAFF yang merekrut limfosit dan menyokong interaksi antara sel T dan B dalam persekitaran terkurung [111]. Pengaktifan sel B tempatan telah ditunjukkan dalam TLS dengan ekspresi Activation Induced Cytidine Deaminase (AICDA), enzim yang bertanggungjawab untuk penggabungan semula suis kelas dan hipermutasi somatik [112] dan percambahan aktif. Pembezaan tempatan sel plasma autoreaktif juga telah diperhatikan [113].
Dalam model SLE murine yang disebabkan oleh pristan, sel B membiak dan menukar kelas dalam TLS, dan sel plasma dan plasmablast penghasil antibodi Sm/RNA menghasilkan autoantibodi tempatan [114,115]. Lebih-lebih lagi,buah pinggangdaripada pesakit LN mengandungi struktur seperti pusat germinal yang mengandungi FDC. Pusat-pusat ini mungkin mempunyai peranan dalam tindak balas imun khusus tisu tempatan yang aktif [41]. Mengenal pasti peristiwa yang memulakan pembentukan TLS harus memajukan pemahaman kitabuah pinggangkerosakan pada pesakit dengan LN. BAFF dan tahap autoantibodi serum berkorelasi dengan pembentukan TLS dalambuah pinggang[42]. Mengurangkan tahap BAFF mengurangkan bilangan sel T dalam glomeruli dan menghalang LN dan pembentukan atau penyelenggaraan TLS [42].
Tambahan pula, kehadiran FDC, atau pengikatan IgG-ICs kepada Fc RIIB, boleh memberikan sumber antigen utuh [41,116,117] untuk pengembangan dan pengaktifan sel B, dan penghasilan limfotoksin 1 2, yang mungkin seterusnya menggalakkan pembangunan TLS [118,119]. Sebagai alternatif, CD11b ditambah sel myeloid merembeskan tahap BAFF yang tinggi dan meningkatkan keupayaan kemotaktik sel B dengan memodulasi isyarat yang disebabkan oleh chemokine [120], dengan itu membawa kepada pengagregatan sel dan pembahagian TLS. Oleh kerana peningkatan tahap BAFF menguatkan pengaktifan sel T tempatan [121], mereka boleh menggalakkan aktiviti TFH dan memanjangkan tindak balas pusat germinal in situbuah pinggangTLS. Selanjutnya, pada pesakit dengan LN, hanya interaksi sel-ke-sel antara sel TFH dan sel B mendorong tahap Bcl-6 dan IL-21 yang tinggi dalam interstitium [122]. Ini mungkin mewakili kesan BAFF yang menggalakkan ekspresi ICOSL pada sel B yang diaktifkan [123] dan mendorong pembentukan sel TFH [124,125]. Oleh itu,buah pinggangTLS mungkin terbentuk dalam LN disebabkan oleh penyusupan sel hematopoietik ke dalambuah pinggang, tetapi tahap BAFF yang tinggi diperlukan untuk membentuk atau mengekalkan TLS berpetak dengan betul. Ini menunjukkan bahawa tahap tinggi atau pengeluaran BAFF yang berpanjangan mungkin merupakan peristiwa penting dalam pembentukan TLS berpetak.

Cistanche bagus untukbuah pinggang
3.2. Petunjuk molekul untuk pembentukan struktur limfoid tertier
CXCL13 yang dihasilkan oleh sel stromal fibroblastik adalah kemokin penting untuk sel B dan induser tisu limfoid (LTi). Tikus yang tidak mempunyai CXCL13 tidak membentuk nodus limfa kecuali untuk bahagian muka, serviks, dan mesenterik [126]. Induksi pembentukan TLS [127] pada tikus boleh dicapai dengan mengekspresikan CXCL13 yang didorong oleh promoter insulin tikus (RIP), yang aktif dalam pankreas danbuah pinggang. Ini membawa kepada pembentukan TLS yang dicirikan oleh zon sel B dan T yang diasingkan, kehadiran DC konvensional, dan rangkaian sel stromal yang padat dan saluran darah jenis high endothelial venule (HEV) [128]. CXCL12 (atau faktor terbitan sel stromal 1 (SDF1)) dinyatakan oleh sel stroma sumsum tulang dan penting dalam hematopoiesis sumsum tulang dan pembangunan sel B [129]. CXCL12 dinyatakan oleh HEV dalam organ limfoid sekunder (SLO) dan bertindak sebagai kemokin pengambilan sel B yang penting, manakala sel T kebanyakannya tidak bertindak balas [130] (Jadual 1).
Sel epitelium tiub daripada tikus rawan lupus boleh mengekspresikan reseptor IL-23 dan menghasilkan kemokin CCL20 yang boleh menarik limfosit kebuah pingganginterstitium (Rajah 1) [7]. Selanjutnya, IL-23 bertindak pada sel epitelium tiub boleh menyekat pengeluaran arginase 1 yang mengkatabolismekan arginin dan oleh itu membawa kepada peningkatan kepekatan arginin yang diperlukan untuk pertumbuhan tempatan limfosit [7]. Melalui mekanisme pertama, sel epitelium tiub mampu menghasilkan kemokin proinflamasi untuk menarik limfosit yang boleh diaktifkan secara tempatan. Melalui mekanisme kedua, sel epitelium tiub boleh memaparkan kapasiti imunosupresif yang boleh dielakkan dengan kehadiran IL-23 dan mungkin perangsang lain.
CCL19 dan CCL21 dinyatakan oleh HEV dan beberapa sel stromal. Mereka adalah ligan untuk CCR7 yang terdapat pada sel T, DC, dan sel LTi. Tikus Plt yang tidak mempunyai gen CCL19 dan CCL21 yang dinyatakan oleh tisu limfoid dalam saluran limfa menunjukkan peranan penting untuk CCR7 dan CCL19 / CCL21 dalam homing sel T. Dalam model RIP-overexpression, CCL21 terbukti lebih berkesan daripada CCL19 dalam mendorong pembentukan TLS [131,132]. Walau bagaimanapun, walaupun dengan overexpression CCL21, tidak ada pembentukan folikel sel B yang jelas [131]. CCL28 mempunyai peranan dalam pengambilan dan penempatan sel B dan T dan menggalakkan tindak balas imun adaptif [133-135]. Isyarat daripada interaksi antara CCL28 dan CCR3/CCR10 memacu proses ini dan menarik pelbagai sel imun dari kejiranan tempatan [135,136]. Baru-baru ini, pengambilan sel Treg oleh CCL28 telah diperhatikan, menunjukkan bahawa ia mempunyai peranan dalam modulasi sistem imun, mengekalkan toleransi terhadap antigen diri, dan mencegah perkembangan penyakit autoimun [137,138] (Jadual 1).
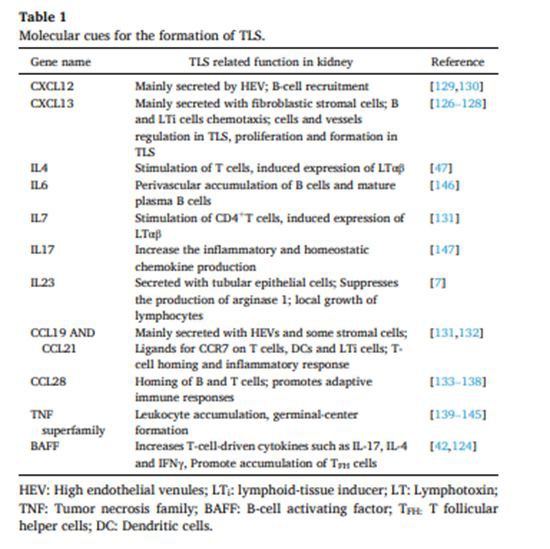
Ahli superfamili TNF (TNFSF), iaitu TNF , limfotoksin (LT) , dan , dan reseptor isyarat mereka TNFRI/II dan LT R, telah dicadangkan untuk menggalakkan pembentukan TLS. Juga, ekspresi ektopik TNF atau LT, tetapi bukan LT, di bawah kawalan RIP membawa kepada pembentukan TLS [139,140]. Kesan yang paling ketara dilihat apabila LT dan LT diekspresikan bersama, mengakibatkan pengumpulan leukosit invasif di pulau pankreas, dan TLS yang jauh lebih besar daripada yang terbentuk dalam tikus transgenik LT [139]. TNFR-I ialah pengawal selia asas organogenesis tisu limfoid dan pembentukan pusat germinal, bukannya TNFR-II [141], dan ia mengantara TLS pankreas yang disebabkan oleh LT [142]. Pengaktifan TNFR-I dan LT R juga telah terlibat dalam TLS aorta, di mana penyimpangan isyarat LT R membawa kepada penindasan ekspresi CCL21 dan CXCL13, dengan akibat pengurangan pembentukan HEV dan perkembangan TLS yang terganggu [143, 144] (Rajah 1). 2).

Walaupun kesan LT , bersendirian atau dengan LT , kelihatan jelas, peranan TNF dipertikaikan. Dalam beberapa penyakit radang, termasuk yang melibatkan TLS, TNF mempunyai aktiviti anti-radang [144]; insulitis dalam tikus NOD dan lupus di New Zealand tikus bertambah baik selepas suntikan TNF [144,145].
Ekspresi berlebihan transgenik IL-6 dan IL-6R membawa kepada pengumpulan perivaskular sel B dan sel B plasma matang [146]. IL-1 yang dihasilkan oleh MSC diekspresikan secara berlebihan dalam tikus yang terdedah kepada lupus dan boleh menyumbang kepada pembentukan TLS [47]. Rangsangan sel T dengan ekspresi teraruh IL-4 atau IL-7 LT ; IL-7 paling mujarab untuk sel T CD4 tambah [131]. Keluarga gen IL{11}} adalah penting dalam pertahanan terhadap patogen dan telah terlibat dalam pelbagai senario keradangan kronik. Seperti ahli TNFRSF, isyarat reseptor IL-17 melalui NF-κB dan IL-17 sel T diinduksi oleh IL-6, TGF dan IL-23, tetapi dihalang oleh IL{17}}. Oleh itu, IL-17 ialah pengantara penting untuk lipopolisakarida yang disebabkan kira-kira [147]. IL-7R dinyatakan oleh sel LTi dan bersama-sama dengan CXCR5) IL-7 menggalakkan pembentukannya dalam SLO [126].
BAFF boleh menggalakkan kecederaan tisu dengan menjejaskan kualiti dan kuantiti sitokin dipacu sel T seperti IL-17, IL-4 dan IFN . Peningkatan tahap BAFF dalambuah pinggangboleh menyebabkan kerosakan glomerular dengan menyerang sel T di dalam glomeruli, atau dengan mendorong pembentukan sel TH17. Tidak jelas sama ada kedudukan sel T adalah proses selari atau bergantung bersama yang menggalakkan glomerulonephritis dan nefritis tubulointerstitial. Telah ditunjukkan bahawa menyekat rangsangan bersama sel T [148] atau meneutralkan IFN dan IL-4 [149,150], membawa kepada peningkatan atau kelewatan dalambuah pinggangpatologi. Sebanding, penyusupan dan pengagregatan sel T telah ditemui dalambuah pinggangbiopsi daripada pesakit SLE [151]. Penyusupan sel imun ke kawasan tubulointerstitial di SLE dikaitkan dengan LN [41], menunjukkan bahawa kedudukan sel T dalam buah pinggang adalah penting dalam penyakit ini.
3.3. Pembuluh dalam struktur limfoid tertier
TLS adalah serupa dengan nodus limfa dari segi struktur, vaskular, komposisi selular, dan profil kemokin. Sel imun termasuk zon sel T dan B dan sel pembentang antigen, termasuk FDC dan DC matang. Pembuluh dalam TLS terutamanya terbahagi kepada saluran limfa dan darah (Rajah 3).

buah pinggangsaluran limfa (LV) dianggap sebahagian daripada interstitium kerana ia tidak mempunyai membran bawah tanah, dan ia buta dan kekurangan pericytes [152]. Kapilari limfa mengekspresikan PROX-1, LYVE-1, CCL21, podoplanin, VEGFR-2 dan VEGFR-3 [153]. Pembuluh limfa TLS mengekspresikan penanda limfa seperti LYVE-1, PROX-1, podoplanin (dalam kedua-dua tikus dan manusia), dan D2–40 (pada manusia) [154], seperti yang dilaporkan oleh pelbagai kajian daripada kronikbuah pinggangpenolakan [155,156], allograf jantung [157], model tetikus transgenik [158] dan model tetikus penyakit primer seperti Sjogren yang berkaitan dengan usia [159]. Namun begitu, masih banyak yang perlu dijelaskan.
Tidak diketahui sama ada saluran TLS menjalankan fungsi yang sama seperti dalam nodus limfa. Nampaknya mereka menyumbang kepada saliran cecair, tetapi ini belum diterokai sepenuhnya. Ia juga tidak diketahui sama ada LV membawa antigen dan sel dalam TLS dan sel menjauhi TLS, seperti saluran aferen dan eferen dalam nodus limfa. Bahawa TLS LVs kerap mengandungi sel [159,160], menunjukkan bahawa mereka mempunyai peranan sebagai pengangkut melalui ungkapan CCL21, yang berinteraksi dengan sel pengekspresi CCR7-. Walau bagaimanapun, LV dalam sesetengah TLS mengumpul sel, menunjukkan bahawa ia tidak memudahkan saliran selular dan telah merosakkan fungsi eferen.
Sel pemastautin nodus limfa mengekspresikan sphingosine-1 fosfat (S1P) dan interaksinya dengan reseptor S1P1 pada limfosit adalah penting untuk pelepasannya daripada nodus limfa. FTY720 (fingolimod) ialah agonis S1P1 yang menyebabkan internalisasi dan pengumpulan limfosit dalam nodus limfa [161], dengan itu berfungsi sebagai imunosupresan. Apabila tikus NOD dengan TLS pankreas dirawat dengan FTY720, mereka tidak akan terus mengalami kemusnahan pulau kecil dan diabetes [162]. FTY720 menghalang perkembangan penyakit hanya pada masa tikus mempamerkan TLS [163]. TLS pankreas mereka dikaitkan dengan skor insulitis yang tinggi selepas rawatan FTY720, menunjukkan bahawa sel terperangkap di dalamnya. Kemusnahan pulau kecil dan diabetes berlaku dalam beberapa hari selepas menghentikan rawatan FTY720 [162,164]. Oleh itu, nampaknya kecerunan S1P menjejaskan pemerdagangan limfosit dalam TLS LV. Fingolimod boleh memaksa TLS untuk larut pada pesakit dan tikus dengan lupus.
LV mengangkut antigen larut atau berkaitan sel ke dalam nodus limfa. Protein berkaitan vesikel plasma (PLVAP) diekspresikan oleh sel endothelial limfa saluran darah dalam sinus limfa dalam nodus limfa. Sel endothelial limfatik positif PLVAP menyumbang kepada penyaringan limfosit dan antigen berat molekul tinggi yang memasuki nodus limfa [165]. Memandangkan TLS mengandungi sistem saluran [166], adalah munasabah untuk mempersoalkan sama ada LV dalam TLS dan nodus limfa berfungsi sama. Pengangkutan antigen mungkin kurang kritikal berbanding SLO kerana antigen ialah komponen sebenar TLS. Walau bagaimanapun, memandangkan sel pembentang antigen biasanya terdapat dalam TLS, ini boleh dipertikaikan.
Seperti yang dinyatakan di atas, LV dalam nodus limfa mempersembahkan antigen diri [167–169] sama ada secara langsung melalui ekspresi molekul kompleks histokompatibiliti utama (MHC) atau antigen pada sel pembentangan antigen 'klasik'. Pembentangan antigen diri oleh LV [167] boleh memudahkan induksi sama ada toleransi atau pengaktifan sel T dalam nodus limfa atau TLS. Kajian yang menyiasat keupayaan TLS LV untuk membentangkan antigen dan mendorong salah satu daripada hasil ini belum dijalankan.
HEV ialah saluran darah positif alamatin nod persisian (PNAd) dengan struktur yang berbeza. HEV nampaknya mempunyai peranan dalam pengangkutan limfosit bawaan darah ke dalam TLS. Fenomena ini adalah sejenis penyusupan khusus yang terutamanya sel T memori dengan ekspresi L-selectin yang rendah (mungkin disebabkan oleh ekspresi PNAd) boleh memasukibuah pinggang[139]. Kajian eksperimen terhadap tikus yang kekurangan LT atau LT LN mendapati bahawa pembangunan HEV yang mengekspresikan PNAd terbantut, yang membawa kepada pengurangan saiz dan selular penyusupan limfoid [139]. Oleh itu, isyarat LT R mungkin diperlukan untuk pengagregatan limfoid yang teratur dan pembentukan HEV.
4. Kesimpulan dan soalan terbuka
Walaupun tindak balas imun yang dijana dalam SLO boleh menjana perlindungan terhadap patogen, tindak balas auto-imun dalam TLS mungkin merosakkan. Pusat germinal dalam TLS mempunyai ciri yang serupa dengan pusat germinal dalam SLO dan menyediakan asas untuk pengembangan klon sel imun dan hipermutasi somatik [41]. Walaupun kehadiran kompleks imun telah dianggap penting dalam pembentukan TLS, bukti yang lebih terkini menunjukkan bahawa di bawah pengaruh sel epitelium tiub sitokin boleh menghasilkan sitokin yang mampu menarik sel T [7].
Sel B yang terdapat dalam TLS telah terbukti telah mengalami hipermutasi somatik [41] dan oleh itu pengeluaran autoantibodi tempatan dan kemungkinan pembentukan IC in situ adalah pasti. Sel Th17 terdapat dalambuah pinggangorang dan tikus dengan lupus yang menunjukkan sumbangan langsung sel-sel ini dalam tindak balas keradangan danbuah pinggangkerosakan [101,170–172]. Hakikat bahawa repertoir TCR daripadabuah pinggangsel menyusup dalam tikus dan orang yang menghidap lupus dihadkan [93] menunjukkan bahawa antigen khusus buah pinggang, masih bebas, sedang diiktiraf. Sel Th17 adalah penting dalam pembentukan TLS dalam penyebaran keradangan dalam sistem saraf pusat dan paru-paru neonatal [173-175]. Peranan yang sama boleh diunjurkan untuk sel dalam penubuhan dan penyelenggaraan keradangan di LN.
Kehadiran sel Treg dalambuah pinggangTLS dan kemungkinan fungsinya tidak diketahui. Ada kemungkinan bahawa mereka dikecualikan melalui mekanisme yang tidak diketahui atau jika ada ia menjadi kehilangan fungsi yang diharapkan. Adalah diketahui bahawa sel Treg dengan kehadiran persekitaran keradangan kehilangan fungsi pengawalseliaan mereka [78].
Walaupun telah didakwa bahawa keamatan keradangan interstisial mewakili tanda yang tidak menyenangkanbuah pinggangfungsi masih tidak diketahui bagaimana TLS menyumbang kepadabuah pinggangkerosakan. Sel T boleh memusnahkanbuah pinggangsel pemastautin seperti itu telah ditunjukkan untuk podosit [21], melalui sitotoksisiti langsung atau dengan menjejaskan fungsi sel buah pinggang melalui tindakan sitokin seperti yang ditunjukkan untuk IL-23 [7] dan BAFF [123].
Yang belum diterokai sepenuhnya adalah bidang sumbangan TLS kepada pembangunanbuah pinggangfibrosis yang tidak dapat dipulihkan dan mentakrifkan penghujung fungsi. Sitokin yang dihasilkan oleh sel yang menyusup bersama-sama dengan sumbangan faktor lain yang dihasilkan oleh sel pemastautin buah pinggang boleh menggalakkan pengeluaran kolagen oleh fibroblas.
Teknologi akan datang termasuk penjujukan RNA sel tunggal [176] dan transkriptomi spatial akan membolehkan pencirian interaksi antara sel yang terdiri daripada TLS danbuah pinggangsel pemastautin. Mereka juga mungkin membenarkan pencirian subset dalam kalangan pesakit dengan LN, kerana sudah pasti LN adalah heterogen secara klinikal dan patogenetik. Usaha untuk membalikkan patologi buah pinggang dengan menghantar ubat kepadabuah pinggangsel pemastautin (podocytes [22], sel epitelium tiub [7]) sepatutnya membenarkan pemulihan fungsi sel buah pinggang yang lebih berkesan manakala kesan sampingan yang terhasil daripada pentadbiran sistemik dapat dielakkan.
Ucapan terima kasih
Disokong oleh geran penyelidikan Pihak Berkuasa Kesihatan Wilayah Norway Utara HNF 1427-18.
Daripada: 'Saling interaksi imun danbuah pinggangsel pemastautin dalam pembentukan struktur limfoid tertier dalam lupus nefritis' olehSimin Jamaly et al
---1568-9972/© 2021 The Authors. Diterbitkan oleh Elsevier BV Ini ialah artikel akses terbuka di bawah lesen CC BY.