Kekebalan Semula Jadi Epitelium Gastrointestinal—serantau Dan Organoid Sebagai Model Baharu
Jun 20, 2023
Saluran gastrousus manusia sentiasa bersentuhan dengan rangsangan mikrob. Halangannya perlu memastikan kewujudan bersama bakteria komensal sambil membolehkan pengawasan patogen yang menceroboh. Di tengah-tengah interaksi terletak lapisan epitelium, yang menandakan sempadan badan. Ia dilengkapi dengan pelbagai penderia imun semula jadi yang berbeza, seperti reseptor seperti Tol, untuk melancarkan tindak balas keradangan kepada mikrob. Disfungsi sistem yang rumit ini mengakibatkan patologi yang berkaitan dengan keradangan, seperti penyakit radang usus. Walau bagaimanapun, kerumitan interaksi selular, asas molekulnya, dan perkembangannya masih kurang difahami. Dalam tahun-tahun kebelakangan ini, organoid yang berasal dari sel stem telah mendapat perhatian yang semakin meningkat sebagai model yang menjanjikan untuk kedua-dua pembangunan dan pelbagai jenis patologi, termasuk penyakit berjangkit. Di samping itu, organoid membolehkan kajian imuniti semula jadi epitelium secara in vitro. Dalam ulasan ini, kami menumpukan pada penghalang epitelium gastrousus dan organisasi serantaunya untuk membincangkan penderiaan dan pembangunan imun semula jadi.
Pendedahan kepada rangsangan mikrob boleh meningkatkan imuniti, kerana rangsangan mikrob boleh merangsang badan untuk menghasilkan sel imun dan molekul imun, seterusnya merangsang tindak balas imun badan. Khususnya, pendedahan kepada rangsangan mikrob boleh mengaktifkan sel imun seperti makrofaj, sel dendritik, dan sel pembunuh semula jadi, mempercepatkan pembiakan dan pembezaan sel imun, dan meningkatkan daya hidup dan rintangan penyakit sel imun. Di samping itu, rangsangan mikrob juga boleh menggalakkan tindak balas keradangan dan peraturan imun, dan meningkatkan pertahanan imun badan terhadap patogen. Oleh itu, pendedahan yang munasabah kepada rangsangan mikrob boleh menggalakkan peningkatan imuniti manusia. Ia boleh dilihat bahawa kita perlu meningkatkan imuniti. Cistanche boleh meningkatkan imuniti dengan ketara. Abu daging mengandungi pelbagai bahan aktif secara biologi, seperti polisakarida, dua cendawan, Huang Li, dll. Bahan-bahan ini boleh merangsang pelbagai jenis daging dalam sistem imun. sel, meningkatkan daya tahan imun mereka.

Klik manfaat kesihatan cistanche
Kata kunci
Saluran gastrousus. Kekebalan. Regionalisasi dan organoid.
pengenalan
Saluran gastrousus (GI) diperlukan untuk pencernaan makanan dan menjangkau dari rongga mulut melalui esofagus, perut, usus kecil, dan usus besar ke dubur. Lumen GI dijajah oleh pelbagai jenis komensal, simbion, dan kadang-kadang patogen. Penjajahan mikrob mengikut kecerunan dengan kurang daripada 103 mikrob/ml dalam perut kepada 103 –107 mikrob/ml dalam usus kecil dan 1011– 1012 mikrob/ml dalam kolon (disemak dalam [1–3]). Dari perut kelenjar dan seterusnya, saluran GI dilapisi oleh satu lapisan sel epitelium kolumnar. Lapisan epitelium ini terdiri daripada sel-sel khusus yang berbeza, saling terkunci rapat oleh kompleks protein simpang, menguatkuasakan halangan fizikal (Rajah 1).
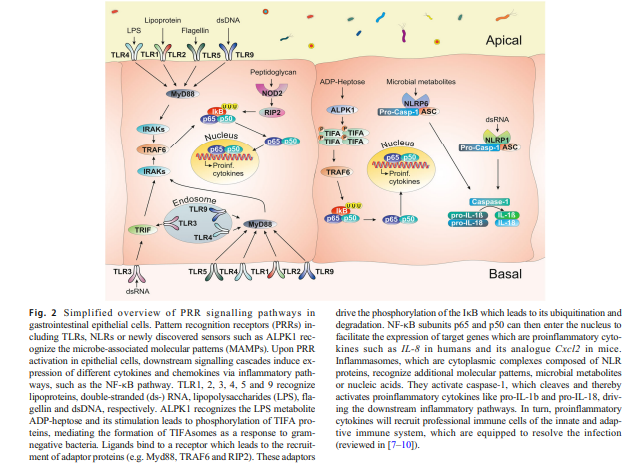
Interaksi antara mikrobiota usus serta patogen yang tertelan dan sel epitelium dimediasi oleh reseptor pengecaman corak (PRR), termasuk reseptor seperti Tol (TLR), domain oligomerisasi pengikat nukleotida (NOD) – seperti reseptor (NLR), dan lain-lain. reseptor sitosol (Rajah 2, disemak dalam [7, 11]). PRR ini memainkan peranan penting dalam mengenali corak molekul berkaitan mikrob (MAMP) dan corak molekul berkaitan kerosakan (DAMP). Selepas pengaktifan PRR dalam sel epitelium, lata isyarat hiliran mendorong ekspresi sitokin dan kemokin yang berbeza melalui laluan keradangan, seperti laluan NF-κB, untuk mengarahkan sel imun profesional (disemak dalam [8, 12-16]). Sebagai tambahan kepada PRR klasik, sensor selanjutnya aktiviti bakteria, seperti alpha-kinase 1 (ALPK1) baru-baru ini telah ditemui [17-19]. Inflammasom, kompleks sitoplasma yang terdiri daripada protein NLR, mengenali corak molekul tambahan, seperti metabolit bakteria (disemak dalam [7, 9]).
Tindak balas imun semula jadi gastrousus, termasuk penderiaan PRR, mesti mengimbangi keperluan perlindungan daripada patogen yang berpotensi berbahaya dengan dapat bertolak ansur dengan pendedahan kepada mikrobiom luminal yang pelbagai. Oleh itu, ekspresi dan fungsi isyarat PRR dijangka memberi kesan besar bukan sahaja pada penderiaan patogen tetapi juga pada homeostasis tisu (Kotak 1) dan penyakit radang termasuk gastroenteritis akut, gastritis, dan penyakit radang usus (IBD) (disemak dalam [ 12, 13, 20, 21]). Walaupun setiap penyakit ini memaparkan patogen yang sama sekali berbeza, mereka berkongsi ciri kritikal: antara muka antara persekitaran dan badan terganggu dengan ketara. Walau bagaimanapun, terdapat perdebatan berterusan tentang sama ada perubahan dalam lapisan epitelium usus, khususnya yang menjejaskan fungsi imun semula jadinya, adalah punca atau akibat daripada penyakit yang disebutkan di atas.
Kebanyakan pengetahuan tentang isyarat PRR telah dikumpulkan daripada penyelidikan tentang sel hematopoietik. Ia telah menjadi satu cabaran untuk mendiskriminasi fungsi isyarat PRR dalam sel epitelium daripada sel imun yang menyusup. Halangan utama termasuk kesukaran untuk mengasingkan sel epitelium tulen dan meningkatkan antibodi yang boleh dipercayai terhadap PRR. Dengan kemajuan organoid yang berasal daripada sel stem epitelium usus, model eksperimen reduksionis kini tersedia yang membolehkan penyiasatan terhadap tindak balas imun semula jadi sel epitelium primer. Organoid ditakrifkan sebagai kultur sel berdimensi 3- terbitan sel stem yang mempunyai kapasiti penyusunan sendiri dan mengekalkan beberapa fungsi organ asal (cth rembesan, penapisan, penyerapan, pengecutan). Memandangkan organoid boleh ditanam sama ada daripada sel stem dewasa pemastautin tisu (ASC) atau daripada sel stem pluripotent (PSC), sel-sel tersebut tidak berubah. Bersama-sama, kedua-dua jenis organoid merangkumi repertoir organ yang luas yang boleh ditiru (disemak dalam [4, 22, 23]). Kedua-dua teknologi mempunyai kelebihan mereka (disemak dalam [4, 22, 23]). Sebagai contoh, kultur organoid terbitan ASC mempunyai potensi pengembangan yang besar dan agak homogen, dan organoid terbitan PSC adalah lebih kompleks dalam erti kata bahawa ia menggabungkan sel-sel asal perkembangan yang sangat berbeza (cth sel epitelium dan mesenkim). Organoid yang berasal dari PSC membenarkan analisis langkah-langkah perkembangan tetapi mungkin tidak mencapai tahap pembezaan penuh ke dalam lapisan epitelium seperti yang terdapat dalam vivo [24]. Organoid yang berasal dari ASC yang dihasilkan daripada tisu janin juga boleh membenarkan kajian pematangan epithelia janin sejak mereka berumur dalam budaya [24, 25].

Kajian ini akan menyerlahkan pandangan daripada kajian menggunakan organoid dan membincangkan potensi teknologi ini untuk kajian imuniti semula jadi epitelium. Kami memberi tumpuan kepada organisasi serantau dalam saluran gastrousus.
Identiti serantau dan isyarat imun semula jadi dalam saluran GI
Apabila melihat penyakit gastrousus adalah penting untuk ambil perhatian bahawa sesetengah daripada mereka terhad kepada bahagian tertentu saluran gastrousus. IBD termasuk penyakit Crohn (CD) dan kolitis ulseratif (UC), yang menunjukkan corak keradangan yang berbeza dan khusus penyakit: manakala UC bermula di rektum dan ditemui di kolon, CD boleh menjejaskan semua bahagian saluran GI dari rongga mulut hingga ke dubur. Tambahan pula, CD dicirikan oleh keradangan segmental, tidak berterusan dalam saluran GI, manakala UC biasanya digambarkan sebagai keradangan berterusan kolon (disemak dalam [26, 27]). Dalam esofagus, perut, dan kolon, kejadian kanser adalah tinggi, dan jangkitan serta keradangan boleh menggalakkan perkembangan dan perkembangan kanser ini (disemak dalam [28, 29]). Sebaliknya, transformasi malignan dalam usus kecil sangat jarang berlaku (disemak dalam [30]). Kekhususan segmen yang jelas bagi penyakit-penyakit ini dalam saluran GI kekal membingungkan, tetapi adalah menggoda untuk membuat spekulasi bahawa asal khusus wilayah mereka berakar umbi dalam gangguan khusus wilayah bagi sistem fungsi penghalang epitelium yang seimbang, imuniti semula jadi, dan pertumbuhan semula mukosa. . Oleh itu, adalah menarik untuk menyerlahkan perbezaan dalam segmen dalam saluran GI.

Saluran GI terdiri daripada beberapa segmen yang ditakrifkan secara anatomi dengan fungsi fizikal yang sangat berbeza (disemak dalam [31]). Fungsi utama perut ialah pencernaan makanan dan penyingkiran patogen yang masuk oleh asid gastrik. Nutrien tidak perlu mencapai lapisan epitelium perut; Oleh itu, badan banyak melabur dalam penghalang mukus pelindung, melindungi sel epitelium bukan sahaja daripada asidnya tetapi juga daripada kandungan luminal (disemak dalam [32, 33]). Sebaliknya, fungsi utama usus kecil bukan sahaja pencernaan tetapi juga pengambilan nutrien. Selaras dengan ini, usus kecil mempunyai luas permukaan yang diperbesarkan dengan ketara disebabkan oleh vili yang menonjol ke dalam lumen usus, di mana permukaan sel bersentuhan rapat dengan nutrien. Kebanyakan pencernaan berlaku di usus kecil proksimal, duodenum, dan jejunum, di mana vilinya panjang dan nipis. Jejunum mempunyai nisbah tertinggi sel Paneth yang merembeskan peptida antimikrobial [34], yang menghiasi lendir yang agak longgar, dengan itu menjaga lapisan epitelium dan memastikan crypts steril (disemak dalam [35]).
Villi menjadi semakin pendek dan lebih luas ke arah ileum (disemak dalam [36]), di mana sekali lagi, lendir mengambil alih bahagian perlindungan yang penting: dengan nisbah sel goblet tertinggi, ileum mempunyai lapisan mukus yang lebih tebal dan lebih rendah. kadar pencernaan dan penyerapan daripada jejunum [34] (disemak dalam [31]). Akhir sekali, kolon menyerap semula air dan melabur ke dalam penutup lendir yang luas, tebal dan berlapis dua untuk dapat menyimpan trilion bakteria komensal dengan selamat. Kolon tidak mempunyai vili dan crypt lebih kecil daripada usus kecil. Tiada sel Paneth, dan nisbah sel goblet boleh mencapai sehingga 25 peratus daripada lapisan epitelium [37]. Oleh itu, tiga segmen usus mempunyai strategi yang berbeza untuk mengekalkan jarak selamat antara sel epitelium dan mikrobiota. Pengiktirafan MAMP dan pengaktifan laluan imun adalah satu lagi lapisan interaksi ini dan oleh itu, adalah munasabah bahawa ia juga distrukturkan di sepanjang saluran GI (disemak dalam [38]). Walau bagaimanapun, ia kekal sebagai teka-teki yang menarik tentang apa sebenarnya yang membentuk struktur organisasi PRR.
Walaupun intuitif bahawa gen penting untuk fungsi serantau, seperti pencernaan dan pengambilan nutrien, mengikuti pembahagian ruang sepanjang paksi cephalocaudal (disemak dalam [39]), organisasi sedemikian tidak dijangka untuk isyarat imun semula jadi epitelium. Kajian terdahulu telah melaporkan peraturan isyarat PRR sebagai tindak balas kepada rangsangan dengan MAMP. Sebagai contoh, tindak balas TLR4 berkurangan selepas kelahiran, mungkin kerana pendedahan kepada LPS semasa penghantaran dan kolonisasi usus berikutnya [40]. Juga, rangsangan TLR9 dengan ligan CpG-DNA membawa kepada penurunan dalam ekspresi Tlr4 dan menghalang isyarat TLR4 [41]. Oleh itu, adalah dijangka bahawa hubungan dengan mikroorganisma, molekul mereka, dan metabolit dalam saluran GI akan membawa kepada pembungkaman ekspresi PRR ke arah lumen usus (disemak dalam [14]). Walau bagaimanapun, keputusan yang bercanggah, disebabkan oleh kesukaran teknikal seperti antibodi yang tidak boleh dipercayai yang menyasarkan TLR, membawa kepada kekeliruan di lapangan dan tidak jelas, sama ada PRR tertentu dinyatakan atau tidak (disemak dalam [42]). Tompok Utara awal untuk mRNA Tlr2 dan Tlr4 dalam sel epitelium terpencil ex vivo menunjukkan bahawa tahap ekspresi kedua-dua molekul Tlr ini adalah khusus segmen: Tlr2 dinyatakan terutamanya dalam kolon, manakala Tlr4 terutamanya dinyatakan dalam perut dan kolonPengarang menyebut ini " pembahagian strategik" TLR ini [43]. Kajian terbaru kini mendapati bahawa prinsip ekspresi khusus segmen ini melangkaui kedua-dua TLR ini, dan telah membongkar organisasi serantau yang sangat kompleks bagi isyarat PRR yang tidak selalu mengikut beban mikrob [44, 45].
Yang pertama daripada dua kajian datang daripada kumpulan Barton dan mendedahkan beberapa peringkat organisasi ekspresi TLR. Kumpulan itu menghasilkan lima jenis tikus wartawan, masing-masing membolehkan analisis ekspresi TLR2, 4, 5, 7, dan 9. TLR2 dan 5 dinyatakan dalam usus kecil dan kolon proksimal, TLR4 dinyatakan dalam kolon dan TLR7 dan 9 tidak dinyatakan. Ekspresi wartawan dalam organoid dari tikus ini meniru ekspresi in vivo, menunjukkan bahawa ungkapan itu bebas daripada sentuhan dengan mikrobiota atau dengan sel imun [45].
Kajian kedua menggunakan biobank organoid manusia dan murine yang baru dijana meliputi segmen saluran GI yang berbeza: korpus, pilorus, duodenum, jejunum, ileum, dan kolon. Analisis transkrip organoid mengesahkan corak ekspresi untuk TLR yang dilaporkan oleh kumpulan Barton, tetapi di samping itu mendedahkan sebahagian besar ekspresi pembezaan TLR, NLR, komponen inflammasom, dan gen berkaitan imuniti semula jadi yang lain (Rajah 3 dan [44] ]). Sebagai contoh, Nod2 terutamanya dinyatakan dalam perut, manakala ekspresi beberapa komponen laluan inflammasom seperti Nlrp1b, Nlrp6 dan Aim2 dihadkan kepada usus. Pelbagai reseptor dinyatakan secara seragam; sebagai contoh, ungkapan Tlr3 dikesan dalam setiap segmen saluran GI murine dalam jumlah yang tinggi, manakala Tlr5 dinyatakan dalam setiap segmen tetapi dalam jumlah yang rendah [44]. Akibatnya, setiap segmen nampaknya mempunyai pelengkap khusus reseptor imun semula jadi dan komponen isyaratnya sendiri.
Membandingkan murine dengan organoid gastrousus manusia menunjukkan bahawa dalam kedua-dua spesies prinsip organisasi kompleks komponen isyarat PRR adalah sama, tetapi profil ekspresi PRR individu mungkin berbeza. Sesetengah PRR, seperti TLR4 dan NLRP6, bercorak serupa di sepanjang saluran GI kedua-dua spesies. TLR4 dinyatakan terutamanya dalam perut dan kolon dan ekspresi NLRP6 terhad kepada segmen usus. Sebaliknya, beberapa PRR seperti TLR1 dan TLR2 menunjukkan corak yang berbeza antara kedua-dua spesies. Manakala dalam organoid murine, ekspresi kedua-duanya meningkat di sepanjang saluran GI dan paling tinggi dalam kolon, dalam ekspresi organoid manusia paling tinggi dalam perut dan menurun di sepanjang saluran GI [44]. Selain itu, ekspresi TLR5 lebih tinggi dalam organoid manusia, dengan tahap tertinggi diperhatikan dalam perut [44].
Seperti yang dinyatakan di atas, organoid juga membenarkan ujian sama ada laluan tertentu berfungsi dengan penambahan ligan dan analisis seterusnya ekspresi gen sasaran hiliran. Melengkapkan analisis ekspresi khusus rantau, kajian itu juga mendapati bahawa organoid manusia dan murine menunjukkan fungsi khusus wilayah: perut murine bertindak balas terhadap ligan TLR4 LPS, tetapi bukan ligan TLR2 PAM3CSK4 atau flagellin ligan TLR5, dengan mengawal selia NF- Gen sasaran κB Cxcl2. Murine jejunum mengimbangi Cxcl2 sebagai tindak balas kepada PAM3CSK4 dan flagellin, tetapi bukan sebagai tindak balas kepada LPS. Di samping itu, kolon menyatakan Cxcl2 sebagai tindak balas kepada semua 3 ligan yang diuji ini [44]. Sebaliknya, organoid manusia dari semua rantau menyatakan IL analog Cxcl2 manusia-8 sebagai tindak balas kepada flagellin, tetapi bukan sebagai tindak balas kepada LPS dan PAM3CSK [44]. Oleh itu, bukan sahaja ungkapan tetapi juga fungsi PRR dalam usus sangat teratur dan khusus segmen. Eksperimen ini dijalankan dengan menambahkan rangsangan pada medium organoid, justeru hanya merangsang bahagian basal, kerana bahagian apikal menghadap lumen organoid yang tertutup rapat. Eksperimen lain menunjukkan bahawa terdapat tahap organisasi yang lebih tinggi kerana ungkapan PRR dalam segmen boleh dihadkan kepada jenis sel tertentu atau bahkan lokasi subselular, seperti hanya petak basal. Ini digariskan dengan lebih terperinci di bawah.

Setiap kawasan saluran GI menyatakan set spesifik gen imun semula jadi. Walaupun generalisasi adalah sukar, data semasa mencadangkan bahawa TLRs dinyatakan paling tinggi dalam perut dan kolon, manakala usus kecil dicirikan oleh ekspresi komponen inflammasom. Pada masa ini, mekanisme molekul asas dan faedah evolusi tidak jelas.
Kami mengesyaki bahawa halangan fizikal dan kimia yang meliputi lapisan epitelium dalam segmen usus yang berbeza masing-masing memerlukan pemantauan ancaman khusus. Sebagai contoh, perut dan kolon kedua-duanya mempunyai lapisan lendir tebal dua lapis dengan lapisan mukus dalam melekat kuat pada lapisan epitelium, manakala usus kecil diliputi oleh lapisan lendir yang nipis dan likat [46]. Perlembagaan berbeza lapisan mukus pula berkemungkinan disebabkan oleh fungsi berbeza segmen usus masing-masing (pencernaan vs pengambilan nutrien vs penyerapan air). Boleh dibayangkan bahawa ketebalan lendir mempengaruhi jenis PRR yang diperlukan di tapak tertentu.
Sel khusus dengan fungsi imun dalam epitelium
Konsep lama dalam imuniti semula jadi epitelium ialah kewujudan pengecaman imun semula jadi khusus jenis sel. Prototaip sel epitelium khusus dengan fungsi pertahanan ialah sel mikrofold (M) dan sel Paneth—baru-baru ini dilengkapi dengan sel piala khusus, sel piala sentinel. Kewujudan sel khusus tersebut menyerlahkan sistem yang rumit dan berlebihan yang memastikan keseimbangan pengambilan nutrien, kewujudan bersama mikrobiota, dan pemantauan kemungkinan penceroboh. Pembezaan terarah organoid kini juga membolehkan kajian sel-sel ini dalam kultur sel.
Sel M terletak dalam epitelium yang berkaitan dengan folikel yang meliputi tompokan Peyer. Mereka mempunyai morfologi unik dengan sempadan berus yang tidak teratur dan struktur mikrovili yang berkurangan. Peranan mereka adalah untuk mengangkut antigen dalam lumen usus merentasi lapisan epitelium ke tisu limfoid yang mendasari untuk pengawalan tindak balas imun [47]. Sel M sendiri serta epitelium yang berkaitan dengan folikel ditunjukkan untuk menyatakan beberapa TLR [48] (disemak dalam [14]). Walau bagaimanapun, sel M sukar untuk dikaji kerana tidak banyak dalam tisu epitelium dan ia hanya ditemui berhampiran struktur kompleks tompok Peyer [47]. Namun begitu, sel M boleh dijana dalam kultur organoid menggunakan pembezaan terarah. Untuk ini, pengaktif reseptor ligan NF-κB (RANKL) ditambah kepada medium, yang mengimbangi faktor transkripsi SpiB, yang merupakan ciri pembezaan sel M [49]. Organoid yang dihasilkan daripada tikus yang kekurangan genetik untuk subunit NF-κB RelB tidak dapat menghasilkan sel M selepas rangsangan dengan RANKL, menunjukkan bahawa pengaktifan NF-κB adalah penting untuk pembangunan sel M [50]. Dalam budaya organoid manusia, sebagai tambahan kepada RANKL, limfotoksin, dan asid retinoik adalah penting untuk mendorong pembezaan ke arah sel M. Sel M ini secara khusus mengambil virus enterik seperti rotavirus dan reovirus, menunjukkan fenokopi yang betul bagi fungsi sel M semulajadi juga dalam kultur organoid [51]. Kerja organoid masa depan perlu terus membongkar kesalinghubungan isyarat NF-κB epitelium, pembangunan sel M, dan komunikasi dengan sel imun.
Sel Paneth bercampur dengan sel stem usus di dasar crypt dan telah lama dianggap sebagai penjaga petak sel stem kerana mereka merembeskan peptida antimikrobial. Sebagai contoh, sel Paneth merembeskan alpha-defensin, satu proses yang ditunjukkan dikawal oleh corak mikrob dan mekanisme imun semula jadi [52, 53]. Di samping itu, NOD2, yang pertama kali dikesan di kawasan crypt usus kecil murine [54], mengawal rembesan beberapa alpha-defensin oleh sel Paneth, yang seterusnya membawa kepada pengaktifan imuniti adaptif. Sel Paneth juga mengekspresikan TLR5 dan organoid yang diperkaya sel Paneth mengekspresikan paras TLR5 yang tinggi. Penjujukan RNA selepas rangsangan mendedahkan bahawa walaupun organoid usus kecil biasa hanya menyatakan tahap sederhana gen sasaran hiliran TLR5 sebagai tindak balas kepada rangsangan dengan flagellin, seperti sitokin yang disebabkan oleh NF-kB, organoid yang diarahkan untuk mengandungi bilangan sel Paneth yang tinggi melekapkan lebih kuat. tindak balas, menunjukkan bahawa sel Paneth adalah tindak balas utama kepada flagellin dalam usus kecil [44, 45]. Berbeza dengan ekspresi gen sasaran, tindak balas paling dramatik sel Paneth (degranulasi, penyemperitan, dan kematian sel) tidak dicetuskan oleh rangsangan dengan ligan TLR tetapi memerlukan rangsangan dengan interferon-gamma sitokin yang diperolehi sel imun profesional [55]. Keputusan daripada organoid ini adalah selaras dengan pemerhatian yang menunjukkan degranulasi dan penyemperitan sel Paneth selepas rangsangan interferon-gamma dalam vivo [55]. Ini menggariskan secara elegan sistem semakan dan imbangan dalam lapisan epitelium.

Sel goblet adalah penting untuk pertahanan epitelium kerana ia menghasilkan mucin glikosilasi yang penting untuk pembentukan penghalang mukus pada lapisan epitelium (disemak dalam [56]). Pada tikus, kekurangan MUC2 mengakibatkan keradangan spontan dan meningkatkan kerentanan terhadap jangkitan [57, 58]. Baru-baru ini, subset sel goblet bernama sel goblet sentinel telah diterangkan dalam kolon tetikus. Menggunakan eksplan tisu, kajian mengenal pasti penebalan lapisan mukus sebagai tindak balas kepada pendedahan kepada ligan TLR1/2, 4, dan 5, tetapi tidak kepada ligan TLR9, NOD1, dan NOD2 [59], bersesuaian dengan laporan Tlr 2 sebelum ini. ,4 dan 5 dinyatakan dalam sel goblet [60]. Penulis menentukan bahawa tindak balas juga bergantung kepada kehadiran inflammasom Nlrp6 dan bebas daripada limfosit mukosa menggunakan tisu daripada pelbagai tikus kalah mati [59]. Juga, laporan terdahulu menunjukkan kepentingan keradangan NLRP6 untuk rembesan lendir oleh sel goblet [61]. Pengimejan mendedahkan bahawa sel-sel goblet tertentu yang terletak di kawasan apikal crypt yang diendocytosed bertanda pendarfluor LPS [59]. Sel goblet sentinel yang baru dipanggil ini bukan sahaja mengalami degranulasi cepat dan pengusiran epitelium selepas rawatan dengan ligan TLR tetapi juga menghantar isyarat kalsium kepada sel jiran melalui jambatan sitoplasma antara sel yang dibentuk oleh persimpangan jurang, mungkin merangsang sel goblet lain untuk meningkatkan rembesan mukus [59] . Kedua-dua sel goblet dan sel Paneth tergolong dalam keturunan penyembur. Organoid membenarkan pembezaan terarah ke arah kedua-dua identiti sel, menghasilkan organoid yang banyak diperkaya sama ada dalam sel goblet atau sel Paneth [62]. Membandingkan transkrip organoid yang condong ini membantu mengenal pasti pengawal selia utama laluan pembezaan [63]. Analisis lanjut data omics serta analisis fungsi organoid ini akan membolehkan pemahaman yang lebih baik tentang peranan kedua-dua jenis sel dalam pertahanan imun semula jadi.
Akhir sekali, sel stem sendiri juga telah dilaporkan menyatakan PRR tertentu seperti TLR4 [64, 65], yang tidak terdapat pada vili usus kecil murine atau sel Paneth [66]. Di samping itu, majoriti ekspresi Nod2 dalam crypt murine nampaknya terhad kepada sel stem [67]. Rangsangan dengan ligan NOD2 meningkatkan kemandirian sel stem dan pembentukan organoid, menunjukkan bahawa rangsangan PRR juga boleh mengawal pertumbuhan semula epitelium usus secara langsung.
Tidak dinafikan, usaha semasa untuk menghasilkan atlas ekspresi gen yang meliputi setiap jenis sel dengan lebih terperinci tidak lama lagi akan memberikan gambaran yang lebih lengkap tentang organisasi selular isyarat imun semula jadi di dalam usus serta di seluruh badan [68-71]. ].
Kekutuban sel dan tindak balas imun semula jadi khusus sisi
Akhir sekali, adalah juga relevan untuk mempertimbangkan bahawa sel epitelium gastrousus sangat terpolarisasi, dengan bahagian apikal khusus menghadap lumen usus dengan mikrobiotanya, dan bahagian basolateral menghadap tisu. Di bawah homeostasis, MAMP mencapai bahagian apikal sahaja. Walau bagaimanapun, apabila halangan epitelium dilanggar, mikroorganisma juga boleh mencabar bahagian basolateral. Oleh itu, telah dihipotesiskan bahawa sel epitelium boleh secara selektif memasang tindak balas pro-radang hanya apabila dirangsang dari sisi basolateral, untuk memadankan ancaman yang ditimbulkan oleh isyarat. Sebagai contoh, TLR9 ditunjukkan untuk mendorong laluan isyarat yang berbeza apabila dirangsang dari bahagian apikal atau basolateral dalam garisan sel kanser [72] dan TLR5 hanya mendorong gen tindak balas NF-κB IL-8 apabila dirangsang dari bahagian basal [73 ].
Walaupun kajian terdahulu menggunakan pelabelan antibodi terhadap TLR telah melaporkan ungkapan khusus pada satu sisi sahaja (disemak dalam [14, 16]), analisis tikus wartawan TLR menggunakan pewarnaan tag HA tidak mengesahkan ini tetapi sebaliknya menunjukkan TLR2, 4, dan 5 reseptor pada kedua-dua bahagian apikal dan basal kolon proksimal serta beberapa TLR4 intraselular [45]. Perbezaan yang ketara ini mungkin disebabkan oleh pendekatan teknikal yang berbeza.
Organoid kini membenarkan ujian fungsi langsung terhadap tindak balas imun khusus sisi, kerana polarisasi selular dikekalkan dalam organoid. Di bawah keadaan standard apabila organoid ditanam dalam matriks ekstraselular, bahagian apikal menghadap lumen organoid dan bahagian basal menghadap matriks ekstraselular [74-76]. Apabila ditanam di luar matriks ekstraselular, kekutuban boleh terbalik [77, 78]. Apabila sel daripada organoid disemai ke permukaan kultur sel standard, seperti hidangan kultur atau transwell, bahagian apikal menghadap ke lumen telaga [44, 79-82].
Beberapa kajian menggunakan organoid untuk menguji fungsi umum PRR tertentu tanpa menangani perbezaan khusus antara rangsangan apikal dan basal. Kajian ini termasuk rangsangan dalam medium organoid, yang, di bawah keadaan standard, merangsang bahagian basal sel. Menggunakan teknik ini, regulasi gen sasaran hiliran NF-κB dikenal pasti selepas rangsangan basal dengan ligan TLR4 dalam perut, TLR2 dan 3 dalam usus kecil, dan TLR2, 3, 4, dan 5 dalam kolon tikus [44, 45, 83] dan kepada ligan TLR2 dan 5 dalam perut dan TLR5 dalam usus kecil dan kolon manusia [44]. Tambahan pula, rangsangan basal organoid kolon murine dengan agonis TLR4 menyebabkan pembezaan selular, terutamanya ke arah garis keturunan rembesan [64], manakala agonis NOD2 mendorong peningkatan kemandirian sel stem [67, 84], dan taurin merangsang NLRP6-pengawalseliaan bergantung. daripada gen sasaran hiliran inflammasom IL-18 [85]. Dalam semua kajian ini, rangsangan apikal tidak diuji.
Hanya beberapa kajian telah menangani fungsi khusus sampingan PRR. Perlu diperhatikan bahawa bertentangan dengan kajian yang menggunakan garis sel kanser terpolarisasi, setakat ini, tiada kajian yang menggunakan organoid telah mengenal pasti pengaktifan khusus sampingan gen proinflamasi yang bergantung kepada NF-κB yang tipikal. Monolayers Transwell yang diperoleh daripada organoid kolon manusia menyatakan tahap yang sama bagi gen sasaran NF-κB IL-6 apabila dirangsang dari bahagian apikal atau basal dengan ligan TLR1/2, 3, 4, 5, 7/8, dan 9 [82]. Organoid gastrik Murine juga bertindak balas terhadap rangsangan apikal dengan ligan TLR4 LPS dalam beberapa ujian, termasuk dalam transwells dan suntikan mikro LPS ke dalam lumen organoid [44]. Sel-sel epitelium usus kecil Murine tidak mengekspresikan gen sasaran NF-κB icam1 sebagai tindak balas kepada pelbagai ligan, tidak kira sama ada ia telah ditambah kepada organoid utuh, sekali gus merangsang bahagian basal, atau ditambah kepada sel tunggal yang tercerai, dengan itu merangsang semua sisi [55].
Walau bagaimanapun, melihat di luar tindak balas NF-κB, kajian baru-baru ini mengenal pasti fungsi khusus sampingan TLR3 dan kepentingannya dalam jangkitan virus [82]. Keputusan eksperimen dengan monolayers terhasil organoid kolon manusia menunjukkan bahawa ekspresi gen pertahanan virus kritikal jenis I dan jenis III interferon dikawal selia selepas rangsangan basal dengan agonis TLR3, tetapi tidak selepas rangsangan dengan agonis TLR lain. Apabila dijangkiti virus, begitu juga, tindak balas interferon organoid adalah lebih kuat apabila dijangkiti dari bahagian basal berbanding jangkitan dari bahagian apikal. Ini dapat dilihat dalam lapisan tunggal yang berasal dari organoid dan juga dalam organoid yang disuntik mikro dengan virus. Kajian selanjutnya mengenal pasti penyesuai pengisihan clathrin AP-1B sebagai molekul yang bertanggungjawab untuk ekspresi terpolarisasi TLR3. Sejajar dengan itu, tikus kekurangan Ap-1b menunjukkan tindak balas imun yang lebih teruk selepas jangkitan virus [82]. Ini mengesahkan fungsi terpolarisasi PRR dan menyerlahkan kepentingan tahap peraturan ini dalam memodulasi lagi pengiktirafan dan pertahanan patogen.
Setakat ini, tiada jawapan "satu saiz sesuai untuk semua" kepada soalan kekutuban, dan menyelesaikan sifat khusus tapak bagi isyarat PRR kekal sebagai tugas yang mencabar secara teknikal untuk masa hadapan.
Toleransi sebagai tindak balas kepada penjajahan dan sebagai program pembangunan lalai
Mekanisme yang menyumbang kepada organisasi imuniti semula jadi epitelium masih tidak jelas. Konsep utama dalam hal ini ialah induksi toleransi selepas penjajahan usus steril semasa kelahiran, apa yang dipanggil tingkap peluang (disemak dalam [86–88]). Konsep ini menyatakan tempoh permulaan sistem imun semula jadi dan adaptif selepas kelahiran, yang menetapkan peringkat untuk homeostasis imun dan interaksi mikrob perumah seterusnya.
Sistem imun neonatal dan imuniti semula jadi epitelium dilengkapi secara unik untuk menguasai peralihan ini daripada kemandulan kepada kewujudan bersama mikrobiota. Semasa lahir, usus neonatal manusia matang sepenuhnya dengan vili usus dan crypt yang mengandungi sel Paneth. Lapisan epitelium usus neonatal murine lebih tidak matang dan mengalami perubahan dramatik yang boleh diukur pada tahap transkrip yang membandingkan peringkat perkembangan yang berbeza [89] dan boleh dilihat dalam seni bina tisu dan pembezaan sel: Paksi crypt-villus belum terbentuk lagi dan percambahan sel adalah lebih rendah, tanpa penghijrahan sel atau pengelupasan. Ia tidak mengandungi sel Paneth matang; bagaimanapun, enterosit menghasilkan peptida antimikrob seperti cathelicidin (CRAMP) [90]. Sel Paneth muncul apabila crypts terbentuk 2 minggu selepas kelahiran [91]. Pada masa penyapihan, epitelium terbentuk sepenuhnya dengan crypt dan vili, enterosit, sel goblet, dan sel enteroendokrin; Sel Paneth telah mengambil alih pengeluaran peptida antimikrob; dan sel goblet telah meningkatkan pengeluaran mucins untuk membentuk lapisan mukus (disemak dalam [92]).
Peralihan epitelium yang bergantung kepada usia ini berjalan seiring dengan penurunan beransur-ansur ekspresi TLR5 dalam epitelium usus kecil. Pada masa yang sama, ekspresi TLR3 meningkat semasa tempoh neonatal. PRR lain, seperti TLR2, 4, dan 9, dinyatakan pada tahap yang sama dalam tikus neonatal dan dewasa [45, 93].
Mekanisme yang membawa kepada peraturan ekspresi dan fungsi PRR selepas kelahiran masih tidak jelas. Seperti yang dinyatakan di atas, beberapa kajian telah mencadangkan sumbangan alam sekitar, khususnya penjajahan mikrob, kepada peraturan ekspresi PRR selepas kelahiran [40, 41] (disemak dalam [14]). Walau bagaimanapun, tikus bebas kuman vs bebas patogen spesifik tidak menunjukkan perbezaan dalam ekspresi TLR sama ada dalam usus kecil atau kolon, menunjukkan bahawa tiada pengawalseliaan TLR3 atau pengurangan TLR5 dalam tempoh awal ini bergantung kepada mikrobiota [45, 93]. Juga, dalam organoid, ekspresi banyak, tetapi tidak semua, komponen isyarat PRR telah ditakrifkan dalam organoid daripada tisu yang tidak pernah bersentuhan dengan produk mikrob [44]. Ini menunjukkan bahawa sebahagian besar organisasi laluan isyarat imun semula jadi ditakrifkan secara bebas daripada sentuhan dengan mikrobiota dan nampaknya ditentukan oleh proses pembangunan lalai, seperti yang digariskan di atas, yang membentuk identiti tisu umum di sepanjang saluran GI. . Ini tidak mengecualikan penalaan lanjut ekspresi PRR oleh faktor persekitaran semasa dewasa.
Kepentingan pengawalan tepat pada masanya interaksi mikrob epitelium menjadi jelas apabila epitelium yang tidak matang secara pramatang berhadapan dengan penjajahan mikrob: bayi pra-matang terdedah kepada perkembangan necrotizing enterocolitis (NEC), yang dicirikan oleh nekrosis usus, sepsis sistemik, dan pelbagai organ. kegagalan. Walaupun patogenesis dianggap multifaktorial, beberapa kajian telah menunjukkan bahawa ia berkembang sebagai tindak balas kepada ketidakseimbangan antara isyarat proinflamasi dan mekanisme pembaikan dalam usus pramatang (disemak dalam [94]) dan sumbangan PRR telah dicadangkan [41, 65, 95]. –97]. Beberapa kajian telah menggunakan organoid janin manusia [24, 98, 99], organoid murine normal yang terdedah kepada bakteria dan hipoksia untuk memodelkan NEC [100], atau organoid daripada model NEC murine serta daripada pesakit NEC [101]. Kajian masa depan akan menggunakan model organoid yang mantap dan baharu ini untuk mentakrifkan lagi sumbangan epitelium dalam NEC.
Memodelkan aspek IBD yang bergantung kepada epitelium dengan organoid
Kehilangan integriti penghalang epitelium usus adalah ciri penentu IBD, iaitu CD dan UC, dan nampaknya disebabkan oleh interaksi pelbagai faktor kecenderungan genetik, faktor persekitaran, perubahan mikrobiota usus, dan perubahan tindak balas imun tempatan dan sistemik (disemak semula). dalam [27]). Terapeutik semasa kebanyakannya menyasarkan tindak balas imun (yang menyimpang) dalam IBD, yang dikaitkan dengan kadar tinggi bukan responden dan kesan sampingan (disemak dalam [27]). Pemahaman yang lebih baik tentang sumbangan khusus epitelium kepada patofisiologi IBD diperlukan untuk mengenal pasti sasaran terapeutik baru yang mungkin juga boleh memberi kesan secara langsung kepada pemulihan halangan epitelium usus dan dengan itu penyembuhan mukosa.
Untuk mendapatkan pandangan tentang patologi epitelium, beberapa kumpulan telah menubuhkan biobank hidup yang terdiri daripada organoid yang dihasilkan daripada pesakit individu dengan UC atau CD. Walaupun pendekatan ini jelas, setakat ini, hanya beberapa kajian telah melaporkan hasil daripada organoid yang diperoleh daripada kumpulan pesakit ini [102-104]. Ini mungkin dijelaskan oleh pemerhatian bahawa organoid daripada pesakit dengan IBD lebih sukar untuk dihasilkan. Pengalaman kami sendiri ialah organoid yang dihasilkan daripada pesakit CD berkembang dengan lebih perlahan semasa laluan pertama dan beberapa sampel telah hilang— yang dikaitkan dengan kadar pencemaran bakteria yang lebih tinggi dalam kultur [105].
Pencirian organoid yang diperoleh daripada pesakit dengan IBD mendedahkan fenotip dengan saiz yang berkurangan dan kapasiti tunas, peningkatan kadar kematian sel, serpihan luminal, dan polarisasi sel epitelium separa terbalik [106]. Perbandingan global organoid daripada pesakit UC atau CD dan kawalan sihat menunjukkan bahawa perbezaan transkrip dan metilasi yang dilihat dalam epitelium usus dikekalkan secara in vitro [102, 103, 107]. Juga, kajian awal daripada organoid yang dihasilkan daripada pesakit dengan CD mencadangkan perubahan kekal sel stem usus dalam IBD. Ini berdasarkan pemerhatian bahawa organoid yang dihasilkan daripada lesi CD aktif mengekalkan tahap ekspresi tinggi penanda sel stem epitelium usus [108]. Ini sedikit sebanyak disahkan dalam kajian baru-baru ini di mana organoid kolon yang diperolehi daripada pesakit IBD kanak-kanak menunjukkan corak ekspresi berpanjangan gen penyampaian antigen [109].
Memfokuskan pada perubahan dalam fungsi penghalang epitelium usus, termasuk kehilangan persimpangan ketat dan desmosom, yang biasanya ditemui dalam IBD [110], telah ditunjukkan bahawa organoid daripada pesakit CD mengekalkan fenotip perubahan persimpangan ini di bawah keadaan kultur [105]. Ini terutamanya berlaku apabila organoid dihasilkan daripada tapak keradangan yang teruk [105]. Pengurangan dalam protein junctional juga boleh diinduksi dalam organoid daripada penderma yang sihat dengan penggunaan sitokin proinflamasi TNF- dan/atau IFN- [106, 111]. Walau bagaimanapun, corak tetap perubahan protein simpang dalam organoid daripada pesakit dengan IBD diperhatikan hanya pada tahap protein tetapi tidak pada tahap mRNA [105].
Pemerhatian ini mencadangkan bahawa beberapa perubahan ditetapkan dalam organoid daripada pesakit IBD. Pemerhatian bahawa beberapa, tetapi tidak semua, perubahan kekal hanya kelihatan pada protein, tetapi bukan tahap RNA, menunjukkan bahawa terdapat perubahan kekal dalam pengubahsuaian selepas transkrip atau degradasi protein dalam organoid daripada pesakit IBD. Ini bagaimanapun masih perlu disiasat secara terperinci.
Apa sebenarnya yang mendorong perubahan kekal dalam corak ekspresi epitelium yang meradang tidak jelas. Kesan mikrobiota telah lama disyaki; bagaimanapun, kajian baru-baru ini menunjukkan bahawa kesan mikrobiota pada epitelium hilang dari semasa ke semasa [112]. Kajian itu membandingkan beberapa kemudahan tetikus kerana komposisi mikrobiom berbeza koloni tetikus telah dikenal pasti sebagai faktor yang mengelirukan dalam kajian vivo. Untuk menjelaskan kesan ini, kajian membandingkan isolat epitelium dan kultur organoid daripada tikus bebas kuman dan dua koloni tikus bebas patogen khusus yang berasingan dengan mikrobiota yang berbeza. Walaupun epitelium yang baru diasingkan menunjukkan kesan pendedahan mikrobiota pada tahap RNA dan protein, kesan ini hilang selepas beberapa minggu kultur organoid usus kecil [112]. Juga, perbandingan global ekspresi gen organoid yang dijana daripada kawasan yang meradang atau tidak meradang bagi pesakit IBD yang sama menunjukkan bahawa organoid IBD di kawasan yang meradang telah kehilangan ekspresi gen keradangan selepas beberapa minggu dalam budaya. Transkriptom organoid kemudiannya dikelompokkan bagi setiap pesakit; Oleh itu, perbezaan kekal antara IBD dan kawalan sihat kekal. Fenotip keradangan dalam organoid IBD kemudiannya boleh diinduksi semula dengan penambahan koktel sitokin [107]. Secara keseluruhannya, ini menunjukkan bahawa perubahan kekal yang diperhatikan dalam organoid daripada pesakit IBD adalah bebas daripada sentuhan dengan mikrobiota atau sitokin.
Oleh itu, walaupun adalah munasabah untuk membuat spekulasi bahawa beberapa perubahan kekal dalam sel epitelium usus daripada pesakit dengan IBD mungkin disebabkan oleh perubahan dalam isyarat imun semula jadi, bukti untuk ini pada masa ini adalah terhad. Di samping itu, tidak semua perubahan epitelium yang diperhatikan di kawasan yang meradang dalam usus dipelihara secara kekal dalam epitelium yang disucikan, menunjukkan sumbangan penting dari persekitaran tempatan. Pada masa hadapan, kajian baharu dengan model organoid yang lebih kompleks, juga menggabungkan sel imun, rangsangan sitokin radang, dan kultur bersama dengan mikroorganisma, seharusnya membantu menangani hipotesis ini dengan lebih terperinci.
Kesimpulan, perspektif masa depan dan Outlook
Ringkasnya, walaupun banyak penyakit dalam saluran GI masih tidak difahami sepenuhnya, bukti yang semakin meningkat menunjukkan peranan penting epitelium gastrousus dalam patogenesis kebanyakannya-walaupun peranan khususnya masih tidak jelas.
Pengetahuan terhad tentang fungsi imun semula jadi epitelium gastrousus telah dikaitkan dengan kekurangan model eksperimen yang sesuai. Dengan pelaksanaan teknologi organoid, satu langkah besar telah diambil untuk mengatasi masalah ini. Organoid yang dihasilkan dari setiap kawasan saluran gastrousus akan menambah dengan ketara kepada pengetahuan sedia ada. Seperti yang didedahkan oleh kajian terdahulu, penjanaan organoid memberikan kelebihan penting untuk dapat memerhatikan tindak balas sel gastrousus primer berbanding garis sel yang diubah, yang kebanyakannya dihasilkan daripada tumor malignan gastrousus. Salah satu ciri organoid yang paling menarik ialah ia mengekalkan ciri khusus segmen saluran gastrousus yang dijana daripadanya sebagai sebahagian daripada identiti sel mereka semasa dewasa. Menurut kajian eksperimen semasa, identiti serantau ditetapkan dalam sel stem gastrousus. Dalam konteks ini, isu yang tinggal adalah untuk menentukan dengan tepat bagaimana dan bila semasa pembangunan pengaturcaraan intrinsik ini berlaku.

Apabila melihat konsep khusus tentang bagaimana epitelium boleh bertindak balas atau berinteraksi dengan persekitaran, teknologi organoid kini telah membolehkan pencahayaan ekspresi dan fungsi khusus pembezaan dan segmen PRR dalam epitelium gastrousus. Akibat fungsi keseluruhan untuk sistem pengawalseliaan yang kompleks dalam keseluruhan saluran gastrousus masih tidak jelas dan perlu ditangani pada masa hadapan. Untuk ini, ia juga penting untuk mengkultur organoid dengan sel imun (disemak dalam [113]), sel sistem saraf enterik [114], dan faktor luminal seperti kultur bersama bakteria (disemak dalam [115]) (Rajah . 4).
Aspek penting lagi ialah organoid yang dihasilkan daripada tisu pesakit yang terjejas oleh penyakit GI seperti IBD mengekalkan beberapa ciri yang dilihat dalam spesimen tisu yang sepadan yang diperoleh daripadanya. Ini menawarkan kemungkinan unik untuk menguraikan lagi sumbangan khusus epitelium dan penyakit kepada patogenesis penyakit GI-bukan sahaja yang melibatkan perubahan yang disebabkan oleh keradangan tetapi juga yang melibatkan perubahan dalam penyakit malignan. Kedua-duanya mungkin ternyata melibatkan sumbangan khusus imuniti semula jadi yang berasal dari epitelium. Untuk ini, penubuhan "biobank hidup" yang sistematik akan menjadi langkah penting. Sebagai visi untuk masa depan, biobank hidup tersebut boleh disambungkan pada biobank sedia ada, yang pada masa ini menyediakan biobahan "mati" semata-mata. Ini akan mewakili satu lagi langkah penting bukan sahaja untuk penyelidikan tetapi juga dalam memudahkan diagnostik dan terapi individu untuk pesakit.
Kotak 1. Imuniti semula jadi dan sel epitelium dalam saluran GI tidak jelas sama ada kesan yang diperhatikan adalah disebabkan oleh isyarat imun semula jadi dalam sel epitelium atau sel imun profesional.
Untuk merungkai hubungan antara sel imun profesional dan sel epitelium, beberapa kajian telah menggunakan kalah mati khusus epitelium, atau lebih baru-baru ini, organoid epitelium. Dalam model tetikus, tiada pemadaman khusus epitelium PRR yang membawa kepada keradangan spontan. Walau bagaimanapun, tikus dengan kalah mati khusus epitelium MyD88 lebih terdedah kepada kolitis eksperimen dan menunjukkan gangguan penghalang yang teruk, goblet terjejas dan tindak balas sel Paneth [121], dan mengurangkan pengeluaran mucin dan peptida antimikrobial [121, 122]. Organoid usus kecil tidak melekapkan tindak balas keradangan kepada beberapa ligan PRR yang telah dimurnikan [55], walaupun ini tidak boleh digeneralisasikan dan bergantung pada spesies, lokasi, dan umur tisu organoid dihasilkan daripada [44, 45].
Ketiadaan fenotip keradangan spontan dalam model kalah mati PRR khusus sel epitelium menyokong hipotesis bahawa faktor selain daripada tindak balas keradangan umum epitelium mempunyai kesan ke atas homeostasis epitelium. Sebagai contoh, rangsangan dengan NOD2 agonis muramyl dipeptide (MDP) meningkatkan bilangan organoid yang tumbuh daripada sel stem terpencil, menunjukkan bahawa isyarat imun semula jadi menyokong kemandirian sel stem [67, 84]. Tambahan pula, data daripada tikus menyerlahkan kepentingan kesan anti-apoptosis isyarat NF-κB sebagai tindak balas kepada rangsangan lain, seperti TNF- [123]. Menariknya, pada manusia, polimorfisme dalam gen imun semula jadi termasuk NOD2 dan TLR4 dikaitkan dengan peningkatan risiko untuk membangunkan IBD [124] dan penyumbatan TNF- kini merupakan rawatan yang paling mujarab untuk IBD dalam sesetengah pesakit (disemak dalam [125]).
Gambar muncul, di mana tahap rangsangan imun semula jadi yang rendah adalah penting untuk rembesan mukus, integriti penghalang, dan kemandirian sel epitelium. Kemerosotannya mungkin membenarkan pemindahan bakteria usus dari lumen ke dalam tisu subepitelium, yang membawa kepada keradangan.

Ucapan terima kasih
Kami berterima kasih kepada Ömer Kaya untuk bantuan dengan ilustrasi dan Rike Zietlow untuk menyunting.
Sumbangan pengarang
Idea: SB Konsep awal: SB dan Ö.K.; carian literatur: Ö.K., NS dan SB; Draf awal: Ö.K. Menyemak semula, menulis semula, menambah bahagian: NS, SB Semua pengarang menyemak semula manuskrip akhir secara kritis.
Pembiayaan
Pembiayaan Open Access didayakan dan dianjurkan oleh Projekt DEAL. Kerja ini disokong Deutsche Forschungsgemeinschaft (DFG GRK 2157; Model Tisu 3D untuk Mengkaji Jangkitan Mikrob oleh Patogen Manusia, Projek 10, hingga SB), Pusat Penyelidikan Klinikal Antara Disiplin (IZKF; www.med.uni-wuerzburg.de/izkf /startseite) di Würzburg (Berikan AD-427 kepada NS dan SB), dan DFG SPP1982 SCHL1962/5-2 kepada NS.
Pengisytiharan
Konflik kepentingan
Pengarang mengisytiharkan tiada kepentingan bersaing.
Buka Akses
Artikel ini dilesenkan di bawah Creative Commons Atribusi 4.0 Lesen Antarabangsa, yang membenarkan penggunaan, perkongsian, penyesuaian, pengedaran dan pengeluaran semula dalam sebarang medium atau format, asalkan anda memberikan kredit yang sewajarnya kepada pengarang asal ) dan sumbernya, berikan pautan kepada lesen Creative Commons, dan nyatakan jika perubahan telah dibuat. Imej atau bahan pihak ketiga lain dalam artikel ini disertakan dalam lesen Creative Commons artikel melainkan dinyatakan sebaliknya dalam garis kredit kepada bahan tersebut. Jika bahan tidak disertakan dalam lesen Creative Commons artikel dan penggunaan yang anda maksudkan tidak dibenarkan oleh peraturan berkanun atau melebihi penggunaan yang dibenarkan, anda perlu mendapatkan kebenaran terus daripada pemegang hak cipta.
Rujukan
1. Goodwin CS (1984) Mikrob dan jangkitan usus
2. Sekirov I, Russell SL, Antunes LCM, Finlay BB (2010) Mikrobiota usus dalam kesihatan dan penyakit. Physiol Wahyu 90:859–904
3. Simon GL, Gorbach SL (1986) Mikroflora usus manusia. Gali Dis Sci 31:147S–162S
4. Bartfeld S, Clevers H (2017) Organoid yang berasal dari sel stem dan aplikasinya untuk penyelidikan perubatan dan rawatan pesakit. J Mol Med:1–10. https://doi.org/10.1007/s00109-017-1531-7
5. Barker N (2014) Sel stem usus dewasa: pemacu kritikal homeostasis epitelium dan penjanaan semula. Nat Rev Mol Sel Biol 15:19–33
6. Bartfeld S, Koo BK (2017) Sel stem gastrik dewasa dan nichenya. Wiley Interdiscip Rev Dev Biol 6:e261. https://doi.org/ 10.1002/wdev.261
7. Liwinski T, Zheng D, Elinav E (2020) Mikrobiom dan reseptor imun semula jadi sitosol. Immunol Wahyu 297:1–18
8. Burgueño JF, Abreu MT (2020) Reseptor seperti Tol Epitelium dan peranannya dalam homeostasis usus dan penyakit. Nat Rev Gastroenterol Hepatol 17:263–278
9. Christian S, Kanneganti TD (2020) Inflammasom dan garis halus antara pertahanan dan penyakit. Curr Opin Immunol 62:39–44
10. Ying L, Ferrero RL (2019) Peranan isyarat NOD1 dan ALPK1/TIFA dalam imuniti semula jadi terhadap Helicobacter pylori. Jangkitan ms:159–177
11. Takeuchi O, Akira S (2010) Reseptor pengecaman corak dan keradangan. Sel 140:805–820
12. Peterson LW, Artis D (2014) Sel epitelium usus: pengawal selia fungsi penghalang dan homeostasis imun. Nat Rev Immunol 14:141–153
13. Pott J, Hornef M (2012) Isyarat imun semula jadi pada epitelium usus dalam homeostasis dan penyakit. EMBO Rep 13:684–698
14. Abreu MT (2010) Isyarat reseptor seperti tol dalam epitelium usus: bagaimana pengecaman bakteria membentuk fungsi usus. Nat Rev Immunol 10:131–144
15. Zhang K, Hornef MW, Dupont A (2015) Epitelium usus sebagai penjaga integriti halangan usus. Mikrobiol Sel 17:1561–1569
16. Yu S, Gao N (2015) Membahagikan reseptor seperti tol sel epitelium usus untuk pengawasan imun. Sel Mol Life Sci 72: 3343–3353
17. Zhou P, She Y, Dong N, Li P, He H, Borio A, Wu Q, Lu S, Ding X, Cao Y, Xu Y, Gao W, Dong M, Ding J, Wang DC, Zamyatina A, Shao F (2018) Alpha-kinase 1 ialah reseptor imun semula jadi sitosol untuk ADP-heptosa bakteria. alam semula jadi. 561:122–126
18. Milivojevic M, Dangeard AS, Kasper CA, Tschon T, Emmenlauer M, Pique C, Schnupf P, Guignot J, Arrieumerlou C (2017) ALPK1 mengawal TIFA/TRAF6-imuniti semula jadi yang bergantung kepada heptose{{5} },7-bifosfat bakteria gram-negatif. PLoS Pathog 13:e1006224. https://doi.org/10.1371/journal.ppat. 1006224
19. Zimmermann S, Pfannkuch L, Al-Zeer MA et al (2017) ALPK1- dan tindak balas imun semula jadi yang bergantung kepada TIFA yang dicetuskan oleh sistem rembesan jenis IV helicobacter pylori. Rep Sel 20:2384– 2395
20. Abreu MT, Fukata M, Arditi M (2005) TLR isyarat dalam usus dalam kesihatan dan penyakit. J Immunol 174:4453–4460 174/8/4453 [pii]
For more information:1950477648nn@gamil.com
