Akromegali Disertai Diabetes Mellitus Dan Penyakit Buah Pinggang Polikistik
Mar 04, 2022
Untuk maklumat lanjut:emily.li@wecistanche.com
Daisuke Otani, Takaaki Murakami, Takeshi Matsubara, Masato Hojo, Takuro Nakae, Koki Moriyoshi, Akihiro Yasoda, Ryota Usui, Hisato Tatsuoka, Masahito Ogura, Nobuya Inagaki dan Taizou Yamamoto
1) Jabatan Diabetes, Endokrinologi dan Pemakanan, Pusat Pengajian Perubatan Siswazah Universiti Kyoto, Kyoto, Jepun
2) Jabatan Diabetes dan Endokrinologi, Hospital Besar Shiga, Moriyama, Jepun
3) Jabatan Nefrologi, Sekolah Siswazah Perubatan Universiti Kyoto, Kyoto, Jepun
4) Jabatan Pembedahan Saraf, Hospital Besar Shiga, Moriyama, Jepun
5) Jabatan Patologi Diagnostik, Pertubuhan Hospital Kebangsaan Pusat Perubatan Kyoto, Kyoto, Jepun
6) Pusat Penyelidikan Klinikal, Pertubuhan Hospital Kebangsaan Pusat Perubatan Kyoto, Kyoto, Jepun
Abstrak
Akromegali dicirikan oleh rembesan hormon pertumbuhan berlebihan (GH) autonomi, secara amnya disebabkan oleh adenoma pituitari yang menghasilkan GH, dan dikaitkan dengan pelbagai komorbiditi sistemik termasuk diabetes mellitus. Polikistikbuah pinggangpenyakit(PKD) dicirikan oleh pertumbuhan banyak sista dalam buah pinggang yang merosotbuah pinggangfungsi. Walaupun kemungkinan kesan buah pinggang akibat pendedahan GH yang berlebihan telah menjadi isu semasa dalam perubatan eksperimen, hanya lima kes akromegali yang wujud bersama dan PKD telah dilaporkan sebelum ini, dan sedikit diketahui mengenai pengaruh akromegali padabuah pinggangpenyakit. Kami merawat seorang lelaki berumur 50-tahun dengan diabetes mellitus yang menunjukkan penurunan mendadak dan cepatbuah pinggangfungsibersama dengan peningkatan proteinuria, yang membawa kepada diagnosis PKD dan akromegali. Tahap protein kencingnya meningkat bersama-sama dengan rembesan GH yang berlebihan dan kawalan glisemik yang semakin teruk. Peningkatan jumlah isipadu buah pinggang juga diperhatikan. Pembedahan transsphenoidal untuk adenoma pituitari telah berjaya dilakukan. Peningkatan ketara hiperglikemia dan proteinuria diperhatikan selepas pembedahan, tetapi fungsi buah pinggang tidak berubah. Kursus klinikal pesakit mencadangkan aspek biasa rembesan GH yang berlebihan sebagai faktor mempercepatkan perkembangan nefropati diabetik dan PKD melalui laluan langsung dan tidak langsung. Walaupun akromegali yang wujud bersama dan PKD jarang berlaku secara klinikal, kewaspadaan untuk diagnosis awal akromegali adalah sesuai pada pesakit diabetes dan/atau PKD, terutamanya bagi mereka yang menunjukkan pemburukan disfungsi buah pinggang yang tidak dijangka.
Kata kunci: Akromegali, Diabetes mellitus,Pertumbuhan hormon, Polikistikbuah pinggangpenyakit

ACROMEGALY adalah gangguan luar biasa yang dicirikan oleh rembesan autonomi dan berlebihan hormon pertumbuhan (GH) yang biasanya disebabkan oleh adenoma pituitari yang menghasilkan GH [1, 2].
Insiden tahunan akromegali dilaporkan kira-kira 3-4 kes setiap juta dalam kebanyakan kajian; kelaziman berkisar antara 85 hingga 133 kes setiap juta dalam kajian terkini termasuk di Jepun [3]. Akromegali dikaitkan dengan pelbagai komorbiditi sistemik termasuk penyakit kardiovaskular, komplikasi metabolik (hiperglikemia dan hiperlipidemia), penyakit pernafasan, osteoarthropathy, patah tulang belakang, dan kemungkinan peningkatan risiko beberapa neoplasma dan dengan peningkatan kematian apabila tidak dirawat dengan secukupnya [2, 3]. Prevalens diabetes mellitus pada pesakit dengan akromegali telah dilaporkan lebih tinggi daripada populasi normal, antara 11 hingga 53 peratus [3]. Walaupun GH merangsang rembesan insulin, hormon ini kebanyakannya mendorong rintangan insulin dengan menentang tindakan insulin dan seterusnya meningkatkan prevalens diabetes mellitus [3].
Polikistikbuah pinggangpenyakit(PKD) adalah gangguan buah pinggang yang dicirikan oleh pertumbuhan banyak sista dalam buah pinggang yang menggantikan parenkim buah pinggang dan merosot fungsi buah pinggang [4]. Terdapat dua jenis PKD: PKD dominan autosomal (ADPKD) yang disebabkan oleh mutasi germline dalam gen PKD1 dan PKD2, yang biasanya didiagnosis pada masa dewasa, dan PKD resesif autosomal (ARPKD), yang biasanya dikenal pasti dalam beberapa minggu pertama selepas kelahiran. ADPKD dianggarkan menjejaskan satu individu bagi setiap 4,033 penduduk di Jepun [5] dan bertanggungjawab untuk 5 hingga 10 peratus kes peringkat akhirbuah pinggangpenyakit[4]. Pesakit yang terjejas biasanya hadir dengan buah pinggang yang diperbesarkan dengan pelbagai sista dua hala [6]. Isipadu buah pinggang, serta proteinuria dan kadar penapisan glomerular (GFR), boleh digunakan sebagai penanda untuk perkembangan penyakit; perubahan dalam fungsi buah pinggang sangat dikaitkan dengan jumlah buah pinggang dalam pesakit ADPKD Jepun [7].
Walaupun beberapa kes akromegali dan ADPKD yang wujud bersama telah dilaporkan [8-12], sedikit yang diketahui tentang pengaruh akromegali terhadap keterukan dan perkembangan PKD, terutamanya dalam kes yang turut mempunyai nefropati diabetik. Kami melaporkan di sini kes akromegali yang jarang berlaku disertai oleh kedua-dua diabetes mellitus dan PKD yang menunjukkan penurunan pesat dalam fungsi buah pinggang dan peningkatan dalam jumlah keseluruhan buah pinggang. Kes sekarang menyoroti kesan potensi rembesan GH yang berlebihan padabuah pinggangfungsidan struktur serta kepentingan klinikal kewaspadaan untuk akromegali dalam kes diabetes dan disfungsi buah pinggang progresif yang berkaitan dan PKD.

Cistanche baik untuk buah pinggang
Pembentangan Kes
Seorang lelaki berusia 50-tahun dengan kawalan glisemik yang semakin teruk telah dirujuk ke klinik kami untuk rawatan diabetes mellitus. Dia tidak mempunyai sejarah keluarga yang menghidap diabetes, pituitari atau tumor endokrin lain termasuk pelbagai neoplasia endokrin jenis 1. Walaupun dia tidak mempunyai sejarah keluarga PKD yang kukuh, bapanya mempunyaihipertensidan meninggal dunia akibat pecah aneurisme aorta, tetapi tiada maklumat klinikal yang lebih terperinci mengenai penyakit buah pinggang tersedia. Pesakit kami tidak mempunyai sebarang sekatan diet dan menafikan mengambil alkohol.
Sejarah perubatannya mendedahkan bahawa dia sedang mengambil ubat termasuk valsartan (160 mg sehari), amlodipine (1{{20}} mg sehari) dan carvedilol (20 mg sehari) untuk hipertensi sejak dia berumur 36 tahun. Pada usia 46 tahun, beliau telah didiagnosis dengan diabetes mellitus jenis 2 berdasarkan paras hemoglobin A1c (HbA1c) 9.7 peratus dan paras glukosa darah 399 mg/dL dengan keputusan negatif untuk antibodi dekarboksilase asid anti-glutamat dan telah ditetapkan. metformin (500 mg sehari) dan glimepiride (0.5 mg sehari). Pada masa diagnosis awal diabetesnya, tiada penemuan yang menunjukkan nefropati diabetik [protein urinalisis: negatif, nisbah albumin/kreatinin (Cr) air kencing: 7.1 mg/gCr] atau retinopati diperhatikan. Sembilan bulan kemudian, dia mengalami mikroalbuminuria [nisbah albumin/Cr air kencing: 285.5 mg/gCr]. Pada usia 48 tahun, proteinuria terang-terangan berkembang [nisbah protein air kencing/Cr (UPCR): 0.96 g/GCR, serum Cr (SCr): 0.96 mg/dL, anggaran GFR (eGFR): 67 mL/min/1.73 m2 ], walaupun tahap HbA1cnya dikekalkan sehingga 6.4 peratus di bawah rawatan perubatan yang disebutkan di atas. Walau bagaimanapun, pada usia 50 tahun, kawalan glisemik pesakit bertambah teruk (HbA1c: 7.6 peratus), dan dia mengalami retinopati diabetik pra proliferatif dua hala. Dia kemudiannya dirujuk ke klinik kami (Gamb. 1).

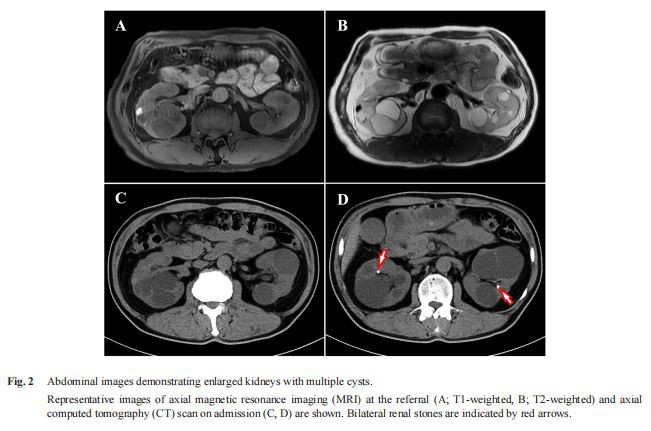
Pada lawatan pertamanya, UPCRnya dinaikkan kepada 1.20 g/GCR serentak dengan penurunan eGFR (40 mL/min/1.73 m2 ). Ultrasonografi perut dan pengimejan resonans magnetik (MRI) mendedahkan buah pinggang yang diperbesarkan dengan pelbagai sista dua hala (Rajah 2A, 2B), yang mencadangkan PKD. Anggaran jumlah isipadu buah pinggang (TKV) ialah 1,078 mL. Biopsi buah pinggang tidak dilakukan kerana banyak sista buah pinggang. Selepas peningkatan sementara kawalan glisemiknya mungkin disebabkan oleh panduan pemakanan tambahan, HbA1cnya meningkat semula, dan UPCRnya meningkat dengan cepat (Rajah 1). Semasa susulan, temu bual semula yang teliti mendedahkan bahawa pesakit telah melihat pembesaran secara beransur-ansur pada tangan dan kakinya selama beberapa tahun. Sebagai tambahan kepada diabetes bukan bergantung kepada insulin yang refraktori rawatan, ciri mukanya yang kasar dan pembesaran tangan dan kaki membawa kepada syak wasangka akromegali. Oleh itu, beliau telah dimasukkan untuk penilaian lanjut.
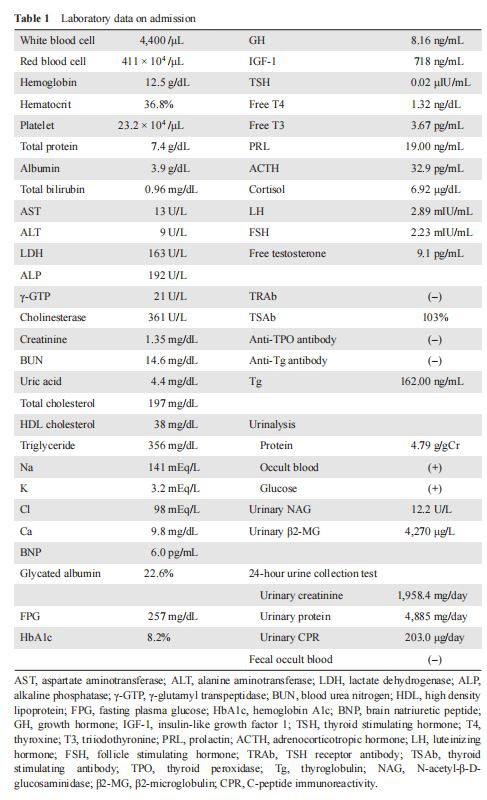
Semasa kemasukan, dia berjaga-jaga; ketinggian, 187 cm; berat, 88 kg; nadi, 63 denyutan seminit; dan tekanan darah, 117/83 mmHg. Dia telah ditetapkan metformin [500 mg semel in die (sid)], glimepiride (0.5 mg sid), valsartan (160 mg sid), amlodipine (10 mg sid) dan carvedilol (20 mg sid).
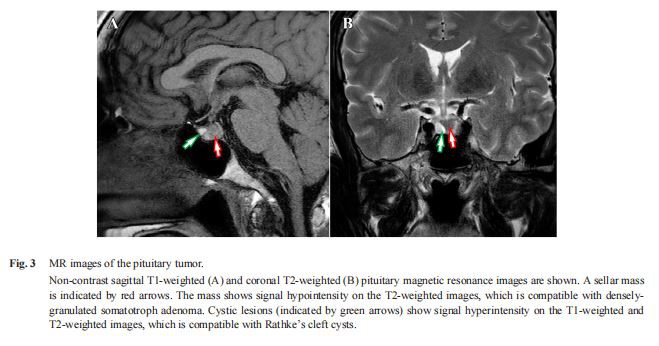
Data makmal mengenai kemasukan ditunjukkan dalam Jadual 1. Diagnosis akromegali disahkan oleh ciri klinikalnya seperti berikut: (i) tahap faktor pertumbuhan 1 (IGF-1) serum insulin ialah 718 ng/mL (normal julat rujukan: 87 hingga 245 ng/mL); (ii) paras GH serum telah dinaikkan pada garis dasar (8.16 ng/mL) dan tidak ditindas dengan sewajarnya (nadir: 6.72 ng/mL) semasa ujian toleransi glukosa oral 75 g; (iii) dan MRI pituitari mendedahkan jisim bintang 9 mm diameter [13]. Jisim menunjukkan keamatan isyarat yang rendah pada imej berwajaran T{14}} dan mempunyai lesi hiperintensis yang menunjukkan sista celah Rathke (Gamb. 3). Radiografi buku lali menunjukkan ketebalan pad tumit (23 mm), yang konsisten dengan diagnosis akromegali.
Data endokrin juga menunjukkan hiperprolaktinemia, hipertiroidisme subklinikal, dan paras tiroglobulin (Tg) serum yang tinggi (Jadual 1). Reseptor anti-TSH, anti-tiroid peroksidase (TPO), dan antibodi anti-Tg adalah negatif. Ultrasonografi tiroid mendedahkan kelenjar tiroid yang diperbesarkan, manakala technetium-99m pertechnetate thyroid scintigraphy menunjukkan penyerapan yang meresap ditindas dalam kelenjar tiroid (0.3 peratus ), mencadangkan tiroiditis yang merosakkan. Tindak balas TSH dan prolaktin (PRL) kepada hormon pelepas thyrotropin (TRH) intravena telah tumpul, manakala tindak balas gonadotropin yang dirangsang hormon pelepas kortikotropin (CRH) dan kortisol dan tindak balas gonadotropin yang dirangsang hormon luteinizing (LHRH) adalah normal.
Data buah pinggang mendedahkan bahawa UPCR dan eGFR masing-masing adalah 4.79 g/GCR dan 43 mL/min/1.73 m2. Imbasan tomografi berkira (CT) abdomen menunjukkan pertumbuhan sista buah pinggang serta dua halabuah pinggangbatu(Gamb. 2C, 2D). Anggaran TKV ialah 1,180 mL. Angiografi resonans magnetik (MRA) otak menunjukkan pelebaran aneurisma fusiform segmen A2 proksimal arteri serebral dan basilar anterior kiri. Ekokardiografi mendedahkan hipertrofi ventrikel kiri tanpa keabnormalan injap yang jelas.

Tiga bulan selepas kemasukan, pembedahan transsphenoidal untuk tumor pituitari dilakukan. Tumor itu secara intraoperatif didapati berwarna putih. Di samping itu, lesi sista dalam tumor pituitari mengandungi cecair mukus yang kurang berwarna dan putih dengan lapisan epitelium bersilia nipis, yang mencadangkan sista sumbing Rathke apabila dipertimbangkan dengan penemuan MRI [14]. Pemeriksaan patologi tumor mendedahkan sel-sel seperti lembaran dengan nukleus bujur dan sitoplasma asidofilik atau amfofilik, yang konsisten dengan adenoma pituitari (Rajah 4A, 4B). Imunostaining untuk GH dan PRL adalah positif (Rajah 4C, 4D) dan imuno-histokimia anti-Cytokeratin (CAM 5.2) menunjukkan terutamanya corak perinuklear filamen keratin, menunjukkan ciri-ciri struktur yang serupa dengan adenoma somatotroph berbutir padat (Rajah 4E) , selaras dengan corak isyarat hipointense pada imej MRI berwajaran T2-(Gamb. 3B) [15, 16]. Indeks pelabelan Ki{17}} adalah kurang daripada 5 peratus (Gamb. 4F). Tahap serum GH dan IGF{{20}} selepas pembedahan telah dinormalisasi (masing-masing 0.92 ng/mL dan 170 ng/mL), menunjukkan kejayaan pembedahan pembedahan adenoma pituitari yang menghasilkan GH. Tiga bulan selepas pembedahan, tahap HbA1c dan UPCR telah menurun dengan ketara (masing-masing 5.7 peratus dan 1.09 g/GCR), tetapi eGFR tidak berubah (34 mL/min/ 1.73 m2 ) (Rajah 1).
Perbincangan
Kami melaporkan kes akromegali yang sangat jarang berlaku bersamaan dengan diabetes mellitus dan PKD. Dalam kes ini, pesakit menunjukkan perkembangan albuminuria yang agak awal dan perkembangan pesat proteinuria yang terang-terangan dan kerosakan buah pinggang, yang sebahagiannya diperbaiki dengan pembedahan pembedahan adenoma pituitari yang menghasilkan GH. Untuk pengetahuan kami, laporan kes pertama akromegali yang dikaitkan dengan ADPKD telah dilaporkan pada tahun 2002 [8]; empat kes lain telah dilaporkan sejak itu [9-12] dan semua individu yang terjejas adalah perempuan (Jadual 2). Kes sekarang menunjukkan bahawa gabungan penyakit ini juga boleh berlaku pada lelaki. Ruggenenti et al. secara ringkas menyebut pesakit ADPKD dengan adenoma pituitari yang telah menjalani rawatan berterusan dengan oktreotida analog somatostatin selama 2 tahun untuk mengawal rembesan GH [9]. Data terperinci mengenai fungsi buah pinggang dan jumlah buah pinggang tidak tersedia dalam semua lima kes. Dalam laporan ini, kami menerangkan secara terperinci perubahan buah pinggang jangka panjang dalam kes dengan akromegali yang disertai dengan diabetes mellitus dan PKD yang menonjolkan keperluan kewaspadaan klinikal untuk akromegali dan PKD dalam kes diabetes mellitus yang luar biasa. Di samping itu, kes ini memberikan petunjuk kepada hubungan patologi antara GH yang berlebihan danbuah pinggangpenyakit, bukan sahaja melalui laluan terus tetapi juga melalui laluan tidak langsung seperti nefropati diabetik.
Diagnosis tertunda akromegali kekal sebagai isu klinikal [3]. Dalam kes ini, akromegali yang mendasari mungkin telah menjejaskan kawalan glisemiknya, kerana peningkatan diperhatikan selepas pembedahan. Tambahan pula, diabetes mellitus yang tidak bergantung kepada insulin yang refraktori boleh membawa kepada syak wasangka akromegali yang belum teruji dalam tetapan klinikal [3].

Akromegali yang tidak didiagnosis boleh menjejaskan kerosakan buah pinggang secara tidak langsung melalui status kawalan glisemik yang lebih teruk; peningkatan HbA1c dalam kes ini nampaknya menjejaskan tahap UPCR pesakit. Terdapat bukti terkumpul bahawa paksi GH/IGF-1 memainkan peranan penting dalam pembangunan awalkencing manisbuah pinggangpenyakit[17, 18]. Malah, IGF-1 mendorong percambahan sel mesangial serta pengeluaran matriks mesangial [19] dan nampaknya melindungi sel mesangial daripada kerosakan DNA yang disebabkan oleh hiperglisemia [20]. Oleh itu, GH terlibat dalam hipertrofi glomerular melalui IGF-1, walaupun beberapa kesan GH pada sklerosis glomerular adalah bebas daripada IGF-1 [21]. Di samping itu, baru-baru ini menunjukkan bahawa GH secara langsung meningkatkan tahap spesies oksigen reaktif dan mendorong penyusunan semula sitoskeleton aktin dalam podosit glomerular melalui reseptor GH berfungsi yang dinyatakan pada sel-sel ini [22]. Ini mungkin menyebabkan apoptosis dan disfungsi podosit glomerular [23, 24], kejadian awal dalam nefropati diabetik.
Menariknya, perkembangan albuminuria yang agak awal ditemui selepas diagnosis pesakit diabetes mellitus dalam kes ini. Lebih-lebih lagi, dia mengalami proteinuria yang berterusan walaupun di bawah status kawalan glisemik yang boleh diterima. Selepas susulan klinikal di bawah andaian nefropati diabetik, PKD didapati menjadi punca lain proteinuria dan kerosakan buah pinggangnya, berdasarkan ultrasonografi abdomen dan penemuan MRI. Walaupun kes kami tidak mempunyai firmakeluargasejarah PKD, bapanya meninggal dunia akibat pecah aneurisme aorta; kajian terdahulu mendapati bahawa sejarah keluarga tidak hadir dalam 20 hingga 40 peratus pesakit ADPKD di mana diagnosis ADPKD ditubuhkan berdasarkan kajian pengimejan [6]. Dalam konteks ini, ujian pengimejan buah pinggang seperti ultrasonografi, MRI, dan CT adalah wajar dalam kes diabetes yang menunjukkan perkembangan awal albuminuria dan perkembangan yang tidak dijangka kepada proteinuria dan disfungsi buah pinggang untuk memastikan diagnosis segera PKD.
Telah dipastikan bahawa pendedahan berpanjangan kepada GH dan IGF{0}} hipersekresi boleh dikaitkan dengan perubahan morfologi dalam buah pinggang dan patogenesis PKD [25]. Pada tikus transgenik untuk GH manusia, perubahan buah pinggang yang teruk termasuk pelebaran sistik besar-besaran tubul telah diperhatikan [26]. Dalam buah pinggang model tetikus PKD, ekspresi mRNA IGF-1 telah meningkat dengan perkembangan lesi sista [27]. Begitu juga, tahap IGF-1 buah pinggang berkorelasi positif dengan perkembangan penyakit dalam model tikus PKD, manakala penurunan tahap IGF-1 buah pinggang akibat diet mengakibatkan pengurangan saiz buah pinggang dan sista [28] . Selain itu, kekurangan polycystin-1 dalam talian sel sista PKD1 telah dikaitkan dengan peningkatan sensitiviti kepada IGF-1 serta kesan permisif adenosin monofosfat (cAMP) kitaran pada pertumbuhan sel [29]. Kajian lain menunjukkan bahawa transduser isyarat GH dan pengaktif paksi transkripsi (STAT) telah diaktifkan secara tidak normal dalam tikus kekurangan PKD1-, yang membawa kepada percambahan yang dipertingkatkan [30]. Memandangkan fakta bahawa STAT3 yang diaktifkan didapati sangat dinyatakan dalam sel epitelium tiub daribuah pinggangpesakit dengan sista buah pinggang mudah [31], kemungkinan implikasi pengaktifan STAT3 oleh GH dalam perkembangan sista buah pinggang telah dicadangkan [32]. Bukti ini menunjukkan bahawa GH dan IGF-1 mungkin memainkan peranan patogenik dalam PKD.
Dalam konteks ini, TKV dalam kes ini, yang diukur dengan stereologi menggunakan MRI abdomen atau CT, harus dibincangkan. Berdasarkan model regresi kesan campuran membujur yang diterangkan oleh Irazabal et al. [33], pesakit kami dikelaskan sebagai Kelas 1B [TKV terlaras ketinggiannya (HtTKV) pada usia 50 tahun: 576.5 mL/m], di mana anggaran kadar pertumbuhan HtTKV ialah 1.5 hingga 3 peratus setiap tahun. Sebaliknya, HtTKV beliau semasa kemasukan ialah 631.0 mL/m, dan kadar pertumbuhan mencapai 9 peratus dalam tempoh satu tahun. Walaupun susulan TKV selepas pembedahan akan membantu untuk mengesahkan penglibatan akromegali dalam perkembangan PKD,buah pinggangujian pengimejan tidak dapat diperoleh kerana pemberhentian lawatan biasa pesakit. Memandangkan peningkatan pesat HtTKV yang berpotensi, penyiasatan lanjut mengenai perkaitan akromegali dengan perkembangan PKD adalah wajar, walaupun kejadian mereka bersama-sama secara klinikal sangat jarang berlaku.
Akhir sekali, kemungkinan penggunaan tolvaptan dalam kes ini harus disebut. Tolvaptan ialah antagonis reseptor vasopressin V2, yang telah diluluskan untuk ADPKD pada tahun 2014 di Jepun. Oleh kerana kajian terdahulu menunjukkan tolvaptan mengurangkan kadar tahunan pertumbuhan TKV dan memperlahankan kadar tahunan penurunan eGFR pada pesakit ADPKD peringkat kemudian [34, 35], ia boleh dianggap sebagai pilihan rawatan masa depan dalam kes sedemikian.
Kesimpulannya, kami melaporkan kes akromegali yang disertai dengan diabetes mellitus dan PKD. Proteinuria dan fungsi buah pinggang yang semakin teruk mencadangkan aspek biasa rembesan GH yang berlebihan sebagai faktor mempercepatkan kedua-dua nefropati diabetik dan PKD. Walaupun akromegali dan PKD yang wujud bersama jarang berlaku secara klinikal, kewaspadaan untuk diagnosis awal akromegali dan juga PKD adalah sesuai pada pesakit yang menghidap diabetes yang luar biasa atau pemburukan proteinuria yang tidak dijangka danbuah pinggangdisfungsi.

Rujukan
1 Melmed S (2006) Kemajuan perubatan: akromegali. N Engl J Med 355: 2558–2573.
2. Melmed S (2009) Patogenesis dan rawatan akromegali. J Clin Invest 119: 3189–3202.
3. Gadelha MR, Kasuki L, Lim DST, Fleseriu M (2019) Komplikasi sistemik akromegali dan kesan landskap rawatan semasa: kemas kini. Endokr Wahyu 40: 268–332.
4. Wilson PD (2004) Penyakit buah pinggang polikistik. N Engl J Med 350: 151–162.
5. Horie S, Mochizuki T, Muto S, Hanaoka K, Fukushima Y, et al. (2016) Garis panduan amalan klinikal berasaskan bukti untuk penyakit buah pinggang polikistik 2014. Clin Exp Nephrol 20: 493–509.
6. Pei Y (2006) Pendekatan diagnostik dalam penyakit buah pinggang polikistik dominan autosomal. Clin J Am Soc Nephrol 1: 1108–1114.
7. Tokiwa S, Muto S, China T, Horie S (2011) Hubungan antara isipadu buah pinggang dan fungsi buah pinggang dalam penyakit buah pinggang polikistik dominan autosomal. Clin Exp Nephrol15: 539–545.
8. Fajfr R, Müller B, Diem P (2002) Hypophyseal incidentaloma dalam pesakit dengan penyakit buah pinggang polikistik dominan autosomal. Praxis (Bern 1994) 91: 1123–1126 (Dalam bahasa Jerman).
9. Ruggenenti P, Remuzzi A, Ondei P, Fasolini G, Antiga L, et al. (2005) Keselamatan dan keberkesanan rawatan somatostatin bertindak panjang dalam penyakit buah pinggang polikistik yang dominan autosomal. Int Buah Pinggang 68: 206–216.
10. Kannabiran M, Singh V, Grewal S (2006) Akromegali yang membentangkan sebagai gangguan psikotik dalam keluarga dengan penyakit buah pinggang polikistik dominan autosomal keluarga. Ger J Psikiatri 9: 136–138.
11. Syro LV, Sundsbak JL, Scheithauer BW, Toledo RA, Camargo M, et al. (2012) Somatotroph pituitari adenoma dengan acromegali dan penyakit buah pinggang polikistik dominan autosomal: polimorfisme SSTR5 dan mutasi PKD1. Pituitari 15: 342–349.
12. Mangaraj S, Patro D, Choudhury AK, Baliarsinha AK (2019) Kes jarang berlaku bagi penyakit buah pinggang polikistik dominan acromegali dan autosomal: laporan kes dan kajian ringkas literatur. Wakil Kes AACE Clin 5: e302–e306.
13. Kumpulan kajian disfungsi hipotalamus-pituitari Kementerian Kesihatan Buruh dan Kebajikan (2019) Diagnosis dan rawatan disfungsi hipotalamus-pituitari. Nihon Naibunpi Gakkai Zasshi 95 Suppl: 1–60 (Dalam Jepun).
14. Nishio S, Fujiwara S, Morioka T, Fukui M (1995) Sista sumbing Rathke dalam adenoma pituitari yang menghasilkan hormon pertumbuhan. Br J Neurosurg 9: 51–55.
15. Heck A, Emblem KE, Casar-Borota O, Bollerslev J, Ringstad G (2016) Analisis kuantitatif MRI berwajaran T2-sebagai penanda berpotensi untuk tindak balas kepada analog somatostatin dalam akromegali yang baru didiagnosis. Endokrin 52: 333–343.
16. Akirov A, Asa SL, Amer L, Shimon I, Ezzat S (2019) Spektrum klinikopatologi akromegali. J Clin Med 8: 1962.
17. Flyvbjerg A (2000) Patofisiologi Putatif peranan faktor pertumbuhan dan sitokin dalam penyakit buah pinggang diabetik eksperimen. Diabetologia 43: 1205–1223.
18. Vasylyeva TL, Ferry RJ Jr (2007) Peranan novel paksi IGF-IGFBP dalam etiopatofisiologi nefropati diabetik. Diabetes Res Clin Pract 76: 177–186.
19. Feld SM, Hirschberg R, Artishevsky A, Nast C, Adler SG (1995) Faktor pertumbuhan seperti insulin I mendorong percambahan mesangial dan meningkatkan mRNA dan rembesan kolagen. Int Buah Pinggang 48: 45–51.
20. Yang S, Chintapalli J, Sodagum L, Baskin S, Malhotra A, et al. (2005) IGF-1R yang diaktifkan menghalang kerosakan DNA akibat hiperglikemia dan menggalakkan pembaikan DNA melalui penggabungan semula homolog. Am J Physiol Fisiol Renal 289: F1144–F1152.
21. Baud L, Fouqueray B, Bellocq A, Doublier S, Dumoulin A (1999) Hormon pertumbuhan dan somatostatin dalam kecederaan glomerular. J Nefrol 12: 18–23.
22. Reddy GR, Pushpanathan MJ, Ransom RF, Holzman LB, Brosius FC, et al. (2007) Pengenalpastian podosit glomerular sebagai sasaran untuk tindakan hormon pertumbuhan. Endokrinologi 148: 2045–2055.
23. Pagtalunan ME, Miller PL, Jumping-Eagle S, Nelson RG, Myers BD, et al. (1997) Kehilangan podocyte dan kecederaan glomerular progresif dalam diabetes jenis II. J Clin Invest 99: 342–348.
24. Kumar PA, Kotlyarevska K, Dejkhmaron P, Reddy GR, Lu C, et al. (2010) Ekspresi yang bergantung kepada hormon pertumbuhan (GH) daripada transkrip antisense semula jadi mendorong jari zink E-box-binding homeobox 2 (ZEB2) dalam podosit glomerular: tindakan baru GH dengan implikasi untuk patogenesis nefropati diabetik. J Biol Chem 285: 31148–31156.
25. Kamenický P, Mazziotti G, Lombès M, Giustina A, Chanson P, et al. (2014) Hormon pertumbuhan, faktor pertumbuhan seperti insulin-1 dan buah pinggang: implikasi patofisiologi dan klinikal. Endokr Wahyu 35: 234–281.
26. Wanke R, Hermanns W, Folger S, Wolf E, Brem G (1991) Pertumbuhan dipercepatkan dan lesi visceral dalam tikus transgenik yang menyatakan gen asing keluarga hormon pertumbuhan: gambaran keseluruhan. Pediatr Nephrol 5: 513–521.
27. Nakamura T, Ebihara I, Nagaoka I, Tomino Y, Nagao S, et al. (1993) Ekspresi gen faktor pertumbuhan dalam buah pinggang penyakit buah pinggang polikistik murine. J Am Soc Nephrol 3: 1378–1386.
28. Aukema HM, Housini I (2001) Kesan protein soya diet terhadap penyakit dan IGF-I pada lelaki dan perempuan Han: tikus SPRD-Cy. Int Buah Pinggang 59: 52–61.
29. Parker E, Newby LJ, Sharpe CC, Rossetti S, Streets AJ, et al. (2007) Hiperproliferasi sel sista PKD1 disebabkan oleh pengaktifan faktor pertumbuhan seperti insulin-1 sistem isyarat Ras/Raf. Int Buah Pinggang 72: 157–165.
30. Fragiadaki M, Lannoy M, Themanns M, Maurer B, Leonhard WN, et al. (2017) STAT5 memacu percambahan abnormal dalam penyakit buah pinggang polikistik dominan autosomal. Int Buah Pinggang 91: 575–586.
31. Liu M, Xu YF, Feng Y, Zhai W, Che JP, et al. (2013) Pengaktifan Androgen-STAT3 boleh menyumbang kepada perbezaan jantina dalam sista buah pinggang manusia. Int J Clin Exp Pathol 6: 686–694.
32. Yamamoto M, Matsumoto R, Fukuoka H, Iguchi G, Takahashi M, et al. (2016) Kelaziman sista renal mudah dalam akromegali. Intern Med 55: 1685–1690.
33. Irazabal MV, Rangel LJ, Bergstralh EJ, Osborn SL, Harmon AJ, et al. (2015) Klasifikasi pengimejan penyakit buah pinggang polikistik dominan autosomal: model mudah untuk memilih pesakit untuk ujian klinikal. J Am Soc Nephrol 26: 160–172.
34. Torres VE, Chapman AB, Devuyst O, Gansevoort RT, Perrone RD, et al. (2017) Tolvaptan dalam penyakit buah pinggang polikistik dominan autosomal peringkat kemudian. N Engl J Med 377: 1930–1942.
35. Oguro M, Kogure Y, Hoshino J, Ubara Y, Mizuno H, et al. (2018) Tolvaptan pada pesakit Jepun dengan penyakit buah pinggang polikistik dominan autosomal peringkat kemudian. J Nephrol 31: 961–966.
