Biomaterial Antioksidan Semulajadi Baru Dari Daun Cinnamomum Osmophloeum Kanehira Menindas Melanogenesis Dan Melindungi Daripada Kerosakan DNA
Mar 21, 2022
Kenalan: ali.ma@wecistanche.com
Yung-Shu Ho 1, Jane-Yii Wu 1,* dan Chi-Yue Chang 2
Abstrak:Cinnamomoum osmophloeum Kanehira (COK) ialah spesies pokok asli di Taiwan. Komposisi kimia,antioksidanaktiviti, cendawantyrosinaseperencatan, penindasan sintesis melanin, dan perlindungan terhadap kerosakan DNA hidrosol daripada daun COK melalui penyulingan wap telah diperiksa. Kami melakukan 1,1-difenil-2-penyingkiran radikal picrylhydrazyl, pengkelat ion logam, mengurangkan kuasa, dan ujian kapasiti antioksida setara Trolox (TEAC) dan menentukan korelasi antara jumlah kandungan fenolik dan aktiviti antioksidan. Penemuan menunjukkan bahawa sifat anti-oksidatif COK hidrosol berkait rapat dengan kandungan fenolnya. Selain itu, juzuk utama hidrosol, iaitu sinamaldehid dan benzaldehid, mempunyai kesan anti-tirosinase yang bergantung kepada dos terhadap kedua-dua aktiviti monophenolase dan diphenolase. Analisis GC-MS mendedahkan bahawa komponen bioaktif utama hidrosol ialah trans-cinnamaldehyde(87.7 peratus ), benzaldehid (7.0 peratus ), dan sinamil asetat (5.3 peratus ). Selain itu, kami mendapati bahawa hidrosol dengan kehadiran benzaldehid lebih kuat daripada sinamaldehid tulen, dan meningkatkantyrosinaseaktiviti perencatan hidrosol. Dalam analisis kinetik, plot dan replot Lineweaver–Burk menunjukkan bahawa hidrosol COK ialah perencat jenis campuran. Selain itu, kami mendapati bahawa dos COK hidrosol yang sangat rendah menindas sintesis yang disebabkan oleh hormon perangsang-melanosit bagi faktor transkripsi berkaitan mikroftalmia, yang membawa kepada penurunan sintesis melanin dalam sel B16-F10melanoma. Keputusan ini menunjukkan bahawa penghasilan hidrosol daripada daun COK menggunakan penyulingan wap boleh menyediakan sumber yang selamat dan mujarab.kulit-pemutihanejen untuk aplikasi kosmetikdan farmaseutikal, denganantioksidan, anti-tirosinase, anti-melanogenesis, dan aktiviti pelindung DNA.
Kata kunci: antioksidanaktiviti; Cinnamomoum osmophloeum; hidrosol;tyrosinaseaktiviti menghalang;pemutihan; Kesan perlindungan kerosakan DNA

Klik untukCistanchebatang dan produk untuk memutihkan kulit
1. Pengenalan
Gangguan kulit manusia seperti lentigo, bintik-bintik umur, melasma, dan melanoma malignan telah dikaitkan dengan pembentukan dan pengumpulan melanin [1]. Perencatan tyrosinases dan melanogenesis dapat memperbaiki gangguan dermatologi dan sindrom hiperpigmentasi. Di samping itu, pasaran global untuk agen pemutihan kulit dan produk kosmetik telah berkembang baru-baru ini kerana warna kulit lebih cerah digemari oleh ramai individu berkulit gelap [2]. Oleh itu, berkesan dan selamattyrosinasedan perencat sintesis melanin dianggap penting untuk pencegahan penyakit pigmentasi dan isu kesihatan manusia yang berkaitan dengan melanin yang lain [3,4]. Selain itu, bahan toksik alam sekitar menyebabkan pelbagai tekanan oksidatif kepada manusia, dan boleh menghasilkan spesies nitrogen reaktif atau spesies reaktifoksigen (ROS) [5]. Radikal bebas dan ROS yang berlebihan dikaitkan dengan laluan isyarat keradangan, yang akhirnya membawa kepada kerosakan selular, penuaan, gangguan saraf, diabetes, aterosklerosis, radang, penyakit kardiovaskular, kanser, dan melanogenesis [6,7]. Beberapa kajian mencadangkan bahawaantioksidanboleh menghalang kerosakan tekanan oksidatif dengan bertindak sebagai penghapus radikal bebas atau ROSscavengers [7,8]. Selain itu, kedua-dua perencat penjanaan ROS dan pemulung ROS boleh mengurangkan pengeluaran pigmen melanin [9]. Secara khusus,tyrosinaseadalah enzim utama yang memangkinkan langkah pengehad kadar pada dua langkah pertama semasa proses sintesis melanin [10], dan pengawalan menurun tyrosinaseis merupakan matlamat kritikal untuk pencegahan penyakit kulit dan pengeluaranpemutihan kulitagen [11].Oleh itu, pembangunan antioksidan semula jadi yang berkesan menghalang tyrosinase untuk pencegahan atau rawatan hiperpigmentasi kulit yang tidak diingini dan perlindungan terhadap kerosakan DNA adalah penting.
Cinnamomum osmophloeum Kanehira (COK) ialah spesies kayu manis asli Taiwan dengan banyak kegunaan sebagai ubat herba Cina. Sebatian aktif minyak pati COK menunjukkan potensi yang sangat baik sebagai antibakteria farmakologi [12]. Walaupun kajian terdahulu tentang ekstrak alkohol daun COK menunjukkan aktiviti anti-tirosinase, hampir semua kajian ini tertumpu kepada etanolekstrak atau minyak pati daripada COK. Selain itu, tiada kajian kuantitatif dan sistematik telah dilaporkanantioksidanharta benda,tyrosinaseaktiviti perencatan dan penindasan sintesis melanin oleh ekstrak air (hidrosol) daun COK. Oleh itu, kajian ini dijalankan untuk menyiasat kesan hidrosol COK terhadap tekanan oksidatif dan melanogenesis dalam sel melanoma B16F10 dan melindungi daripada kerosakan DNA. Kajian ini adalah laporan terperinci pertama tentang komposisi kimia danantioksidan, perencatan tyrosinase, penindasan melanogenesis, dan aktiviti perlindungan kerosakan DNA hidrosoldaripada daun COK.

2. Bahan-bahan dan cara-cara
2.1. Bahan Kimia dan Antibodi
cendawantyrosinase, butylated hydroxytoluene (BHT), -tocopherol, 6-hydroxy-2,5,7,8-tetramethylcroman-2-asid karboksilik (Trolox), asid trichloroacetic (TCA), gallic asid, potassiumferricyanide, ferric chloride, ferrous chloride, ferrozine, 1,1-diphenyl-2-picrylhydrazyl (DPPH),2,20-azino-bis-3-ethylbenzthiazoline{{14} } asid sulfonik (ABTS), reagen Folin–Ciocalteu, L-tirosin dan L-3,4-dihydroxyphenylalanine (L-DOPA) diperoleh daripada Merck Co. (Darmstadt, Jerman). Semua bahan kimia dan pelarut yang digunakan dalam kajian adalah gred analitik atau kromatografi cecair berprestasi tinggi. Antibodi terhadap faktor transkripsi berkaitan mikroftalmia (MITF) dan -aktin diperoleh daripada Teknologi Isyarat Sel (Danvers, MA, Amerika Syarikat) dan Sigma Chemical Co. (St. Louis, Amerika Syarikat), masing-masing.
2.2. Penyediaan Hidrosol: Pengekstrakan daripada Daun COK Menggunakan Penyulingan Stim
Daun daripada pokok COK berusia 13-tahun di Taiwan (No.186, Yongping Road, Zhongliao Township, Nantou County, Taiwan) telah dikeringkan dengan udara. Menggunakan pengisar keluli tahan karat, daun kemudiannya dikisar menjadi serbuk halus (kurang daripada <10 mesh)="" dan="" kemudian="" disimpan="" pada="" suhu="" bilik.="" seterusnya,="" 3.5="" kg="" serbuk="" daun="" cok="" kering="" diekstrak="" menggunakan="" penyulingan="" wap="" selama="" 4="" jam.="" proses="" ini="" diulang="" empat="" kali.="" menggunakan="" vakum,="" ekstrak="" ditapis="" dan="" kemudian,="" menggunakan="" penyejat="" berputar,="" ekstrak="" kering="" telah="" diperolehi="" (rajah="" 1).="" ekstrak="" akhirnya="" disejat="" untuk="" mendapatkan="" berat="">

2.3. Kromatografi Gas/Spektrometri Jisim (GC/MS) Analisis Hidrosol
Instrumen Thermo-GC/MS dengan THERMO WaxMS berpaut silang 5 peratus fenil- 95 peratus lajur kapilari metilpolysiloxane (60 m × 0.25 mm id, ketebalan filem {{1 0}}.25 µm) telah digunakan dengan helium sebagai gas pembawa pada kadar aliran malar 1.0 mL/min. Lajur dikekalkan pada 200 ◦C selama 5 minit selepas suntikan dan kemudian dipanaskan pada 5 ◦C/min hingga 260 ◦C. Minyak pati tulen (1.0 mL) disuntik dengan nisbah perpecahan 1:100. Suhu penyuntik, talian pemindahan dan punca ion ialah 250 ◦C, 250 ◦C, dan 200 ◦C, masing-masing. Pengesanan MS dilakukan dalam mod hentaman elektron pada 70 tenaga eVionisasi dan arus pengionan 60 µA; instrumen itu dikendalikan dalam mod pemerolehan imbasan penuh dalam julat 50–350 amu. Sebatian dikenal pasti dengan membandingkan masa pengekalan dan indeks puncak kromatografi dengan piawai rujukan tulen, yang disuntik di bawah keadaan yang sama. Corak pemecahan MS dibandingkan dengan sebatian tulen, dan pangkalan data spektrum massa telah dicari menggunakan pangkalan data MSspectral Institut Piawaian dan Teknologi Kebangsaan (NIST) [13].

2.4.Jumlah Kandungan Fenolik
Jumlah kandungan fenolik (TPC) ekstrak ditentukan menggunakan Folin-Ciocalteu assayas yang diterangkan sebelum ini [14]. Secara ringkas, sampel hidrosol (100 µL) dicampur dengan 100 µL aliquot reagen Folin–Ciocalteu (10-pencairan kali ganda) dan 10 µL aliquot natrium karbonat (10 peratus , b/v). Selepas disimpan selama 30 minit, penyerapan diukur pada 735 nm. TPC dinyatakan sebagai kesetaraan asid gallic (GAE) dalam mg setiap 100 g bahan segar.
2.5. Ujian Penghapusan Radikal Bebas DPPH
Seperti yang diterangkan sebelum ini, menggunakan ujian DPPH, aktiviti penghapusan radikal hidrosol telah ditentukan [15], dengan pengubahsuaian. Secara ringkas, pelbagai pencairan sampel hidrosol (75 µL dalam tiga kali ganda) telah ditambah kepada 150 µL aliquot DPPH (0.02 g/100 mL) dan penyerapan diukur pada 517 nm selepas 30 minit. BHT digunakan sebagai kawalan positif (0.5 mg/mL etanol). Aktiviti pemusnahan radikal dinyatakan sebagai nisbah perencatan ( peratus ) menggunakan persamaan berikut:
Nisbah perencatan( peratus )=[1 − (A/B)] × 100 peratus
di mana A ialah penyerapan sampel hidrosol dan B ialah penyerapan kosong.
2.6. Kepekatan Perencatan Pecahan
Ujian kepekatan perencatan pecahan (FIC) telah dilakukan seperti yang diterangkan sebelum ini [16], dengan pengubahsuaian. Secara ringkas, FeSO4 (20 µL; 2 mM) dicampur dengan pencairan hidrosolsampel yang berbeza (200 µL). Selepas menambah ferrozine (40 µL; 5 mM), tindak balas dibenarkan untuk diteruskan selama 10 minit dan kemudian penyerapan diukur pada 562 nm. Tambahan pula, 0.5 mg/mL etilena diamine tetraacetic acid (EDTA) digunakan sebagai kawalan positif. Perencatan peratusan pembentukan kompleks ferrozine-Fe2 ditambah dikira menggunakan formula berikut:
Kesan pengkelat logam ( peratus )=[1 − (A/B)] × 100 peratus
di mana A ialah penyerapan sampel hidrosol dan B ialah penyerapan kosong.
2.7. Mengurangkan Ujian Kuasa
Kuasa pengurangan hidrosol COK ditentukan dengan memantau pengurangan Fe3 tambah kepadaFe2 tambah seperti yang diterangkan sebelum ini [17], dengan pengubahsuaian. Secara ringkas, kepada 50 µL pencairan hidrosol, 50-µLaliquots penimbal fosfat (pH 6.6, 200 mM) dan 50-µL aliquot kalium ferricyanide (1 peratus , w/v) adalah tambah. Selepas pengeraman pada 50 ◦C selama 20 minit, 50 µL TCA (10 peratus, w/v) telah ditambah; dan campuran telah diempar pada 9,{15}} rpm selama 3 minit. Akhir sekali, 50 µL supernatan dicampur dengan 50 µL air suling dan 50 µL ferik klorida dalam air (0.1 peratus, w/v), dan penyerapan diukur pada 700 nm melawan kosong selepas 10 minit masa tindak balas. Kawalan positif yang digunakan ialah butylated hydroxytoluene (BHT) dan -tokoferol.
2.8. Ujian Keupayaan Antioksidan Setara Trolox (TEAC).
Antioksidanaktiviti hidrosol COK dinilai mengikut kaedah yang diterangkan sebelum ini [15,18], dengan pengubahsuaian. Secara ringkasnya, larutan kation radikal ABTS pekat (ABTS• tambah) telah dicairkan dalam salin penimbal fosfat (pH 7.4) kepada penyerapan akhir sebanyak 0.80 ± 0.05 pada 734 nm. Selepas mencampurkan (0.02 mL) sampel dengan 1 mL ABTS tambah larutan, terdapat pengurangan dalam penyerapan pada 734 nm selepas 5 min. Trolox digunakan sebagai piawai, dan aktiviti hidrosol dinyatakan sebagai TEAC dengan memplot lengkung Troloxcalibration. Nilai TEAC setara molar bagi sampel hidrosol telah dikira mengikut pengurangan dalam penyerapan larutan Trolox. BHT dan -tokoferol digunakan sebagai kawalan positif.
2.9. Kesan Hidrosol pada Perencatan Tirosinase Cendawan
cendawantyrosinaseaktiviti diukur menggunakan analisis spektrofotometri seperti yang dinyatakan sebelum ini, dengan pengubahsuaian [19]. Secara ringkas, 20 µL L-tirosin atau 20 µL L-DOPA dalam PBS (pH 6.8; 80 µL) dan 80 µL PBS dengan atau tanpa hidrosol ujian telah ditambah ke dalam 96-plat mikro telaga, dan kemudian 20 µL cendawan tirosinase (100 U/ mL) telah ditambah. Selepas pencampuran dan pengeraman pada 37 ◦C selama 20 minit, dopachromeproduction (atau penggunaan) dalam campuran tindak balas ditentukan pada penyerapan 475 nm. Asid kojic, yang menghalang tyrosinase, digunakan sebagai kawalan positif. Peratusan perencatan tyrosinase dikira seperti berikut:
Perencatan ( peratus ) ≡ {[(A − B) − (C − D)]/(A − B)} × 100 peratus
di mana A menunjukkan penyerapan dengan enzim tanpa ketiadaan sampel hidrosol, B menunjukkan penyerapan tanpa enzim atau sampel hidrosol, C menunjukkan penyerapan dengan enzim, dan hidrosol dan Dindikasikan penyerapan tanpa enzim tetapi dengan hidrosol. Kami juga mengira 50 peratustyrosinasekepekatan perencatan (IC50) sampel seperti yang menghalang aktiviti tyrosinase sebanyak 50 peratus .
2.10. Analisis Kinetik Perencatan Tirosinase Cendawan
Campuran tindak balas mengandungi 20 µL L-tirosin atau L-DOPA (0.25 mg/mL) sebagai substrat, 100 µLof cendawan tyrosinase (20 unit/mL) dalam penimbal natrium fosfat 0.2 M ( pH 6.8) dan 80 µL setiap sampel hidrosol dalam jumlah isipadu 200 µL. Ujian dilakukan pada 25 ◦C, dan kinetik perencatan setiap sampel hidrosol dengantyrosinasetelah dianalisis menggunakan plot Lineweaver-Burk. Persamaan timbal balik digunakan untuk keseimbangan pantas daripada perencatan bukan kompetitif jenis campuran, seperti yang dinyatakan dalam Persamaan (1) [20]. Nilai Ki untuk sampel hidrosol dianggarkan daripada replot cerun (Persamaan (2)). Nilai Ki untuk hidrosol dikira daripada replot pintasan paksi 1/v (Persamaan (3)),

di mana Vmax ialah halaju maksimum bagityrosinaseaktiviti, Ksis pemalar pemisahan substrat (S) daripada kompleks enzim-substrat (ES), Kiis pemalar pemisahan perencat[I] daripada kompleks perencat enzim dan Kiis pemalar pemisahan perencat daripada enzim-substrat. -kompleks perencat (ESI).
2.11. Kultur Sel dan Ujian Daya Tahan Sel
B16-Sel melanoma F10 (BCRC60031) diperoleh daripada Bioresource Collection and ResearchCenter (BCRC), Taiwan. Sel B16-F10 telah dikultur dalam medium Eagle's diubah suai Dulbecco (Gibco, California, Amerika Syarikat) yang mengandungi 10 peratus FBS pada 37 ◦C dalam 5 peratus CO2. Dengan tripsinisasi, sel dituai. Daya maju sel diukur menggunakan 3-(4,5-dimethyl-thiazol-2-yl)-2,5-diphenyltetrazoliumbromide (MTT) assay seperti yang diterangkan oleh Lee [15 ].
2.12. Kandungan Melanin Selular
Kandungan melanin diukur menggunakan kaedah yang diterangkan oleh Lee. [15]. Secara ringkas, sel B16-F10 dibiakkan dalam 6-plat perigi pada ketumpatan 0.8 × 105sel setiap telaga dan kemudian diinkubasi selama 24 jam. Sel kemudiannya dirawat dengan 100-nM -melanocyte-stimulating hormone ( -MSH), asid kojic (positivecontrol) dan hidrosol pada pelbagai kepekatan selama 24 jam. Selepas mencuci dua kali dengan PBS, sel-sel telah disalurkan dalam penimbal yang mengandungi 100 mM natrium fosfat (pH 6.8), 1 peratus Triton X-100 dan 0.1 mM fenilmetanasulfonil fluorida dan disimpan pada −80 ◦C selama 30 minit. Selepas mengumpul sel, pelet sel telah dibubarkan dalam 1N NaOH yang mengandungi 10 peratus DMSO pada 65 ◦C selama 1 jam. Selepas itu, penyerapan diukur pada 405 nm.
2.13. Penghapusan Barat
Sel-sel telah dilisiskan seperti yang diterangkan dalam Bahagian 2.11 dan tertakluk kepada pembongkaran Barat untuk protein MITF menggunakan antibodi Anti-MITF.
2.14. Ujian Perlindungan DNA
Kerosakan DNA oksidatif ditentukan mengikut penukaran DNA neo plasmid supercoiledpCI pekeliling ke dalam bentuk bulatan bergegar atau lebih teruk menggunakan kaedah yang diterangkan sebelum ini [21,22] dengan sedikit pengubahsuaian. Campuran tindak balas 20 µL mengandungi 2.5 µL supercoiledpCI neo (150 ng/µL), 10 µL larutan tindak balas Fenton yang mengandungi 30 mM hidrogen peroksida, 100-µMferric chloride dan 100 µM asid askorbik dalam penimbal Tris-HCl 20 mM (pH 7.6), dan 5µL hidrosol(0.3325–5.32 mg/mL) atau kuersetin (kawalan positif; 250 µg/mL). Campuran tindak balas diinkubasi pada 37 ◦C selama 30 minit dan bentuk DNA plasmid diasingkan pada 0.7 peratus gel agarose dan diwarnakan menggunakanSafeView™ (Applied Biological Materials (ABM) Inc., Richmond, Kanada).
Untuk separuh kuantitiantioksidanaktiviti ekstrak, kuantiti bentuk supercoiled dan nicked pCI neo dikira menggunakan instrumen AlphaImager Mini (proteinsimple), dan intensiti jalur pada gel agarose dikira menggunakan perisian Gelpro. Sebagai kawalan negatif dan positif, neoplasmid pCI diinkubasi sahaja dan dengan campuran reagen Fenton, masing-masing. Data dinyatakan sebagai kuantiti DNA bergelung besar berbanding dengan itu (100 peratus ) dalam kawalan negatif. Aktiviti perlindungan ekstrak dikira daripada kuantiti DNA plasmid supergegelung dan tersangkut menggunakan persamaan berikut [23]:
Perlindungan supercoiled plasmid( peratus ) =supercoiled form intensitypCI neo DNA band intensity × 100
Perlindungan plasmid tersangkut( peratus ) =keamatan bentuk nickedpCI keamatan jalur DNA neo × 100
2.15. Analisis statistik
Semua data dinyatakan sebagai min ± sisihan piawai (SD). Perbezaan antara rawatan telah dikenalpasti menggunakan ujian-t Pelajar atau ANOVA diikuti dengan ujian Scheffe. Perbezaan dianggap penting apabila p <>
3. Keputusan dan perbincangan
3.1. Pengenalpastian Sebatian Meruap dalam Hidrosol
Kandungan hidrosol dianalisis menggunakan GC/MS. Komponen telah dikenal pasti mengikut masa pengekalan piawai dan kuantiti ditentukan dari kawasan puncak eluen (Rajah 2). Seperti yang digariskan dalam Rajah 2A–D, trans-cinnamaldehyde, benzaldehyde, dan cinnamyl acetate adalah sebatian utama dalam hidrosol COK dan terdapat pada 87.7 peratus , 7.0 peratus dan 5.3 peratus, masing-masing. Eugenol sebelum ini ditemui dalam minyak pati daripada C. verum pada 7.29 peratus [24] tetapi tidak dikesan dalam hidrosol COK sekarang (Rajah 2). Perbezaan dalam proses pengekstrakan dan kaedah ujian boleh menyumbang kepada perbezaan dalam kandungan sinamaldehid minyak pati C. cassia [25].

3.2. Sifat Antioksidan Hidrosol daripada Daun COK
3.2.1. Aktiviti Pemusnahan Radikal DPPH
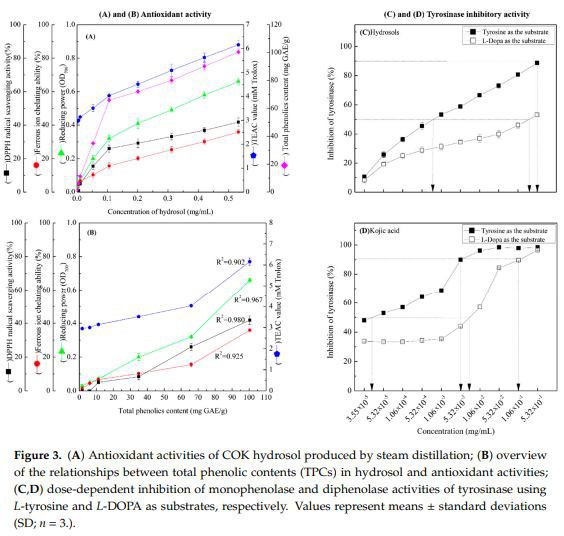
Dalam Rajah 3A, aktiviti penghapusan radikal DPPH hidrosol daripada 1.06×10−2hingga 5.32×10−1 mg/mLadalah antara 5.04 peratus ± 0.96 peratus dan 41.76 peratus ± 2.50 peratus masing-masing. Data ini menunjukkan pemusnahan radikal yang bergantung kepada dos oleh hidrosol COK. Sebagai perbandingan, kawalan positif BHT dan -tocopherol disingkirkan 94.32 peratus ± 0.08 peratus dan 93.82 peratus ± 0.13 peratus daripada radikal reaktif DPPH, masing-masing, pada 0.5 mg/mL. Aktiviti penghapusan radikal COK hidrosol berkemungkinan besar disebabkan oleh cinnamaldehid2 (Rajah ).Banyak kajian menunjukkan bahawa fenolik dan flavonoid menghalang pembentukan radikal DPPH dengan menderma atom hidrogen. Oleh itu, aktiviti penghapusan radikal DPPH spesies Cinnamomum mungkin juga mencerminkan tindakan sebagai penderma hidrogen [26,27].
3.2.2. Khelasi Ion Logam
Kami menilai kapasiti pengikatan Fe2 ditambah hidrosol pada 1.06 × 10−3 dan 5.32 × 10−1 mg/mL, seperti yang ditunjukkan dalam Rajah 3A. Pengkelat logam oleh komponen hidrosol meningkat sedikit dengan kepekatan, tetapi pada 6 mg/mL, hanya mempunyai 37.3 peratus daripada aktiviti pengkelat EDTA (Rajah 3A).
3.2.3. Mengurangkan Kuasa
Seperti yang ditunjukkan dalam Rajah 3A, kuasa pengurangan komponen hidrosol bergantung kepada kepekatan dan lebih tinggi daripada BHT dan -tokoferol (0.22 ± 0.01 dan {{9 }}.33 ± 0.15, masing-masing) pada 0.5 mg/mL. Dalam kajian terdahulu, kuasa pengurangan ekstrak mentah daripada C. osmophloeum ranting dalam pecahan BuOH adalah yang tertinggi di antara semua pecahan dan meningkat secara linear dengan kepekatan [28].antioksidanpotensi berbeza antara sebatian dalam ekstrak, aktiviti antioksidan keseluruhan ekstrak sangat bergantung pada pelarut pengekstrakan. Walau bagaimanapun, kuasa pengurangan (nilai OD {{0}}.7) ekstrak air daripada ranting C. osmophloeum adalah serupa (nilai OD=0.66 ± 0.01) dengan yang ada pada C. osmophloeum hydrosols (Rajah 3A), yang dihasilkan menggunakan penyulingan wap. Pengurangan kuasa biasanya dikaitkan dengan kehadiran agen pengurangan dan aktiviti antioksidan, mencerminkan pemberhentian tindak balas rantai radikal bebas dengan penyediaan atom hidrogen yang mengurangkan. Kuasa pengurangan C. osmophloeum mungkin disebabkan oleh kehadiran kumpulan hidroksil dalam sebatian fenolik (Rajah 2), yang mungkin bertindak sebagai penderma elektron.
3.2.4. Ujian TEAC
Nilai TEAC hidrosol sekarang telah meningkat pada kepekatan yang lebih tinggi daripada 5.32 × 10−3 mg/mLand adalah lebih besar daripada sebatian rujukan -tokoferol dan BHT, seperti yang ditunjukkan dalam Rajah 3A. Kebolehcapaian Sterik ke tapak radikal ABTS plus ialah kriteria utama untuk aktiviti dalam ujian TEAC. Oleh itu, kumpulan fenil bagi juzuk hidrosol sekarang adalah kurang terhalang sedikit daripada Trolox.
3.2.5. Korelasi antara TPC dan Aktiviti Antioksidan
Seperti yang ditunjukkan dalam Rajah 3B, terdapat korelasi yang sangat ketara antara TPC dan aktiviti penghapusan radikal bebas DPPH di GAE daripada 1.75 ± 0.438 kepada 100.41 ± 1.581 mg/g . Pekali korelasi TPC dengan aktiviti penghapusan radikal bebas DPPH, aktiviti FIC, pengurangan kuasa dan TEAC masing-masing ialah0.980, 0.925, 0.967 dan 0.902, masing-masing (Rajah 3B). Secara kolektif, data ini menunjukkan bahawaantioksidanaktiviti hidrosol COK berkait rapat dengan kandungan fenol.
3.3. Kesan Kepekatan Hidrosol COK terhadap Aktiviti Tirosinase
Kami menentukan kesan kepekatan hidrosol COK pada pengoksidaan L-tirosin dan L-DOPA oleh cendawantyrosinasedan membuat perbandingan dengan aktiviti asid kojik, yang merupakan perencat tyrosinase yang terkenal (Rajah 3C, D). Hidrosol sekarang secara kuat dan bergantung kepada dos menghalang aktiviti L-tirosin dan L-DOPA oksidase cendawan tyrosinase (Rajah 3C) tetapi mempunyai aktiviti perencatan tirosinase yang lebih tinggi dengan kehadiran substrat L-tirosin (aktiviti monophenolase) daripada L-DOPA (aktiviti diphenolase). Nilai IC5{{10}} asid kojik terhadap monophenolase dan diphenolaseactivities ialah 4.0 × 10−5 dan 7.8 × 10−3 mg/mL (Rajah 3C), masing-masing, lebih ketara daripada hidrosol sekarang (masing-masing 7.96 × 10−4 mg/mL dan 0.35 mg/mL; Rajah 3D). Oleh itu, untuk mencapai 90 peratus aktiviti perencatan tyrosinase (aktiviti monophenolase), hidrosol dan asid kojik diperlukan pada 0.52 mg/mL dan 4.0 × 10−3 mg/mL, masing-masing apabila L-tirosin digunakan sebagai substrat (Rajah 3C, D ). Walaupun kesan perencatan tyrosinase memerlukan kepekatan COK hydrosolthan kojic acid yang lebih tinggi, aktiviti perencatan tyrosinase yang kuat terbukti dalam eksperimen ini.
Macam-macamtyrosinasepersediaan, kaedah ujian aktiviti, dan ketulenan dan komponen perencat boleh menyumbang kepada perbezaan dalam kinetik perencatan enzim [29]. Walau bagaimanapun, aktiviti biologi ekstrak tumbuhan disumbangkan oleh komponen bioaktifnya, yang mungkin dipengaruhi oleh spesies tumbuhan, masa menuai, musim, asal geografi, amalan agronomi dan kaedah pengekstrakan. Perencat telah dikenal pasti dan dicirikan daripada sumber semula jadi dalam banyak kajian baru-baru ini, dan hubungan antara aktiviti perencatan dan bahan semula jadi telah mantap (Jadual 1). Khususnya, banyak aldehid dan sebatian lain telah diasingkan dan dicirikan sebagai perencat tyrosinase. Ini termasuk cinnamaldehyde, 2-hydroxy-4-methoxy benzaldehyde, anisaldehyde, cuminaldehyde, asid kumik, flavonol, flavon dan isoflavan [4,19,30–37]. Hidrosol sekarang mengandungi 87.7 peratus sinamaldehid dan 7.0 peratus benzaldehid, menunjukkan bahawa sinamaldehid, diikuti benzaldehid, adalah bahan utama yang bertanggungjawab untuk aktiviti perencatan tyrosinase hidrosol. Selaras dengan Jadual 1, kami mendapati bahawa hidrosol dengan kehadiran benzaldehid adalah lebih kuat. daripada cinnamaldehyde tulen, dan meningkatkantyrosinaseaktiviti perencatan hidrosol. Benzaldehydes juga disahkan menghalang kedua-dua aktiviti diphenolase dan aktiviti monophenolase mushroomtyrosinase [38]. Mekanisme perencatan tyrosinase bagi perencat jenis benzaldehid mungkin berasal daripada keupayaan mereka untuk membentuk bes Schiff dengan kumpulan amino primer dalam enzim [33,39]. Penambahan kumpulan penderma elektron pada kedudukan para benzaldehid meningkatkan aktiviti perencatan tyrosinase, mungkin menstabilkan pangkalan Schiff.

3.4. Mod Kinetik Perencatan Tirosinase Cendawan oleh COK Hydrosol
Tingkah laku kinetik hidrosol, pada monophenolase dan aktiviti diphenolase tyrosinasemenggunakan L-tirosin dan L-DOPA sebagai substrat telah dikaji, masing-masing. Thetyrosinasekinetik perencatan hidrosol telah dianalisis menggunakan plot timbal balik berganda Lineweaver-Burk, seperti yang ditunjukkan dalam Rajah 4. Dalam Rajah 4A, B, empat garisan mewakili enzim tidak dihalang (Baris 1) dan perencatan oleh tiga kepekatan (Baris 2 - Baris 4) hidrosol, dan garisan ini bersilang di sebelah kiri paksi 1/v di atas paksi 1/S. Di bawah keadaan percubaan tanpa halangan, halaju maksimum (Vmaks) tindak balas pengoksidaan L-tirosin dan L-DOPA yang dimangkin oleh tyrosinase ialah {{10}}.055 ∆OD475/min dan 0.096 ∆OD475/min tanpa mengandungi hidrosol (Baris 1 dalam Rajah 4A, B), masing-masing. Parameter kinetik Km (pemalar Michaelis) untuk cendawantyrosinasediperoleh daripada Lineweaver–Burk plot menggunakan L-tirosin dan L-DOPA sebagai substrat, masing-masing menunjukkan bahawa Km ialah 0.534 mg/mL dan0.511 mg/mL tanpa mengandungi hidrosol (Garisan 1 dalam Rajah 4A, B).
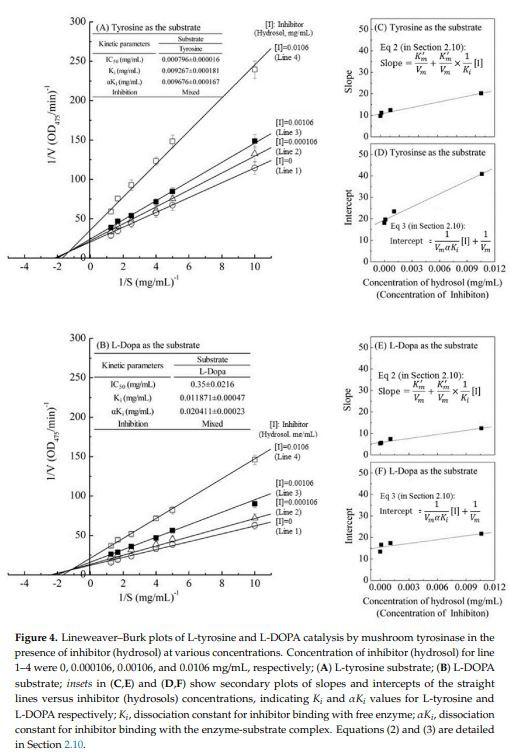
Empat garisan, yang diperoleh daripada enzim yang tidak dihalang dan daripada tiga pelbagai kepekatan hidrosol, bersilang di sebelah kiri paksi 1/v di atas paksi 1/S. Peningkatan kepekatan hidrosol mengakibatkan penurunan Vmax dan peningkatan Km. Secara khusus, apabila L-tirosin digunakan sebagai substrat, peningkatan kepekatan hidrosol menghasilkan berbilang garisan dengan pelbagai cerun dan pintasan, tetapi ini bersilang antara satu sama lain dalam kuadran kedua (Baris 1–4 dalam Rajah 4A). Keputusan yang sama diperoleh apabila L-DOPA digunakan sebagai substrat (Barisan 1–4 dalam Rajah 4B), menyokong penegasan bahawa hidrosol membawa perencat jenis campuran tyrosinase. Selaras dengan perencatan jenis campuran, komponen hidrosol berkemungkinan mengikat enzim bebas dan kompleks enzim-substrat. Perencatan jenis campuran boleh timbul dalam pelbagai cara: perencatan hidrosol boleh timbul kerana mereka berinteraksi dengan perantaraan selepas itu dalam corak tindak balas tetapi tidak dengan kompleks enzim-substrat awal [40]. Oleh itu, kami menentukan pemalar penceraian (Ki dan Ki, masing-masing) untuk perencat yang mengikat enzim bebas (E) dan kompleks enzim-substrat menggunakan plot salingan berganda dan plot cerun dan pintasan menegak berbanding kepekatan hidrosol dengan kehadiran L-tirosin (Rajah 4C, D) atau L- DOPA sebagai substrat (Rajah 4E, F). Seperti yang ditunjukkan dalam Rajah 4A, B, nilai Ki apabila L-tirosin digunakan sebagai substrat adalah kira-kira 1.28 kali lebih rendah daripada dengan kehadiran L-DOPA, menunjukkan pengikatan enzim perencatan yang lebih berkesan dengan L-tirosin berbanding dengan L-DOPA. Selain itu, nilai Ki adalah 1.71 kali lebih besar daripada nilai Ki untuk pengoksidaan L-DOPA, menunjukkan bahawa pertalian komponen hidrosol untuk enzim bebas adalah lebih kuat daripada kompleks enzim-substrat. Data ini mencadangkan bahawa hidrosol mempengaruhi pertalian enzim untuk L-DOPA tetapi tidak mengikat tapak aktif. Selain itu, nilai Ki adalah hampir sama dengan Ki untuk pengoksidaan L-tirosin, menunjukkan bahawa perencat campuran adalah perencat tidak kompetitif, yang mengikat enzim bebas dan kompleks enzim-substrat dengan pemalar keseimbangan yang sama menggunakan L- tirosin sebagai substrat (Rajah 4A). Walau bagaimanapun, pemalar pengikatan keseimbangan untuk enzim bebas dan kompleks-substrat enzim, masing-masing berbeza menggunakan L-DOPA sebagai substrat (Rajah 4B), menunjukkan bahawa perencat jenis campuran (campuran kompetitif dan bukan persaingan) boleh mengikat bukan sahaja dengan enzim bebastetapi juga dengan kompleks enzim-substrat menggunakan L-DOPA sebagai substrat. Kajian terdahulu juga mendedahkan bahawa minyak pati C. cassia dan cinnamaldehyde adalah perencat jenis campuran [19]. Sebaliknya, trans-cinnamaldehyde yang diasingkan daripada kulit C. cassia menunjukkan perencatan kompetitif untuk pengoksidaan L-DOPA oleh cendawan.tyrosinase[32], manakala sinamaldehid diasingkan daripada akar P. cernua adalah perencatan tidak kompetitif [35].
3.5. Kesan Bergantung Kepekatan Kepekatan Hidrosol terhadap Melanogenesis
Untuk menguji kesan hidrosol pada daya maju sel dan melanogenesis pada kepekatan yang berbeza-beza ({{0}}.0035–10.64 mg/mL), kami mendorong melanogenesis dalam sel melanoma B16-F10 menggunakan -MSH dan dibandingkan kesan menggunakan asid kojik sebagai kawalan positif (Rajah 5). Keputusan ujian daya maju sel ini menunjukkan bahawa hidrosol tidak mempunyai sitotoksisiti pada kepekatan 0.0035–1.064 mg/mL dalam sel B16F10melanoma (Rajah 5a). Memandangkan perencat melanogenesis sedang dibangunkan, keselamatan dan keberkesanan harus menjadi pertimbangan yang paling penting untuk banyak aplikasi. Walau bagaimanapun, rawatan sel B16F10melanoma dengan hidrosol menghasilkan pengurangan ketara daya maju sel pada kepekatan 5.32–10.64 mg/mL. Mengikut keputusan daripada kajian saringan keselamatan dan keberkesananpemutihan kulitproduk dalam kultur sel B16F10, 1.064 mg/mL ialah kepekatan ambang untuk saringan primer berasaskan sel. Oleh itu, kepekatan 0.1064-1.064 mg/mL telah digunakan untuk mengkaji mekanisme anti-tirosinase dalam sel melanoma B16F10 oleh hidrosol.
Penindasan melanogenesis oleh rawatan hidrosol pada pelbagai kepekatan telah ditentukan aspercentages kandungan melanin dalam sel (Rajah 5b). Kami juga menganalisis tahap ekspresi MITF menggunakan Western blotting (Rajah 5c). Dalam eksperimen ini, kandungan melanin dan tahap ekspresi MITF ditindas bergantung kepada dos oleh hidrosol COK, menunjukkan bahawa hidrosol COK mengurangkan kandungan melanin dalam sel dengan menekan sintesis MITF.

3.6. Ujian Perlindungan DNA
Spesies oksigen reaktif terkenal merosakkan DNA dan menyebabkan penuaan sel dan kanser. Ujian DNAnicking menawarkan sistem model bebas sel yang mudah untuk menentukan secara sensitif pengeluaran radikal yang merosakkan DNA [41]. Dalam eksperimen ini, tindak balas Fenton menghasilkan radikal hidroksil yang membelah DNA plasmid supergegelung dan menukarnya kepada bentuk DNA yang dicakar, yang telah menurunkan mobiliti elektroforetik. [42,43]. Oleh itu, untuk menilai aktiviti perlindungan DNA hidrosol, kami menginkubasi DNA neo pCI dengan reaktan Fenton [44]. Seperti yang ditunjukkan dalam Rajah 6, bentuk plasmid supercoiled dan nicked jelas dibezakan oleh kadar mobiliti elektroforetik relatifnya pada gel agarose; supercoiledDNA bergerak paling pantas, dan DNA nicked masing-masing bergerak paling perlahan. Selepas rawatan dengan hidrosol, kerosakan DNA berkurangan sedikit pada kepekatan hidrosol 1.33–5.32 mg/mL, masing-masing dengan perlindungan 28–58 peratus bagi bentuk bergelung besar (lorong 6–8). Pada kepekatan hidrosol 0.3325–0.665 mg/mL, tiada perlindungan diperhatikan berbanding kawalan negatif (lorong 4 dan 5). Sebaliknya, kuersetin melindungi DNA plasmid secara berkesan daripada radikal hidroksil- pemecahan pengantara, seperti yang ditunjukkan sebelum ini [45]. Ini adalah data pertama yang menunjukkan kesan perlindungan ekstrak hidrosol daripadaC. daun osmophloeum Kanehira pada kerosakan DNA oleh tindak balas Fenton. Kesan ini mungkin disebabkan oleh kehadiran sebatian polifenol.
4. Kesimpulan
COK telah lama digunakan sebagai tumbuhan ubatan di Taiwan. Walau bagaimanapun, untuk pengetahuan kami, ini adalah laporan pertama yang menunjukkan bahawa hidrosol yang disediakan melalui penyulingan wap daripada daun COK mempunyai aktiviti antioksidan, seperti yang diperhatikan dalam ujianantioksidanaktiviti dan kerosakan DNA. Kami juga menunjukkan bahawa hidrosol ini menindas melanogenesis. Dalam analisis GC/MS, sebatian utama dalam hidrosol COK didapati ialah sinamaldehid dan benzaldehid, dan agen ini kuat menghalang aktiviti monophenolase dan diphenolase tyrosinase. Dalam penilaian kami tentang kinetik perencatan tyrosinase, COK hydrosol mempamerkan perencatan bergantung dos jenis campuran bagi kedua-dua aktiviti L-tirosin dan L-DOPA oksidasetyrosinase. Sebatian hidrosol sekarang juga menindas ekspresi protein MITF, yang membawa kepada pengurangan sintesis melanin yang disebabkan oleh MSH.
Akhir sekali, keselamatan adalah pertimbangan utama untuk perencat tyrosinase, terutamanya bagi yang digunakan dalam kosmetik dan produk makanan, yang boleh digunakan dalam kuantiti terkawal. COK sudah menjadi bahan tambahan semulajadi yang boleh dimakan dan digunakan secara meluas untuk makanan dan kosmetik. Tambahan pula, cinnamaldehyde secara amnya diiktiraf sebagai selamat untuk penggunaan manusia. COK hydrosol ialah biobahan semulajadi yang sangat baik dengan berkesan dan selamattyrosinasedan aktiviti perencatan sintesis melanin dan potensi untuk melindungi daripada kerosakan DNA. Oleh itu, kami percaya bahawa COK hidrosol boleh digunakan sebagai agen depigmen yang selamat dan berkesan untuk banyak aplikasi.

