Bahagian Tiga Peranan Hidrogen Sulfida dalam Fisiologi Buah Pinggang Dan Keadaan Penyakit
Jun 13, 2023
1. Peranan H2S dalam nefropati diabetik
DM adalah penyakit berleluasa yang mengancam kesihatan manusia secara serius. DM boleh menjejaskan organ penting dan menimbulkan beban perubatan yang besar kepada keluarga dan masyarakat [83]. Nefropati diabetik (DN) adalah salah satu komplikasi mikrovaskular DM yang paling teruk. Ciri-ciri patologi utama DN ialah sklerosis glomerular dan fibrosis interstisial [84], dan mekanisme itu dianggap melibatkan induksi OS [85], pengumpulan produk akhir glikosilasi lanjutan (AGEs) [86], pengaktifan laluan isyarat keradangan dan fibrosis [87], hemodinamik buah pinggang yang tidak normal dan pengaktifan RAAS yang tidak normal, sekunder kepada hiperglikemia kronik [88].
Bukti semasa menunjukkan bahawa kekurangan H2S menyumbang kepada pembangunan DN. Tahap H2S plasma adalah lebih rendah pada pesakit dengan DM jenis 2 (T2DM) berbanding individu normal, dan keputusan yang sama telah ditemui pada tikus diabetes [89]. Tahap tinggi sulfat kencing berkaitan dengan kepekatan H2S plasma yang tinggi, dan sulfat kencing yang tinggi boleh mengurangkan risiko perkembangan penyakit buah pinggang dalam pesakit T2DM [90].
Di samping itu, kandungan H2S plasma dalam pesakit DM yang menjalani dialisis adalah lebih rendah daripada populasi normal, dan pada pesakit hemodialisis kronik, tahap H2S yang lebih rendah dikaitkan dengan kecenderungan yang lebih tinggi untuk aterosklerosis uremik [91]. Kajian terbaru menunjukkan bahawa suplemen H2S boleh melambatkan perkembangan DN. Rawatan dengan NaHS memperbaiki lesi buah pinggang dalam T2DM dengan meningkatkan pengambilan glukosa dalam myotubes dan adiposit [92]. Suplemen dengan H2S atau prekursor endogen H2S (L-cysteine) dalam medium kultur menghalang pembebasan sitokin proinflamasi seperti IL-8 dan protein chemotactic monocyte-1 dalam monosit U937 manusia yang dirawat dengan glukosa tinggi [89]. Kami meringkaskan peranan H2S dalam DN dalam Jadual 2 [93-100].

1.1. H2S mengurangkan nefropati diabetik dengan mengurangkan tekanan oksidatif
OS berkembang disebabkan oleh ketidakseimbangan antara tahap ROS dalam sel dan sistem antioksidan [101]. Peningkatan paras glukosa darah membawa kepada pengaktifan laluan protein kinase C dalam sel buah pinggang. Protein kinase C mengaktifkan NADPH II dalam mitokondria dan kemudian meningkatkan OS, yang membawa kepada pengembangan kawasan mesangial glomerular, penebalan membran bawah tanah, gangguan fungsi sel endothelial, dan proteinuria [102]. Pengeluaran ROS juga mengakibatkan pengumpulan matriks ekstraselular, pengaktifan faktor fibrosis, dan kecederaan podosit [103]. Glukosa boleh membentuk AGE dengan pelbagai protein di bawah keadaan nonenzimatik, dan AGE boleh mendorong tindak balas OS dan meningkatkan aktiviti protein kinase C, sekali gus mendorong peningkatan pengeluaran kemokin radang [104].
Secara keseluruhan, glukosa tinggi mendorong OS dalam sel buah pinggang, dan H2S boleh mengambil bahagian dalam proses ini. Marwa et al. [105] mendapati bahawa kerosakan buah pinggang yang disebabkan oleh hiperglisemia melalui OS boleh dilawan oleh NaHS. H2S boleh melindungi fungsi buah pinggang dalam tikus T1DM dengan cara yang berkaitan dengan penindasan OS melalui peningkatan aktiviti superoksida dismutase [106].
Di bawah keadaan fisiologi, Keap1 merata-rata dan merendahkan Nrf2. Walau bagaimanapun, di bawah keadaan antioksidan, tegasan ricih, atau pendedahan agen elektrofilik, Nrf2 berpisah daripada Keap1 dan berpindah ke nukleus, di mana ia menggalakkan ekspresi gen antioksidan hiliran [107]. Eksperimen haiwan telah menunjukkan bahawa pengaktifan laluan isyarat Nrf2 buah pinggang mengurangkan kecederaan OS dan proteinuria dan meningkatkan matriks ekstraselular dan penebalan membran bawah tanah [108]. Dalam sel endothelial yang dirawat dengan glukosa tinggi, H2S mendorong pemisahan Nrf2 dari Keap1 dengan meningkatkan S-sulfihidrasi Keap1, meningkatkan translokasi Nrf2 ke nukleus dan mendorong ekspresi gen antioksidan hiliran, dengan itu mengurangkan tahap molekul OS dan lekatan [109]. Kajian terdahulu telah menunjukkan bahawa H2S mengaktifkan Nrf2 dan meningkatkan ekspresi protein heme oxygenase-1, dengan itu meningkatkan rintangan buah pinggang terhadap OS dalam tikus DM [110].
Kajian terbaru telah mencadangkan bahawa glukosa tinggi boleh mendorong ekspresi NADPH oksidase 4 (NOX4) dan sintesis matriks ekstraselular dengan menurunkan kawal selia kinase protein kinase (AMPK) yang diaktifkan adenosin monofosfat kinase dalam sel buah pinggang [111]. NOX4 ialah ahli kumpulan NADPH oksidase daripada keluarga NOX dan merupakan sumber utama ROS dalam buah pinggang [112]. H2S merekrut iNOS untuk menjana NO untuk menghalang ekspresi NOX4 yang disebabkan oleh glukosa tinggi, OS, dan pengumpulan protein matriks [111].
Glukosa tinggi merekrut sasaran mamalia kompleks rapamycin 1 untuk memburukkan hipertrofi dan meningkatkan sintesis protein dalam sel epitelium dan mesangial buah pinggang. Dalam DN, phosphatidylinositol 3 kinase/protein kinase B/ sasaran mamalia bagi isyarat kompleks rapamycin 1 diaktifkan kerana penindasan aktiviti AMPK [6,113]. Rawatan dengan NaHS membalikkan penurunan fosforilasi AMPK yang disebabkan oleh glukosa tinggi, yang mengurangkan kerosakan buah pinggang [114].

Klik di sini untuk mendapatkanfaedah Cistanche
Autophagy terdiri daripada beberapa langkah kompleks, terutamanya pembentukan vesikel fagositik, sintesis autofagosom, pembentukan autophagolysosomes selepas gabungan autofagosom dan lisosom, dan degradasi autophagolysosomes secara beransur-ansur. Autophagy boleh mengais sisa dalam sel untuk mencapai homeostasis selular dan pembaharuan organel [115]. Dalam pesakit DM, kepekatan ROS meningkat apabila hiperglikemia berterusan, yang boleh menyebabkan autophagy berlebihan atau autophagy terganggu, yang boleh merosakkan sel endothelial [116]. Dalam sel endothelial, kerosakan mitokondria yang disebabkan oleh glukosa tinggi/palmitat dikaitkan dengan OS. Kerosakan mitokondria mengurangkan pengeluaran ATP dan menyebabkan pengaktifan berlebihan berterusan laluan isyarat AMPK, dengan itu membawa kepada autophagy yang berlebihan dan merosakkan sel endothelial lagi. Rawatan H2S boleh menghalang OS dan melemahkan autophagy yang berlebihan [117].
Dalam tahun-tahun kebelakangan ini, semakin banyak kajian mendapati bahawa H2S boleh mengurangkan OS dan menghalang autophagy yang berlebihan yang disebabkan oleh OS, yang mungkin menyediakan jalan baharu untuk rawatan DN.
1.2. Keradangan dan H2S dalam nefropati diabetik
Sistem imun yang tidak normal dan keradangan kronik memainkan peranan penting dalam perkembangan patologi DN [102]. NF-jB adalah pautan pusat dan laluan biasa yang mengawal transkripsi banyak faktor keradangan dan faktor utama dalam kecederaan keradangan endothelial [118]. Apabila laluan NF–jB sel buah pinggang diaktifkan, sel merembeskan faktor lekatan seperti molekul lekatan antara sel–1 dan protein lekatan sel vaskular–1 serta kemokin seperti protein kemotaktik monosit–1 dan IL–1. Molekul dan kemokin lekatan ini menarik monosit, makrofaj, dan limfosit T ke dalam buah pinggang, dengan itu mengaktifkan isyarat TNF dan membawa kepada peningkatan patologi buah pinggang dan fibrosis [119,120]. Dalam tikus dengan DM yang disebabkan oleh streptozotocin (STZ), NaHS melakukan tindakan anti-radang dengan menghalang isyarat NF-jB dalam sel mesangial glomerular [110].
MMP-9, endopeptidase yang bergantung kepada zink, adalah sitokin radang yang membawa kepada degradasi matriks ekstraselular dan pembentukan semula vaskular buah pinggang [121]. Kundu et al. [122] menunjukkan bahawa MMP-9 mengurangkan ekspresi CBS dan CSE dan mengurangkan kandungan H2S dalam tikus DM dan rawatan dengan H2S membalikkan pembentukan semula buah pinggang DM yang disebabkan oleh MMP-9.
1.3. H2S meningkatkan nefropati diabetik dengan melemahkan aktiviti RAAS
RAAS klasik merangkumi beberapa langkah. Secara ringkas, buah pinggang merembeskan renin, yang mengaktifkan angiotensinogen yang dihasilkan daripada hati untuk menghasilkan Ang I. Ang I kemudiannya ditukar kepada Ang II dalam peredaran pulmonari. Ang II, efektor utama RAAS, bertindak pada reseptor Ang II jenis I, menyebabkan otot licin arteriol mengecut dan merangsang rembesan aldosteron ke dalam sferoid korteks adrenal [123]. Hiperglisemia mengaktifkan RAAS buah pinggang, meningkatkan tekanan hidrostatik glomerular, dan menyebabkan proteinuria, glomerulosklerosis, dan fibrosis interstisial [124]. Sekatan RAAS telah ditunjukkan untuk melambatkan perkembangan DN [125]. Seperti yang dinyatakan sebelum ini, renin dirembeskan oleh sel juxtaglomerular, dan H2S boleh mengawal pelepasan renin dengan merendahkan cAMP. Dalam model murine kegagalan jantung yang disebabkan oleh penyempitan aorta melintang, rawatan dengan H2S mengurangkan pengaktifan patologi RAAS buah pinggang dan melindungi jantung, buah pinggang, dan saluran darah [126]. Dalam DN, H2S boleh memainkan peranan pencegahan dengan mengawal pelepasan dan aktiviti renin [22].

suplemen cistanche
H2S juga boleh menghalang sistem RAAS dengan mengawal selia pautan lain. Berbanding dengan sel yang dirangsang glukosa normal, sel yang dirangsang glukosa tinggi mempamerkan regulasi ketara angiotensinogen, enzim penukar angiotensin, dan tahap mRNA reseptor Ang II jenis I, tetapi regulasi ini boleh diterbalikkan dengan rawatan dengan H2S [127]. Satu kajian telah mendapati bahawa tahap ekspresi protein enzim penukar angiotensin, reseptor reseptor Ang II jenis I, dan Ang II dikawal dengan ketara dalam DN. Protein ini dikurangkan selepas rawatan NaHS [110].
Oleh itu, H2S boleh melemahkan OS dan tindak balas keradangan dan menghalang pengaktifan patologi RAAS. Pada peringkat awal DN, H2S boleh memperbaiki penebalan membran bawah tanah glomerular dan hiperplasia matriks mesangial. Pada peringkat akhir, H2S boleh melambatkan fibrosis buah pinggang dan memperbaiki pembentukan semula buah pinggang. Oleh itu, H2S terlibat dalam pelbagai peringkat DN (Rajah 2).
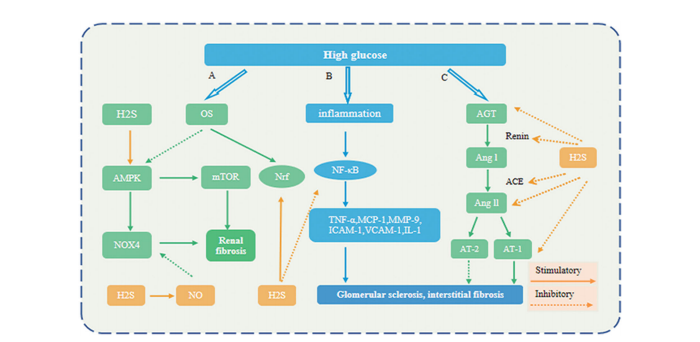
Rajah 2. Mekanisme yang mendasari kesan perlindungan H2S dalam DN. (A) H2S merangsang pembentukan NO, yang mengurangkan tahap NOX4; H2S mengaktifkan AMPK, dengan itu menyekat isyarat mTOR; dan H2S mengaktifkan laluan Nrf2. (B) H2S bertindak sebagai faktor anti-radang dengan menyekat isyarat NF-jB dalam sistem buah pinggang. (C) Renin menukarkan AGT kepada Ang I. Di bawah tindakan ACE, Ang I seterusnya ditukar kepada Ang II, dan Ang II mengikat kepada AT–1, yang memburukkan DN. Pengaktifan RAAS dalam DN diperbaiki oleh rawatan H2S melalui perencatan reseptor AGT, renin, ACE, Ang II, dan AT-1. OS (Tekanan oksidatif); AMPK (kinase protein diaktifkan AMP); NO (nitrik oksida); mTOR (sasaran mekanistik rapamycin); Nrf (Faktor nuklear–erythroid 2–faktor berkaitan 2); NOX4 (NADPH oksidase 4). TNF-a (faktor nekrosis tumor-a); IL-1b (interleukin-1b); VCAM–1 (molekul lekatan sel vaskular–1); ICAM–1(molekul lekatan antara sel–1); MCP-1 (protein kemotaktik monosit-1); MMP-9 (matriks metalloproteinase-9). AGT (Angiotensinogen); ACE (enzim penukar angiotensin); AngI (angiotensin I); AngII (angiotensin II); AT–1 (reseptor Ang II jenis I1).
2. Peranan H2S dalam nefropati hipertensi
Nefropati hipertensi adalah penyebab utama kedua penyakit buah pinggang peringkat akhir selepas DM [128]. Kebanyakan pesakit hipertensi mengalami nefrosklerosis hipertensi ringan hingga sederhana, dengan hanya sedikit pesakit yang memasuki penyakit buah pinggang peringkat akhir. Namun begitu, kejadian penyakit buah pinggang peringkat akhir meningkat secara mendadak apabila nilai BP tidak terkawal untuk jangka masa yang lama atau apabila penyakit buah pinggang adalah keadaan sedia ada [129,130]. Kawalan hipertensi jangka panjang yang lemah memburukkan lagi kerosakan buah pinggang. Kerosakan buah pinggang meningkatkan lagi tahap BP. Oleh itu, hipertensi jangka panjang dan kerosakan buah pinggang membentuk kitaran ganas, mengakibatkan pelbagai kerosakan organ [131].

Herba Cistanche
Walaupun mekanisme khusus tidak jelas, kajian telah mendedahkan bahawa tikus yang kekurangan CSE menunjukkan hipertensi yang ketara dan mengurangkan vasorelaxation yang bergantung kepada endothelium [132]. Dalam tikus, BP juga boleh ditingkatkan melalui perencatan enzim penghasil H2S (CBS dan CSE) [133]. Seperti yang dinyatakan di atas, H2S meningkatkan anggaran GFR (eGFR) dan perkumuhan natrium melalui kencing. Di samping itu, H2S mengawal BP dengan mengawal secara langsung ketegangan vaskular. H2S diakui sebagai faktor hiperpolarisasi yang berasal dari endothelium yang bertindak dengan menyulfhidrat sisa sistein saluran K-ATP [15]. Di samping itu, H2S boleh mengaktifkan laluan isyarat cAMP/protein kinase A, membebaskan kalsium, dan mengawal vasorelaksasi [134].
PPAR ialah kelas faktor transkripsi nuklear yang diaktifkan ligan yang tergolong dalam superfamili reseptor. Tiga subjenis PPAR, PPAR–a PPAR–b/d, dan PPAR–c, telah ditemui. Setiap subjenis PPAR boleh mengurangkan keabnormalan metabolik di bawah tindakan agonis; bagaimanapun, mekanisme tindakan mereka adalah berbeza. Sebagai contoh, pengaktifan PPAR-b / d boleh meningkatkan BP dengan ketara dengan meningkatkan NO dan berfungsi sebagai sasaran terapeutik baru untuk hipertensi [135,136]. Kajian terkini menunjukkan bahawa peranan H2S dalam mengawal selia BP mungkin berkaitan dengan pengaktifan PPARb/d. H2S dianggap berfungsi dengan NO secara sinergi untuk mengawal nada vaskular. Mekanisme molekul tertentu mungkin melibatkan peningkatan regulasi H2S-pengantara ekspresi PPAR-d, peningkatan protein kinase B atau fosforilasi AMPK, dan peningkatan fosforilasi eNOS dengan peningkatan pengeluaran NO [137,138]. Dalam tikus, penggunaan perencat NOS, seperti Nx-nitro-l-arginine metil ester, boleh menyebabkan hipertensi, yang boleh diterbalikkan dengan rawatan dengan NaHS [139]. Walau bagaimanapun, dalam cincin aorta tikus, kepekatan rendah NaHS (10-100 lM) boleh mengurangkan pengeluaran NO dan seterusnya menyebabkan vasokonstriksi. Sebaliknya, pentadbiran NaHS dos yang tinggi telah dilaporkan secara langsung melonggarkan cincin aorta [140]. Penemuan ini mencadangkan peranan crosstalk H2S / NO dalam peraturan BP. Kesan antihipertensi H2S juga bergantung kepada dos, tetapi mekanisme khusus memerlukan kajian lanjut [6].
Ang II boleh menguncup keseluruhan arteriol. Di samping itu, ia boleh menggalakkan rembesan aldosteron dalam korteks adrenal. Aldosteron bertindak pada tubulus buah pinggang dan meningkatkan jumlah darah. Tambahan pula, Ang II mendorong OS dengan mengikat reseptor angiotensin 1 untuk menengahi pengumpulan ROS yang berlebihan, yang membawa kepada kerosakan endothelial. Di buah pinggang, Ang II memburukkan lagi keradangan organ sasaran dengan meningkatkan pembentukan superoksida dan pembebasan kemokin [141,142]. Sebagai tambahan kepada pembebasan renin yang menghalang H2S, satu lagi mekanisme yang mungkin ialah H2S eksogen menghalang pengikatan Ang II kepada reseptor Ang II jenis I, mengurangkan isyarat pengantara Ang II dan menghalang perkembangan patologi pada tikus. Pada tikus dengan hipertensi yang disebabkan oleh Ang II, H2S juga boleh menghalang pengeluaran ROS dalam saluran darah dan mengeluarkan ROS, meningkatkan kapasiti antioksidan [143].
Ringkasnya, H2S memainkan peranan yang sangat diperlukan dalam mengawal BP, mengurangkan proteinuria, dan melambatkan disfungsi buah pinggang dan kemerosotan struktur dengan menghalang Ang II, dan meningkatkan pengeluaran NO [143]. Oleh itu, H2S boleh berubah menjadi sasaran unik untuk rawatan nefropati hipertensi.

Ekstrak cistanche
3. Peranan H2S dalam penyakit buah pinggang obstruktif
Nefropati obstruktif ialah penyakit urologi biasa yang merangkumi batu karang, penyakit buah pinggang polikistik, dan stenosis arteri renal. Halangan ureter mempercepatkan fibrosis buah pinggang, yang dikaitkan dengan permulaan dan perkembangan nefropati obstruktif [144]. Fibrosis buah pinggang juga merupakan ciri patologi utama dalam CKD [145]. Dalam model tetikus halangan ureter (UUO) unilateral, tahap aktiviti enzim pengeluaran H2S dan H2S, termasuk CBS dan CSE, telah disahkan menurun dengan ketara. Selepas pentadbiran NaHS, tahap H2S meningkat, dan fibrosis buah pinggang dikurangkan, dan perubahan ini disertai dengan peningkatan kepekatan H2S [146]. Kerosakan buah pinggang yang disebabkan oleh UUO berkait rapat dengan keradangan dan fibrosis buah pinggang. Kajian terdahulu telah menunjukkan bahawa H2S mengambil bahagian dalam keadaan patologi ini [147]. Suplemen dengan H2S eksogen mengurangkan kecederaan buah pinggang akibat UUO. Tambahan pula, penyelidikan baru-baru ini telah menunjukkan bahawa dalam model tikus nefropati obstruktif, GYY4137 memperbaiki kerosakan keradangan dan fibrosis tubulointerstitial [148,149], seperti juga NaHS [150,151]. Kami meringkaskan peranan H2S dalam penyakit buah pinggang obstruktif dalam Jadual 3 [145-152].

3.1. H2S mengurangkan penyakit buah pinggang obstruktif dengan mengurangkan tekanan oksidatif dan keradangan
Keradangan, OS, ketegangan vaskular, dan laluan isyarat intraselular terlibat dalam perkembangan fibrosis buah pinggang. Induksi fibrosis diburukkan lagi oleh tekanan oksidatif, kerana ROS telah dilaporkan meningkatkan ekspresi Ang II dan TGF-b1 [153,154]. H2S boleh meningkatkan aktiviti enzim antioksidan seperti glutathione dan superoxide dismutase untuk menentang OS. Nrf2 ialah faktor transkripsi yang mengawal tindak balas penyesuaian kepada OS. H2S telah ditunjukkan untuk mendorong ekspresi gen enzim antioksidan dan pengaktifan Nrf2 [107,146]. Autophagy yang berlebihan yang disebabkan oleh peningkatan dalam OS boleh menyebabkan disfungsi endothelial vaskular. Rawatan dengan NaHS dengan ketara memperbaiki kerosakan buah pinggang dalam tikus UUO, mungkin dengan menghalang laluan ROS-AMPK [152].
UUO menyebabkan keradangan pada buah pinggang. Kajian telah mendapati bahawa H2S eksogen menghalang pengaktifan NF-jB, membawa kepada pengurangan tindak balas keradangan, dan mengawal pengeluaran sitokin proinflamasi seperti IL-1b dan TNF-a, yang juga terdapat dalam sel jantung H9C2 [146,155]. Mekanisme isyarat ciri fibrosis buah pinggang melibatkan laluan TGF-b1-Smad dan MAPK. H2S melemahkan fosforilasi Smad3 dan menyekat pengaktifan kinase MAPK. Di samping itu, pentadbiran NaHS mengurangkan ekspresi gen yang berkaitan dengan percambahan, seperti antigen nuklear sel proliferasi dan c-Myc, untuk menghalang percambahan fibroblast dan peralihan fenotip kepada myofibroblast [147].
3.2. H2S dan makrofaj dalam penyakit buah pinggang obstruktif
Zhou et al. [145] mendapati bahawa dalam buah pinggang terhalang tikus UUO, pengurangan pengeluaran H2S berkaitan dengan peningkatan penyusupan makrofaj. Makrofaj ialah sel imun yang terletak di dalam tisu yang berasal daripada monosit dan mempunyai fungsi yang luas. Makrofaj lebih suka mendorong iNOS atau arginase dan dikelaskan sebagai makrofaj M1 atau M2 [156]. Makrofaj M1 yang diaktifkan menyebabkan kerosakan tisu dan keradangan dengan meningkatkan tahap sitokin proinflamasi, NO, dan ROS. Walau bagaimanapun, makrofaj M2 menggalakkan pembaikan tisu dan pengeluaran kolagen dan menghalang aktiviti imun. Dalam kajian terdahulu, makrofaj M1 dan M2 terlibat dalam patogenesis fibrosis buah pinggang. Semasa fibrosis buah pinggang, laluan NF-jB diaktifkan, yang boleh mengaktifkan dan memodulasi makrofaj M1. Faktor pengawalseliaan interferon/transduser isyarat dan pengaktif transkripsi (IRF/STAT, melalui STAT6) laluan isyarat, diaktifkan oleh IL-4 dan IL-13, boleh mengubah makrofaj kepada fenotip M2 [157-159]. H2S boleh mengurangkan penyusupan makrofaj M1 dan M2 dengan ketara dengan menghalang NF–jB dan IL–4/ STAT6. Di samping itu, pengaktifan laluan NF-jB dan IL-4 / STAT6 dalam tikus yang disebabkan UUO disertai dengan pengaktifan inflammasom NLRP3. Penderma H2S menyekat pengaktifan inflammasom NLRP3, yang mungkin menyumbang kepada kesan anti-radang dan antifibrotik H2S [145].
Berdasarkan peranan positif H2S dalam penyakit buah pinggang obstruktif, H2S mungkin merupakan terapi berpotensi baru terhadap kecederaan buah pinggang yang disebabkan oleh halangan kencing [160].

Serbuk cistanche
Kesimpulan
Dalam kajian ini, kami telah membincangkan secara komprehensif peranan H2S dalam penyakit buah pinggang, terutamanya DN, dan meneroka mekanisme molekul yang berkaitan. DN adalah salah satu komplikasi DM yang paling serius, dan banyak kelas ubat tersedia untuk rawatan, tetapi keberkesanannya masih terhad. H2S boleh mengawal autofagi, apoptosis, OS, dan keradangan melalui berbilang laluan isyarat, menyediakan sasaran baharu untuk rawatan. Walau bagaimanapun, berbanding dengan perencat kotransporter 2 natrium-glukosa, yang membentuk kelas baru ubat penurun glukosa darah yang menyekat penyerapan semula glukosa buah pinggang dan mempunyai kesan perlindungan pada buah pinggang, H2S mungkin mempunyai keberkesanan ringan dalam menurunkan glukosa [172]. Di samping itu, peranan H2S dalam AKI, seperti AKI yang berkaitan dengan sepsis dan AKI yang disebabkan oleh dadah, tidak jelas. Penyelidikan mengenai topik tersebut akan memajukan dan meluaskan pemahaman kita secara kritis tentang potensi terapeutik H2S dalam penyakit buah pinggang.
Rujukan
[83] Migdalis I, Leslie D, Mavrogiannaki A, et al. Diabetes mellitus 2014. Int J Endokrinol. 2015;2015:845759.
[84] Stenvinkel P. Penyakit buah pinggang kronik: keutamaan kesihatan awam dan petanda penyakit kardiovaskular pramatang. J Intern Med. 2010;268(5):456–467.
[85] Stanton RC. Tekanan oksidatif dan penyakit buah pinggang diabetes. Curr Diab Rep. 2011;11(4):330–336.
[86] Tesch GH, Lim AK. Pandangan terkini tentang kecederaan buah pinggang diabetik daripada model tetikus db/db nefropati diabetik jenis 2. Am J Physiol Fisiol Renal. 2011; 300(2):F301–10.
[87] Lim AK, Tesch GH. Keradangan dalam nefropati diabetik. Perantara Inflamm. 2012;2012:146154.
[88] Kamiyama M, Zsombok A, Kobori H. Angiotensinogen kencing sebagai biomarker awal novel pengaktifan sistem renin-angiotensin intrarenal dalam diabetes jenis 1 eksperimen. J Pharmacol Sci. 2012;119(4): 314–323.
[89] Jain SK, Bull R, Rains JL, et al. Tahap rendah hidrogen sulfida dalam darah pesakit diabetes dan tikus yang dirawat streptozotocin menyebabkan keradangan vaskular. Isyarat Redoks Antioksida. 2010;12(11):1333–1337.
[90] van den Born JC, Frenay AR, Bakker SJ, et al. Kepekatan sulfat kencing yang tinggi dikaitkan dengan pengurangan risiko perkembangan penyakit buah pinggang dalam diabetes jenis 2. Nitrik Oksida. 2016;55-56:18–24.
[91] Li H, Feng SJ, Zhang GZ, et al. Korelasi kepekatan hidrogen sulfida yang lebih rendah dengan aterosklerosis dalam pesakit hemodialisis kronik dengan nefropati diabetik. Pemurni Darah. 2014;38(3–4):188–194.
[92] Xue R, Hao DD, Sun JP, et al. Rawatan hidrogen sulfida menggalakkan pengambilan glukosa dengan meningkatkan sensitiviti reseptor insulin dan memperbaiki lesi buah pinggang dalam diabetes jenis 2. Isyarat Redoks Antioksida. 2013;19(1): 5–23.
[93] Sun HJ, Xiong SP, Cao X, et al. Sulfhidrasi pengantaraan polysulfide SIRT1 menghalang nefropati diabetik dengan menekan fosforilasi dan asetilasi p65 NF-jB dan STAT3. Biol Redoks. 2021;38:101813.
[94] Yu Y, Xiao L, Ren Z, et al. Penurunan cystathionine b-synthase yang disebabkan oleh glukosa menjadi pengantara kecederaan buah pinggang. Faseb J. 2021;35(5):e21576.
[95] Hussain Lodhi A, Ahmad FU, Furwa K, et al. Peranan tekanan oksidatif dan pengurangan hidrogen sulfida endogen dalam nefropati diabetik. Dadah Des Devel Ther. 2021;15:1031–1043.
[96] Juin SK, Pushpakumar S, Sen U. GYY4137 mengawal pusing ganti matriks ekstraselular dalam buah pinggang diabetes dengan memodulasi isyarat reseptor X retinoid. Biomolekul. 2021;11(10):1477.
[97] Elbassuoni EA, ffziz NM, Habeeb WN. Peranan pengaktifan saluran K(ffTP) pada kesan renoprotektif akibat hidrogen sulfida pada nefropati diabetik. J Sel Fisiol. 2020;235(6):5223–5228.
[98] Qian X, Li X, Ma F, et al. Sebatian pelepas hidrogen sulfida baru, S-propargyl-cysteine, menghalang nefropati diabetes yang disebabkan oleh STZ. Biochem Biophys Res Commun. 2016;473(4):931–938.
[99] Ahmed HH, Taha FM, Omar HS, et al. Hidrogen sulfida memodulasi SIRT1 dan menyekat tekanan oksidatif dalam nefropati diabetik. Biokim Sel Mol. 2019; 457(1–2):1–9.
[100] Li Y, Li L, Zeng O, et al. H(2)S meningkatkan fibrosis buah pinggang dalam tikus diabetes yang disebabkan oleh STZ dengan memperbaiki ekspresi TGF-b1. Ren Fail. 2017;39(1):265–272.
[101] Kumawat M, Sharma TK, Singh I, et al. Enzim antioksidan dan peroksidasi lipid dalam pesakit diabetes mellitus jenis 2 dengan dan tanpa nefropati. N Am J Med Sci. 2013;5(3):213–219.
[102] Mima A. Keradangan dan tekanan oksidatif dalam nefropati diabetik: pandangan baharu tentang perencatannya sebagai sasaran terapeutik baharu. J Diabetes Res. 2013;2013: 248563.
[103] Eid AA, Gorin Y, Fagg BM, et al. Mekanisme kecederaan podosit dalam diabetes: peranan cytochrome P450 dan NADPH oxidases. kencing manis. 2009;58(5): 1201–1211.
[104] Zhang MH, Feng L, Zhu MM, et al. Aktiviti antioksida dan anti-radang paeoniflorin dan oxypaeoniflora pada kerosakan sel mesangial yang disebabkan oleh AGEs. Planta Med. 2013;79(14):1319–1323.
[105] Safar MM, Abdelsalam RM. Penderma H2S melemahkan nefropati diabetik pada tikus: modulasi status oksidan dan laluan poliol. Pharmacol Rep. 2015;67(1): 17–23.
[106] Yang R, Liu XF, Ma SF, et al. Kesan perlindungan hidrogen sulfida pada buah pinggang tikus diabetes jenis 1. Zhongguo Ying Yong Sheng Li Xue Za Zhi. 2016; 32(2):181–184.
[107] Wei Y, Gong J, Thimmulappa RK, et al. Nrf2 bertindak sel secara autonomi dalam endothelium untuk mengawal pembentukan sel hujung dan percabangan vaskular. Proc Natl Acad Sci USA. 2013;110(41):E3910–8.
[108] Zheng H, Whitman SA, Wu W, et al. Potensi terapeutik pengaktif Nrf2 dalam nefropati diabetes yang disebabkan oleh streptozotocin. kencing manis. 2011;60(11): 3055–3066.
[109] Xie L, Gu Y, Wen M, et al. Hidrogen sulfida mendorong Keap1 S-sulfhidrasi dan menyekat aterosklerosis yang dipercepatkan diabetes melalui pengaktifan Nrf2. kencing manis. 2016;65(10):3171–3184.
[110] Zhou X, Feng Y, Zhan Z, et al. Hidrogen sulfida mengurangkan nefropati diabetik dalam model tikus diabetes yang disebabkan oleh streptozotocin. J Biol Chem. 2014; 289(42):28827–28834.
[111] Lee HJ, Lee DY, Mariappan MM, et al. Hidrogen sulfida menghalang ekspresi NADPH oksidase 4 yang disebabkan oleh glukosa tinggi dan peningkatan matriks dengan merekrut sintase nitrik oksida teraruh dalam sel epitelium tiub proksimal buah pinggang. J Biol Chem. 2017;292(14):5665–5675.
[112] Gorin Y, Blok K. Nox4 dan nefropati diabetik: dengan rakan seperti ini, siapa yang memerlukan musuh? Percuma Radic Biol Med. 2013;61:130–142.
[113] Lee MJ, Feliers D, Mariappan MM, et al. Peranan untuk kinase protein diaktifkan AMP dalam hipertrofi buah pinggang yang disebabkan oleh diabetes. Am J Physiol Fisiol Renal. 2007; 292(2):F617–27.
[114] Lee HJ, Mariappan MM, Feliers D, et al. Hidrogen sulfida menghalang sintesis protein matriks yang disebabkan oleh glukosa tinggi dengan mengaktifkan kinase protein diaktifkan AMP dalam sel epitelium buah pinggang. J Biol Chem. 2012;287(7): 4451–4461.
[115] Levine B, Kroemer G. Autophagy dalam patogenesis penyakit. sel. 2008;132(1):27–42.
[116] Li L, Tan J, Miao Y, et al. ROS dan autophagy: interaksi dan mekanisme pengawalseliaan molekul. Sel Mol Neurobiol. 2015;35(5):615–621.
[117] Liu J, Wu J, Sun A, et al. Hidrogen sulfida mengurangkan autofagi yang disebabkan glukosa/palmitat tinggi dalam sel endothelial oleh laluan isyarat Nrf2-ROS-AMPK. Biosci Sel. 2016;6(1):33.
[118] Fernandez-Sanchez A, Madrigal-Santillan E, Bautista M, et al. Keradangan, tekanan oksidatif, dan obesiti. Int J Mol Sci. 2011;12(5):3117–3132.
[119] Wada J, Makino H. Keradangan dan patogenesis nefropati diabetik. Clin Sci (Lond). 2013; 124(3):139–152.
[120] Wang W, Sun W, Cheng Y, et al. Peranan sirtuin-1 dalam nefropati diabetik. J Mol Med. 2019;97(3): 291–309.
[121] Naduk-Kik J, Hrabec E. Peranan metalloproteinase matriks dalam patogenesis diabetes mellitus dan perkembangan retinopati diabetik. Postepy Hig Med Dosw. 2008;62:442–450.
[122] Kundu S, Pushpakumar SB, Tyagi A, et al. Kekurangan hidrogen sulfida dan pembentukan semula buah pinggang diabetes: peranan matriks metalloproteinase-9. Am J Physiol Endokrinol Metab. 2013;304(12):E1365–78.
[123] Patel S, Rauf A, Khan H, et al. Renin-angiotensin aldosteron (RAAS): sistem di mana-mana untuk homeostasis dan patologi. Biomed Pharmacother. 2017;94:317–325.
[124] Thomas MC, Brownlee M, Susztak K, et al. Penyakit buah pinggang kencing manis. Nat Rev Dis Primers. 2015;1:15018.
[125] Bermejo S, Garcıa CO, Rodrıguez E, et al. Sekatan sistem renin-angiotensin-aldosteron pada pesakit dengan penyakit buah pinggang diabetes lanjutan. Nefrologia. 2018;38(2):197–206.
[126] Li Z, Organ CL, Kang J, et al. Hidrogen sulfida melemahkan isyarat patologi renin-angiotensin dan aldosteron untuk memelihara fungsi buah pinggang dan meningkatkan toleransi senaman dalam kegagalan jantung. JACC Basic Transl Sci. 2018;3(6):796–809.
[127] Xue H, Yuan P, Ni J, et al. H(2)S menghalang pengaktifan sistem renin-angiotensin intrarenal akibat hiperglikemia melalui pengecilan penjanaan spesies oksigen reaktif. PLoS One. 2013;8(9):e74366.
[128] Hart PD, Bakris GL. Nefropati hipertensi: cadangan pencegahan dan rawatan. Pakar Opin Pharmacother. 2010;11(16):2675–2686.
[129] Udani S, Lazich I, Bakris GL. Epidemiologi penyakit buah pinggang hipertensi. Nat Rev Nephrol. 2011;7(1): 11–21.
[130] Seccia TM, Caroccia B, Cal o LA. Nefropati hipertensi. Bergerak daripada mekanisme patogenetik klasik kepada yang baru muncul. J Hipertensi. 2017;35(2):205–212.
[131] Bidani AK, Griffin KA. Patofisiologi kerosakan buah pinggang hipertensi: implikasi untuk terapi. Hipertensi. 2004;44(5):595–601.
[132] Yang G, Wu L, Jiang B, et al. H2S sebagai vasorelaxant fisiologi: hipertensi pada tikus dengan penghapusan cystathionine gamma-lyase. Sains. 2008;322(5901): 587–590.
[133] Roy A, Khan AH, Islam MT, et al. Saling kebergantungan cystathionine c-lyase dan cystathionine b-synthase dalam peraturan tekanan darah yang disebabkan oleh hidrogen sulfida pada tikus. Am J Hipertensi. 2012;25(1):74–81.
[134] Zhao W, Wang R. H(2)S yang disebabkan oleh vasorelaksasi dan mekanisme selular dan molekul yang mendasari. Am J Physiol Heart Circ Physiol. 2002;283(2):H474–80.
[135] Kasar B, Pawlak M, Lefebvre P, et al. PPAR dalam T2DM yang disebabkan obesiti, dislipidemia, dan NAFLD. Nat Rev Endokrinol. 2017;13(1):36–49.
[136] Toral M, Romero M, Perez-Vizcaıno F, et al. Kesan antihipertensi pengaktifan reseptor-b/d peroksisom proliferator diaktifkan. Am J Physiol Heart Circ Physiol. 2017;312(2): H189–H200.
[137] Predmore BL, Julian D, Cardounel AJ. Hidrogen sulfida meningkatkan pengeluaran nitrik oksida daripada sel endothelial melalui mekanisme yang bergantung kepada akt. Fisiol Depan. 2011;2:104.
[138] Xiao L, Dong JH, Teng X, et al. Hidrogen sulfida meningkatkan disfungsi endothelial dalam hipertensi dengan mengaktifkan reseptor teraktifkan peroksisom proliferator Delta/endothelial nitric oxide synthase signaling. J Hipertensi. 2018;36(3):651–665.
[139] Ji W, Liu S, Dai J, et al. Hidrogen sulfida mempertahankan terhadap risiko kardiovaskular hipertensi yang disebabkan oleh Nw-nitro-L-argininemethyl ester pada tikus melalui laluan nitrik oksida/endothelial nitric oxide synthase. Chin Med J. 2014;127(21):3751–3757.
[140] Ali MY, Ping CY, Mok YY, et al. Peraturan oksida nitrik vaskular in vitro dan in vivo; peranan baru untuk hidrogen sulfida endogen? Br J Pharmacol. 2006;149(6):625–634.
[141] Ruiz-Ortega M, Esteban V, Ruperez M, et al. Keradangan yang disebabkan oleh hipertensi buah pinggang dan vaskular: peranan angiotensin II. Curr Opin Nephrol Hypertens. 2006;15(2):159–166.
[142] Liao TD, Yang XP, Liu YH, et al. Peranan keradangan dalam perkembangan kerosakan buah pinggang dan disfungsi dalam hipertensi yang disebabkan oleh angiotensin II. Hipertensi. 2008;52(2):256–263.
[143] Al-Magableh MR, Kemp-Harper BK, Hart JL. Rawatan hidrogen sulfida mengurangkan tekanan darah dan tekanan oksidatif dalam tikus hipertensi yang disebabkan oleh angiotensin II. Hipertensi Re. 2015;38(1):13–20.
[144] Stevens S. Penyakit buah pinggang obstruktif. Nurs Clin North Am. 2018;53(4):569–578.
[145] Zhou Y, Zhu X, Wang X, et al. H(2)S mengurangkan kecederaan buah pinggang dan fibrosis sebagai tindak balas kepada halangan ureter unilateral dengan mengawal penyusupan makrofaj melalui perencatan isyarat NLRP3. Exp Cell Res. 2020; 387(1):111779.
[146] Jung KJ, Jang HS, Kim JI, et al. Penglibatan laluan hidrogen sulfida dan homocysteine transsulfuration dalam perkembangan fibrosis buah pinggang selepas halangan ureter. Biochim Biophys Acta. 2013; 1832(12):1989–1997.
[147] Song K, Wang F, Li Q, et al. Hidrogen sulfida menghalang fibrosis buah pinggang nefropati obstruktif. Buah Pinggang Int. 2014;85(6):1318–1329.
[148] Lin S, Visram F, Liu W, et al. GYY4137, penderma hidrogen sulfida yang melepaskan perlahan, memperbaiki kerosakan buah pinggang yang berkaitan dengan uropati obstruktif kronik. J Urol. 2016;196(6):1778–1787.
[149] Lin S, Lian D, Liu W, et al. Terapi harian dengan penderma H(2)S GYY4137 yang mengeluarkan perlahan membolehkan pemulihan fungsi awal dan memulihkan kecederaan buah pinggang yang berkaitan dengan halangan kencing. Nitrik Oksida. 2018;76: 16–28.
[150] Jiang D, Zhang Y, Yang M, et al. Hidrogen sulfida eksogen menghalang kerosakan buah pinggang berikutan halangan ureter unilateral. Neurourol Urodyn. 2014; 33(5):538–543.
[151] Dursun M, Otunctemur A, Ozbek E, et al. Kesan perlindungan hidrogen sulfida pada kecederaan buah pinggang dalam halangan ureter unilateral eksperimen. Int Braz j Urol. 2015;41(6):1185–1193.
[152] Chen Q, Yu S, Zhang K, et al. H2S eksogen menghalang autophagy dalam sel tubul renal tetikus halangan ureter unilateral dengan mengawal selia laluan isyarat ROS-AMPK. Biokim Fisiol Sel. 2018;49(6): 2200–2213.
[153] Song K, Li Q, Yin XY, et al. Hidrogen sulfida: calon terapeutik untuk penyakit fibrotik? Sel Oksid Med Longev. 2015;2015:458720.
[154] Duni A, Liakopoulos V, Roumeliotis S, et al. Tekanan oksidatif dalam patogenesis dan evolusi penyakit buah pinggang kronik: menguraikan benang Ariadne. Int J Mol Sci. 2019;20(15):3711.
[155] Xu W, Chen J, Lin J, et al. H2S eksogen melindungi sel jantung H9c2 daripada kecederaan dan keradangan yang disebabkan oleh glukosa tinggi dengan menghalang pengaktifan laluan NF-jB dan IL-1b. Int J Mol Med. 2015;35(1):177–186.
[156] Orecchioni M, Ghosheh Y, Pramod AB, et al. Polarisasi makrofaj: tandatangan gen yang berbeza dalam M1(LPSþ) lwn. Klasik dan M2(LPS-) lwn. Front Immunol. 2019;10:1084.
[157] Wynn TA, Vannella KM. Makrofaj dalam pembaikan tisu, penjanaan semula, dan fibrosis. Kekebalan. 2016;44(3): 450–462.
[158] Chakarov S, Lim HY, Tan L, et al. Dua populasi makrofaj interstisial yang berbeza wujud bersama merentas tisu dalam relung sub-tisuler tertentu. Sains. 2019;363(6432): aau0964.
[159] Martinez FO, Helming L, Gordon S. Pengaktifan alternatif makrofaj: perspektif fungsi imunologi. Annu Rev Immunol. 2009;27:451–483.
[160] Lin S, Juriasingani S, Sener A. Adakah hidrogen sulfida merupakan terapi baru yang berpotensi untuk mencegah kerosakan buah pinggang semasa halangan ureter? Nitrik Oksida. 2018;73: 15–21.
Jianan Feng, Xiangxue Lu, Han Li, dan Shixiang Wang
Jabatan Nefrologi, Hospital Beijing Chao-Yang, Universiti Perubatan Capital, Beijing, China






