Bahagian Satu Genetik Penyakit Buah Pinggang: Peranan Tidak Dijangka Gangguan Jarang
Jun 09, 2023
Abstrak
Beratus-ratus punca genetik yang berbeza bagi penyakit buah pinggang kronik kini diiktiraf, dan walaupun jarang berlaku secara individu, diambil bersama-sama ia merupakan penyumbang penting kepada keadaan dewasa dan pediatrik. Pendekatan genetik tradisional sangat bergantung pada mengenal pasti keluarga besar dengan berbilang ahli yang terjejas dan menjadi asas untuk mengenal pasti penyakit buah pinggang genetik. Dengan peningkatan penggunaan penjujukan selari secara besar-besaran dan penambahbaikan kepada imputasi genotip, kami boleh menganalisis varian yang jarang berlaku dalam kohort besar individu yang tidak berkaitan, yang membawa kepada penjagaan pesakit yang diperibadikan dan kemajuan penyelidikan yang ketara. Kajian ini menilai sumbangan gangguan jarang berlaku kepada penjagaan pesakit dan kajian penyakit buah pinggang genetik dan menyerlahkan kemajuan utama yang menggunakan teknik baharu untuk meningkatkan keupayaan kami mengenal pasti persatuan penyakit gen baharu.
Kata kunci
penyakit buah pinggang genetik, analisis runtuh, ubat ketepatan, penjujukan selari secara besar-besaran, genomik, penyakit buah pinggang kronik

Klik sini untuk tahuapakah faedah Cistanche
PENGENALAN
Penyakit buah pinggang kronik (CKD) adalah keadaan kompleks yang merangkumi banyak penyakit individu yang dicirikan oleh keabnormalan dalam struktur atau fungsi buah pinggang (1). Di peringkat global, penyakit buah pinggang adalah perkara biasa, dengan anggaran prevalens 9 peratus, dan merupakan penyumbang utama kepada morbiditi dan kematian (2). Sama seperti penyakit biasa yang lain, CKD mempunyai kebolehwarisan yang agak tinggi, dengan anggaran kebolehwarisan pengertian luas antara 19 peratus hingga 54 peratus bergantung pada biomarker yang digunakan (3–5).
Genetic variation can be broadly dichotomized into common variants, present in more than 1% of the alleles of the population [a minor allele frequency (MAF) of >0.01] dan varian jarang berlaku (MAF<0.01) (6–8). The role of common variants in kidney disease has been assessed using genome-wide association studies (GWAS), which have explained only 20% of an estimated 54% heritability in creatinine-based estimated glomerular filtration rate (4). On the other side of the spectrum, rare pathogenic variants are responsible for most Mendelian (monogenic) diseases. There are over 600 Mendelian forms of kidney disease, responsible for 50% of childhood-onset kidney disease; the majority of the causative variants are very rare or private within a specific family (9, 10). Although present at a lower frequency, Mendelian kidney diseases are identified in approximately 10% of adult patients, with the specific diagnostic yield of testing varying based on the individual's type of kidney disease, family history, age at onset, and extra-renal manifestations (11). Similar to pediatric cases, rare and private variants drive most diagnoses in adult cases. The data on the impact of rare disorders in CKD are now emerging and are consistent with analyses of other complex traits, which have demonstrated that a significant amount of missing heritability is explained by rare protein-altering variants that are not well captured by current genotyping and imputation techniques but can be analyzed using massively parallel sequencing of the exome (exome sequencing, ES) or genome (12, 13).
Varian jarang yang terlibat dalam penyakit buah pinggang adalah pelbagai dalam kelas mereka, warisan, gen yang terjejas, dan fenotip klinikal. Sebagai contoh, variasi struktur yang jarang berlaku dan variasi dalam nombor salinan gen telah dikaitkan dengan perkembangan anomali kongenital buah pinggang dan saluran kencing (CAKUT), dan varian nukleotida tunggal dan sisipan dan penghapusan kecil (indels) telah dikaitkan dengan penyakit buah pinggang. merentasi spektrum fenotip (14, 15). Varian somatik yang jarang berlaku telah dikaitkan sebagai serangan kedua dalam perkembangan sista dalam penyakit buah pinggang polikistik dominan autosomal (ADPKD) dan sebagai varian pemacu dalam hematopoiesis klonal potensi tak tentu (CHIP), keadaan bukan malignan yang berkaitan dengan usia yang boleh menyebabkan peningkatan. risiko kegagalan buah pinggang dan komplikasi CKD (16, 17). Varian mozek yang jarang ditemui juga memberi kesan kepada keterukan sindrom Alport berkaitan X, mencadangkan kerumitan lanjut dalam menentukan kesan varian (18).
Dalam ulasan ini, kami menerangkan peranan variasi yang jarang dimainkan dalam genetik penyakit buah pinggang. Kami mengkaji tempat utama mereka dalam kajian diagnostik, termasuk implikasi untuk penjagaan pesakit dan penggunaan ujian genetik dalam ramalan dan rawatan. Kami kemudian meneroka pendekatan biasa yang digunakan untuk mengenal pasti dan mengesahkan persatuan varian baru yang jarang berlaku dengan penyakit. Kami membuat kesimpulan dengan penyiasatan set data yang besar dan penyepaduan data klinikal daripada rekod kesihatan elektronik, yang menawarkan peluang untuk menilai kesan genetik pada skala yang sebelum ini mustahil.

Suplemen cistanche
TETAPAN DIAGNOSTIK KLINIKAL
Penyakit buah pinggang genetik adalah istilah umum yang menangkap ratusan gangguan yang jarang berlaku dengan punca genetik yang dikenal pasti. Sehingga kini, lebih 600 gangguan monogenik dengan fenotip buah pinggang dan urologi telah dikenalpasti (Rajah 1) (19). Hampir semua keadaan genetik ini dilihat dalam kurang daripada 1 dalam 2,000 orang, tetapi secara kumulatif mereka mewakili punca kegagalan buah pinggang yang kelima paling biasa (20). Walaupun beberapa gangguan monogenik menyumbang sebahagian besar daripada kes, kes selebihnya adalah disebabkan oleh sejumlah besar gangguan yang jarang berlaku. Ekor panjang dalam pengedaran penyakit buah pinggang monogenik ini mempunyai implikasi penting untuk algoritma diagnostik klinikal dan usaha penemuan gen. Beberapa kajian diagnostik telah dilakukan untuk menentukan dengan lebih baik hasil diagnostik dan implikasi klinikal ujian genetik dalam populasi pesakit yang berbeza dengan penyakit buah pinggang. Salah satu penemuan utama dalam kajian ini ialah majoriti varian patogen yang dikenal pasti sangat jarang berlaku, dengan MAF maksimum (maks) kurang daripada 1 × 10–4, atau peribadi dalam satu keluarga.

1. Keadaan Pediatrik
Penyakit genetik pada asalnya dianggap kebanyakannya pediatrik, jadi kajian diagnostik awal memberi tumpuan kepada menilai pesakit pediatrik (11, 21). Satu kajian sedemikian menggunakan ES untuk menilai 187 pesakit kanak-kanak dengan sindrom nefrotik tahan steroid dan mengenal pasti punca genetik dalam 49 (26 peratus) kes dan 77 varian diagnostik (22). Menariknya, walaupun pewarisan resesif syarat ini, semua varian adalah sangat jarang berlaku; 32 (42 peratus ) tidak hadir dalam literatur, 39 (51 peratus ) tidak hadir dalam Exome Aggregation Consortium (ExAC), dan 25 lagi (32 peratus ) mempunyai MAF maks kurang daripada 1 × 10− 4. Satu pengecualian ialah sindrom nefrotik tahan steroid kanak-kanak yang disebabkan oleh varian dalam NPHS2, yang menawarkan contoh menarik tentang interaksi varian biasa dan jarang berlaku dalam penyakit ini. NPHS2 p.R229Q ialah varian patogenik yang paling biasa dikenal pasti dalam populasi pesakit ini, dengan MAF maksimum dalam ExAC sebanyak 0.029. Walau bagaimanapun, varian NPHS2 p.R229Q tidak menyebabkan penyakit apabila terdapat dalam keadaan homozigot dan hanya patogenik apabila dipasangkan dengan varian NPHS2 tertentu yang jarang ditemui (23). Dalam kajian yang dipetik, varian memudaratkan yang ditemui dalam trans kepada NPHS2 p.R229Q dalam individu yang terjejas sentiasa jarang berlaku dan selalunya peribadi, dengan NPHS2 p.E264Q adalah yang paling biasa dalam ExAC, mempunyai MAF maksimum 0.003. Begitu juga, penilaian punca genetik CAKUT dalam 232 keluarga mengenal pasti 32 varian penyebab yang berbeza dalam 32 kes (14 peratus) yang mempengaruhi 22 gen dengan 16 (50 peratus) daripada varian ini tidak terdapat dalam literatur dan 28 (88 peratus) sangat jarang atau tidak hadir. daripada Pangkalan Data Pengagregatan Genom (gnomAD) (24).
2. Meluaskan kepada Pesakit Dewasa
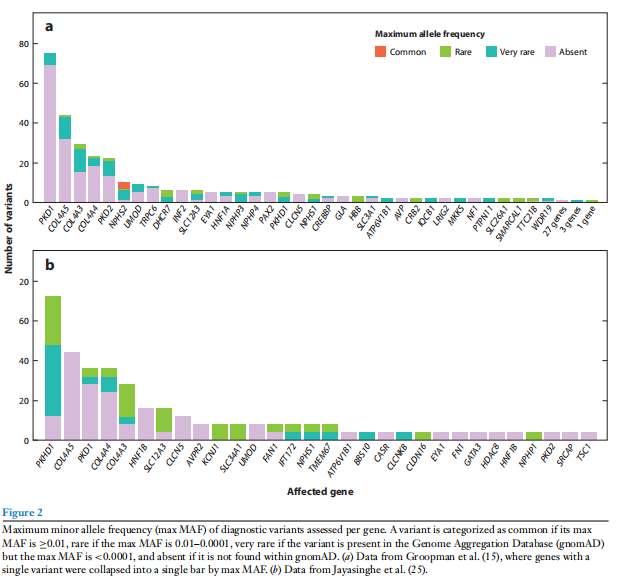
ES telah digunakan untuk menilai populasi pesakit yang pelbagai dengan penyakit buah pinggang, termasuk individu dengan penyakit dewasa. Kajian terbesar untuk berbuat demikian termasuk 3,315 individu dengan CKD dari sebarang sebab, di mana 2,144 telah mengalami kegagalan buah pinggang dan 2,837 adalah orang dewasa pada kemasukan kajian (15). Kajian ini mengenal pasti diagnosis molekul dalam 307 individu (9.1 peratus) yang membawa kepada diagnosis 66 penyakit buah pinggang Mendelian yang berbeza. Kajian itu mengenal pasti 343 varian diagnostik, yang mana 340 99 peratus ) jarang ditemui dalam gnomAD. Kebanyakan varian sama ada sangat jarang berlaku, dengan MAF maksimum kurang daripada 1 × 10−4 (n=84, 24 peratus ), atau persendirian (n=229, 67 peratus ) (Rajah 2a).
3. Kesan Diagnosis Genetik
Salah satu penemuan utama kajian diagnostik ialah kebanyakan diagnosis genetik memberi kesan secara langsung kepada penjagaan pesakit, walaupun dengan bilangan rawatan yang disasarkan yang terhad pada masa ini. Groopman et al. (15) mendapati bahawa diagnosis genetik membawa kepada kesan klinikal dalam 89 peratus kes, termasuk dalam 76 peratus kes di mana penyakit buah pinggang genetik disyaki sebelum ujian. Kesan klinikal ini dinilai secara retrospektif dan terdiri daripada memaklumkan prognosis kepada mengubah keputusan pemindahan dan rawatan. Yang penting, diagnosis genetik pada pesakit dengan CKD yang etiologi tidak diketahui menjelaskan punca penyakit buah pinggang dalam semua kes, membawa implikasi prognostik untuk 77 peratus, memulakan penjagaan subkepakaran yang disasarkan untuk 77 peratus, dan menukar terapi untuk 62 peratus. Data prospektif yang menyokong utiliti klinikal ujian genetik untuk penyakit buah pinggang baru-baru ini diterbitkan pada 204 pesakit yang disyaki penyakit buah pinggang genetik yang menjalani ES. Kesan klinikal langsung telah dilaporkan untuk 47 (59 peratus) proband dengan diagnosis genetik dan 73 (91 peratus) keluarga (25). Kesan klinikal termasuk pencegahan 10 biopsi buah pinggang, perubahan kepada pelan rawatan dalam 16 kes, dan pengawasan yang diubah dalam 35 yang sekali lagi didorong oleh varian yang jarang berlaku (Rajah 2b).

Ekstrak cistanche
4. Prognosis
Kebolehubahan dalam persembahan klinikal bentuk genetik penyakit buah pinggang telah merumitkan penyediaan maklumat prognostik kepada pesakit, walaupun punca genetik dikenal pasti. Selain itu, majoriti varian patogenik yang dikaitkan dengan penyakit buah pinggang adalah sangat jarang atau peribadi dalam keluarga, yang mengehadkan keupayaan kami untuk memberikan prognosis berdasarkan varian individu. Namun begitu, korelasi genotip-fenotip telah menjadi sebahagian daripada genetik manusia sejak penubuhannya, selalunya menggunakan ciri varian yang boleh digeneralisasikan seperti jenis kesan pada protein, sifat asid amino yang diubah, atau kedudukan varian dalam protein. Dalam nefrologi, dua aplikasi paling matang pendekatan ini melihat ADPKD dan sindrom Alport. Bagi pesakit dengan ADPKD, sistem pemarkahan PROPKD (meramalkan hasil buah pinggang dalam penyakit buah pinggang polikistik) telah dibangunkan dan disahkan untuk meramalkan umur median individu pada kegagalan buah pinggang dengan menyepadukan data klinikal dan varian (26). Varian pemangkasan dalam PKD1 membawa risiko kegagalan buah pinggang yang paling tinggi, diikuti oleh varian PKD1 yang tidak dipotong, kemudian varian dalam PKD2, dan nampaknya juga bahawa tidak memotong sisipan dalam bingkai dan pemadaman dalam PKD1 yang mengubah panjang protein membawa risiko yang lebih tinggi daripada varian missense ( 27). Begitu juga, bagi pesakit dengan sindrom Alport, varian karut membawa prognosis yang paling teruk manakala varian splicing dan missense menggambarkan fenotip pertengahan dan ringan, masing-masing. Faktor lain seperti kedudukan varian dalam gen, kedudukannya berbanding gangguan bukan kolagen, dan penggantian asid amino juga telah ditunjukkan untuk memberi kesan kepada prognosis pesakit (28-30). Alat masa depan juga mungkin termasuk maklumat ramalan daripada kedua-dua varian biasa dan jarang untuk meningkatkan kuasa mereka (31). Ketersediaan set data yang lebih besar akan membolehkan penyepaduan lebih banyak varian, dan idealnya lebih banyak keluarga yang berbeza dengan varian yang sama, ke dalam pembangunan alat prognostik yang teguh untuk membolehkan ramalan yang lebih baik. Alat sedemikian boleh memberi kesan ketara kepada ujian klinikal, kerana peserta boleh distratifikasi berdasarkan perkembangan jangkaan penyakit mereka.

Pil cistanche
5. Rawatan
Kajian diagnostik telah menunjukkan bahawa mendapatkan diagnosis genetik boleh memberi kesan langsung kepada rawatan (Jadual 1). Contohnya termasuk penggunaan suplemen koenzim Q10 (CoQ10) dos tinggi untuk pesakit sindrom nefrotik dan varian diagnostik dalam laluan CoQ10 (COQ2, COQ6, ADCK2/COQ8B, PDSS2, MTTL1) dan penggunaan perencat xanthine oxidase untuk pesakit APRT (adenine phosphoribosyltransferase) kekurangan (32, 33). Diagnosis genetik boleh mengehadkan pendedahan kepada rawatan yang tidak berkesan; contohnya, apabila punca genetik sindrom nefrotik dikenal pasti, imunosupresi biasanya tidak digunakan, kerana majoriti kes sindrom nefrotik genetik tidak akan bertindak balas dan rawatan ini membawa risiko yang ketara (34). Kajian masa depan harus menilai faedah mengelakkan kesan buruk, seperti mengurangkan jangkitan dan risiko kanser daripada mengehadkan imunosupresi akibat ujian genetik. Selain itu, keupayaan untuk mengesan pesakit yang tidak didiagnosis dengan penyakit monogenik boleh membantu dengan stratifikasi risiko dalam ujian klinikal untuk mengoptimumkan kuasa dan mengurangkan pendedahan kepada kesan sampingan.

Matlamat utama adalah untuk membangunkan rawatan kuratif. Salah satu contoh paling maju dalam nefrologi ialah aplikasi terapi gen untuk penyakit Fabry (35). Penyakit Fabry disebabkan oleh lebih 1,000 varian berbeza dalam gen GLA, paling jarang berlaku atau persendirian, yang membawa kepada pengurangan aktiviti -galactosidase A dan pengumpulan glikosfingolipid (36). Rawatan standard untuk penyakit ini ialah terapi penggantian enzim (ERT), yang memerlukan infusi biasa dan boleh membawa kepada antibodi anti-ubat yang mengehadkan rawatan. Walau bagaimanapun, dalam kajian keselamatan perintis, lima lelaki dengan penyakit Fabry klasik disebabkan oleh varian missense yang sangat jarang yang dirawat secara stabil dengan ERT telah dirawat dengan terapi gen (35). Mereka menjalani terapi gen ex vivo yang dimediasi oleh lentivirus di mana sel stem/progenitor hematopoietik ditransduksi dengan gen GLA berfungsi, kemudian diperkenalkan semula melalui pemindahan sel stem hematopoietik autologous. Pesakit ini menunjukkan aktiviti normalisasi leukosit -galactosidase A yang tahan lama dan tahap glikosfingolipid yang stabil yang membolehkan tiga (60 peratus) daripada mereka menghentikan ERT mereka, dengan profil kejadian buruk yang munasabah. Kajian ini memberi kami harapan bahawa dengan penambahbaikan lanjut, rawatan kuratif mungkin tersedia untuk lebih ramai pesakit kami.
Penyakit Fabry juga menyediakan contoh lain terapi peribadi yang menarik, termasuk terapi pendamping dan keputusan rawatan untuk pesakit wanita. Mekanisme biasa penyakit dalam keadaan ini ialah pemerdagangan protein yang diubah yang membawa kepada pengurangan aktiviti enzim. Migalastat ialah molekul pendamping yang memulihkan fungsi enzim dan menunjukkan keberkesanan klinikal yang serupa dengan ERT dalam 35-50 peratus individu dengan varian yang boleh diterima tetapi tidak mempunyai kesan pada individu dengan varian yang tidak boleh diterima (37, 38). Kekhususan varian ini menjadikan ujian genetik sebagai langkah utama dalam mengoptimumkan terapi untuk pesakit dengan penyakit Fabry. Sudah lama difikirkan bahawa, disebabkan sifat berkaitan X penyakit ini, wanita adalah pembawa yang tidak terjejas; bagaimanapun, kini jelas bahawa ramai wanita terjejas dan terdapat interaksi yang kompleks antara ciri-ciri varian tertentu dan penyahaktifan X yang condong yang membawa kepada persembahan klinikal yang sangat heterogen (39). Ini telah merumitkan keputusan bila dan cara merawat pesakit wanita penyakit Fabry, kerana sesetengah individu mendapat manfaat daripada terapi tetapi kami kekurangan alat untuk meramalkan tindak balas sebelum pesakit mengalami gejala, menonjolkan kawasan yang memerlukan penyelidikan lanjut.

Serbuk cistanche
Terapi sasaran lain tersedia untuk pesakit dengan penyakit buah pinggang genetik, menggunakan teknik baharu seperti gangguan RNA (RNAi), antisense-oligonucleotides (ASO), dan CRISPR-Cas9. RNAi telah menunjukkan janji besar untuk rawatan penyakit buah pinggang genetik, dengan ujian fasa III positif menggunakan patisiran untuk merawat amiloidosis transthyretin keturunan disebabkan oleh varian TTR dan lumasiran untuk merawat hiperoksaluria primer jenis 1 disebabkan oleh varian AGT (40, 41). Rawatan ini telah direka bentuk untuk menjadi varian agnostik, membolehkan mereka digunakan untuk merawat individu dengan pelbagai varian jarang yang berbeza. CRISPR-Cas9 telah dikaji dalam kohort kecil individu dengan amyloidosis transthyretin dan ditunjukkan untuk mengurangkan pengeluaran TTR serum melalui ketukan gen yang disasarkan menggunakan teknik penghantaran in vivo (42). Rawatan ASO yang melangkau ekson terhadap varian COL4A5 yang dipotong telah ditunjukkan pada tikus untuk mendorong penambahbaikan klinikal dan histologi dengan mengubah kesan protein kepada pemadaman ekson dalam bingkai (43). Ini mungkin menjadi pilihan rawatan untuk pesakit dengan pelbagai varian COL4A5 yang jarang dipotong yang biasanya menyebabkan penyakit yang teruk tetapi masih belum dikaji pada manusia. Pendekatan terapeutik untuk APOL{16}}nefropati yang berkaitan termasuk menggunakan rawatan ASO untuk mengurangkan ekspresi APOL1 dan penggunaan perencat molekul kecil APOL1 untuk mengurangkan fungsinya (44). Terapi yang disasarkan dan diperibadikan ini mungkin digunakan untuk penyakit genetik yang berbeza dan menawarkan pesakit kami harapan untuk rawatan yang lebih baik pada masa hadapan.
RUJUKAN
1. Levin A, Stevens PE, Bilous RW, et al. 2013. Penyakit Buah Pinggang: Meningkatkan Hasil Global (KDIGO) kumpulan kerja CKD. Garis panduan amalan klinikal KDIGO 2012 untuk penilaian dan pengurusan penyakit buah pinggang kronik. Buah Pinggang Int. Suppl. 3(1):1–150
2. Bikbov B, Purcell CA, Levey AS, et al. 2020. Beban global, serantau dan kebangsaan penyakit buah pinggang kronik, 1990–2017: analisis sistematik untuk Kajian Beban Global Penyakit 2017. Lancet 395(10225):709–33
3. Arpegård J, Viktorin A, Chang Z, et al. 2015. Perbandingan kebolehwarisan cystatin C- dan anggaran berasaskan kreatinin fungsi buah pinggang dan kaitannya dengan kebolehwarisan penyakit kardiovaskular. J. Am. Heart Assoc. 4(1):e001467
4. Wuttke M, Li Y, Li M, et al. 2019. Katalog lokus genetik yang dikaitkan dengan fungsi buah pinggang daripada analisis sejuta individu. Nat. Genet. 51(6):957–72
5. Zhang J, Thio CHL, Gansevoort RT, et al. 2021. Pengagregatan keluarga CKD dan kebolehwarisan biomarker buah pinggang dalam populasi umum: Kajian Kohort Talian Hayat. Am. J. Buah Pinggang Dis. 77(6):869–78
6. Karczewski KJ, Francioli LC, Tiao G, et al. 2020. Spektrum kekangan mutasi dikira daripada variasi dalam 141,456 manusia. Alam 581(7809):434–43
7. Lek M, Karczewski KJ, Minikel EV, et al. 2016. Analisis variasi genetik pengekodan protein dalam 60,706 manusia. Alam 536(7616):285–91
8. Projek 1000 Genom. Permaisuri. 2015. Rujukan global untuk variasi genetik manusia. Alam 526(7571):68–74
9. Ars E, Ballarin J, Ruiz P, et al. 2011. Utiliti klinikal ujian genetik pada kanak-kanak dan orang dewasa dengan sindrom nefrotik tahan steroid. Clin. J. Am. Soc. Nephrol. 6(5):1139–48
10. Wühl E, van Stralen KJ, Wanner C, et al. 2014. Terapi penggantian buah pinggang untuk penyakit jarang yang menjejaskan buah pinggang: analisis Pendaftaran ERA-EDTA. Nephrol. Pemindahan Dialisis. 29(Bekalan 4):iv1–8
11. Cocchi E, Nestor JG, Gharavi AG. 2020. Pemeriksaan genetik klinikal pada pesakit dewasa dengan penyakit buah pinggang. Clin. J. Am. Soc. Nephrol. 15(10):1497–510
12. Génin E. 2020. Kebolehwarisan penyakit kompleks hilang: kes selesai? Hum Genet. 139(1):103–13
13. Wainschtein P, Jain D, Zheng Z, et al. 2022. Menilai sumbangan varian jarang kepada kebolehwarisan sifat kompleks daripada data jujukan genom keseluruhan. Nat. Genet. 54(3):263–73
14. Verbitsky M, Westland R, Perez A, et al. 2019. Landskap variasi nombor salinan anomali kongenital buah pinggang dan saluran kencing. Nat. Genet. 51(1):117–27
15. Groopman EE, Marasa M, Cameron-Christie S, et al. 2018. Utiliti diagnostik penjujukan exome untuk penyakit buah pinggang. N. Inggeris. J. Med. 380(2):142–51
16. Tan AY, Zhang T, Michael A, et al. 2018. Mutasi somatik dalam epitelium sista buah pinggang dalam penyakit buah pinggang polikistik dominan autosomal. J. Am. Soc. Nephrol. 29(8):2139–56
17. Vlasschaert C, McNaughton AJM, Chong M, et al. 2022. Persatuan hematopoiesis klonal potensi tak tentu dengan fungsi buah pinggang yang lebih teruk dan anemia dalam dua kohort pesakit dengan penyakit buah pinggang kronik lanjutan. J. Am. Soc. Nephrol. 33(5):985–95
18. Fu XJ, Nozu K, Kaito H, et al. 2016. Mozek somatik dan frekuensi varian yang dikesan oleh penjujukan generasi seterusnya dalam sindrom Alport berkaitan X. Eur. J. Hum. Genet. 24(3):387–91
19. Rasouly HM, Groopman EE, Heyman-Kantor R, et al. 2019. Beban varian patogenik calon untuk gangguan buah pinggang dan genitouriner yang timbul daripada penjujukan exome. Ann. Intern. Med. 170(1):11–21
20. Devuyst O, Knoers NVAM, Remuzzi G, et al. 2014. Penyakit buah pinggang yang jarang diwarisi: cabaran, peluang dan perspektif. Lancet 383(9931):1844–59
21. Ingelfinger JR, Kalantar-Zadeh K, Schaefer F, et al. 2016. Mengelakkan legasi penyakit buah pinggang—fokus pada zaman kanak-kanak. Buah Pinggang Dis. 2(1):46–52
22. Bierzynska A, McCarthy HJ, Soderquest K, et al. 2017. Pemprofilan genomik dan klinikal bagi kohort sindrom nefrotik kebangsaan menyokong pendekatan perubatan ketepatan kepada pengurusan penyakit. Buah Pinggang Int. 91(4):937–47
23. Mikó Á, Menyhárd DK, Kaposi A, et al. 2018. Patogenik bergantung kepada mutasi NPHS2 p.R229Q: panduan untuk penilaian klinikal. Hum. Mutat. 39(12):1854–60
24. van der Ven AT, Connaughton DM, Ityel H, et al. 2018. Penjujukan keseluruhan exome mengenal pasti mutasi penyebab dalam keluarga dengan anomali kongenital buah pinggang dan saluran kencing. J. Am. Soc. Nephrol. 29(9):2348–61
25. Jayasinghe K, Stark Z, Kerr PG, et al. 2021. Kesan klinikal ujian genomik pada pesakit yang disyaki penyakit buah pinggang monogenik. Genet. Med. 23:183–91
26. Cornec-Le Gall E, Ahli Parlimen Audrézet, Rousseau A, et al. 2016. Skor PROPKD: algoritma baharu untuk meramalkan survival buah pinggang dalam penyakit buah pinggang polikistik dominan autosomal. J. Am. Soc. Nephrol. 27(3):942–51
27. Hwang YH, Conklin J, Chan W, et al. 2016. Menapis korelasi genotip-fenotip dalam penyakit buah pinggang polikistik dominan autosomal. J. Am. Soc. Nephrol. 27(6):1861–68
28. Gibson JT, Huang M, Shenelli Croos Cabrera M, et al. 2022. Korelasi genotip-fenotip untuk varian COL4A3–COL4A5 yang mengakibatkan penggantian Gly dalam sindrom Alport. Sci. Rep. 12:2722
29. Yamamura T, Horinouchi T, Nagano C, et al. 2020. Korelasi genotip-fenotip mempengaruhi tindak balas terhadap ubat penargetan angiotensin dalam pesakit Jepun dengan sindrom Alport berkaitan X lelaki. Buah Pinggang Int. 98(6):1605–14
30. Bekheirnia MR, Reed B, Gregory MC, et al. 2010. Korelasi genotip-fenotip dalam sindrom Alport berkaitan X. J. Am. Soc. Nephrol. 21(5):876–83
31. Fahed AC,Wang M,Homburger JR, et al. 2020. Latar belakang poligenik mengubah penetrasi varian monogenik untuk keadaan genomik peringkat 1. Nat. Commun. 11(1):3635
32. Wang N, Zheng Y, Zhang L, et al. 2022. Keluarga mengasingkan kekurangan koenzim utama Q10 yang boleh membawa maut disebabkan oleh dua varian COQ6 novel. Depan. Genet. 12:811833
33. Bollée G, Harambat J, Bensman A, et al. 2012. Kekurangan adenine phosphoribosyltransferase. Clin. J. Am. Soc. Nephrol. 7(9):1521–27
34. Kemper MJ, Lemke A. 2018. Rawatan bentuk genetik sindrom nefrotik. Depan. Pediatr. 6:72
35. Khan A, Barber DL, Huang J, et al. 2021. Terapi gen pengantara Lentivirus untuk penyakit Fabry. Nat. Commun. 12(1):1178
36. McCafferty EH, Scott LJ. 2019. Migalastat: kajian semula dalam penyakit Fabry. Dadah 79(5):543–54
37. Hughes DA, Nicholls K, Shankar SP, et al. 2017. Pendamping farmakologi oral migalastat berbanding terapi penggantian enzim dalam penyakit Fabry: 18-hasil bulan daripada kajian TARIK fasa III rawak. J. Med. Genet. 54(4):288–96
38. Germain DP, Hughes DA, Nicholls K, et al. 2016. Rawatan penyakit Fabry dengan pengasuh farmakologi migalastat. N. Inggeris. J. Med. 375(6):545–55
39. Germain DP, Arad M, Burlina A, et al. 2019. Kesan terapi penggantian enzim pada hasil klinikal pada pesakit wanita dengan penyakit Fabry—semakan literatur sistematik oleh panel pakar Eropah. Mol. Genet. Metab. 126(3):224–35
40. Adams D, Gonzalez-Duarte A, O'Riordan WD, et al. 2018. Patisiran, terapeutik RNAi, untuk amyloidosis transthyretin keturunan. N. Inggeris. J. Med. 379(1):11–21
41. Garrelfs SF, Frishberg Y, Hulton SA, et al. 2021. Lumasiran, terapeutik RNAi untuk jenis hyperoxaluria primer 1. N. Engl. J. Med. 384(13):1216–26
42. Gillmore JD, Gane E, Taubel J, et al. 2021. CRISPR-Cas9 dalam penyuntingan gen vivo untuk transthyretin amyloidosis. N. Inggeris. J. Med. 385(6):493–502
43. Yamamura T, Horinouchi T, Adachi T, et al. 2020. Pembangunan terapi ekson-skip untuk sindrom Alport berkaitan X dengan varian pemangkasan dalam COL4A5. Nat. Commun. 11(1):2777
44. Daneshpajouhnejad P, Kopp JB, Winkler CA, et al. 2022. Kisah berkembang nefropati apolipoprotein L1: penghujung permulaan. Nat. Rev. Nephrol. 18(5):307–20
Mark D. Elliott,1,2,3 Hila Milo Rasouly,1,2 dan Ali G. Gharavi1,2,3
1 Division of Nephrology, Department of Medicine, Columbia University Vagelos College of Physicians and Surgeons, New York, NY, USA; email: ag2239@columbia.edu
2 Pusat Perubatan Ketepatan dan Genomik, Jabatan Perubatan, Kolej Perubatan dan Pakar Bedah Universiti Columbia Vagelos, New York, NY, Amerika Syarikat
3 Institut Perubatan Genomik, Kolej Perubatan dan Pakar Bedah Universiti Columbia Vagelos, New York, NY, Amerika Syarikat






