Bahagian 1: Apakah peranan BDNF dalam Kecederaan Otak Traumatik Eksperimen Dan Klinikal?
Mar 26, 2022
Hubungi: Audrey Hu Whatsapp/hp: 0086 13880143964 E-mel:audrey.hu@wecistanche.com
1 Seksyen Neurosurgeri, Jabatan Neurosains, Universiti Uppsala,75124Uppsala, Sweden;
dfsgustafsson@gmail.com
2 Jabatan Neurosains Klinikal, Perubatan Pemulihan, Universiti Uppsala,75124 Uppsala, Sweden;
andrea.klang@akademiska.se
3 Jabatan Neurosains Klinikal, Institut Karolinska, 17177 Stockholm, Sweden; sebastian.thams@ki.se 4 Jabatan Neurosains, Institut Karolinska,17177 Stockholm, Sweden *Surat menyurat: elham.rostami@neuro.u.se
Abstrak: Kecederaan otak traumatik adalah salah satu punca utama kematian dan morbiditi di dunia tanpa rawatan farmakologi semasa. Peranan BDNF dalam pembaikan dan penjanaan semula saraf telah mantap dan juga telah menjadi tumpuan penyelidikan TBI. Di sini, kami mengkaji model haiwan eksperimen yang menilai ekspresi BDNF berikutan kecederaan serta kajian klinikal pada manusia termasuk peranan polimorfisme BDNF dalam TBI. Terdapat heterogeniti yang besar dalam persediaan eksperimen dan oleh itu keputusan dengan perubahan serantau dan temporal yang berbeza dalam ekspresi BDNF. Beberapa kajian juga telah menilai intervensi yang berbeza untuk mempengaruhi ekspresi BDNF berikutan kecederaan. Kajian klinikal menyerlahkan kepentingan polimorfisme BDNF dalam hasilnya dan menunjukkan peranan perlindungan polimorfisme BDNF selepas kecederaan. Memandangkan kemungkinan menjejaskan laluan BDNF dengan bahan yang tersedia, kami membincangkan kajian masa depan menggunakan tikus transgenik serta iPSC untuk memahami mekanisme asas polimorfisme BDNF dalam TBI dan membangunkan rawatan farmakologi yang mungkin.
Kata kunci: BDNF; neurotropin; faktor neurotropik; kecederaan otak trauma; penjanaan semula saraf; perlindungan saraf; otak; neuron

Cistanche mempunyai kesan neuroprotektif yang sangat baik
1. Pengenalan
Traumatikotakkecederaan (TBI) adalah punca utama kematian di seluruh dunia, dan pada orang dewasa muda di bawah umur 35 tahun, kadar kematian adalah 3.5 kali ganda daripada gabungan kanser dan penyakit jantung [1]. TBI ialah keadaan dinamik dengan kecederaan primer awal yang mencetuskan peristiwa sekunder yang boleh berkembang selama berjam-jam, bulan, malah bertahun-tahun. Peristiwa ini boleh memudaratkan seperti iskemia, kegagalan tenaga, dan keradangan, atau berfaedah seperti peningkatan ekspresineurotropindan faktor pertumbuhan yang menggalakkan kelangsungan hidup dan keplastikan neuron.
Neurotropin, khususnyaberasal dari otakfaktor neurotropik (BDNF), telah dikenal pasti memainkan peranan penting dalam peristiwa selular yang berlaku dalam proses pemulihan berikutan TBI, seperti kelangsungan hidup neuron, percambahan aksonal, dan sinaptogenesis [2]. Oleh kerana peranan penting BDNF, impaknya telah disiasat secara meluas dalam model TBI eksperimen dan kajian manusia [3]. Ia juga telah menunjukkan bahawa polimorfisme BDNF mempengaruhi hasil selepas TBI, tetapi mekanisme asas belum difahami sepenuhnya. Seperti yang akan kita terokai dalam artikel ini, terdapat juga percanggahan dalam hasil daripada model eksperimen yang mengkaji ungkapan BDNF mengenai masa selepas kecederaan, penyetempatan anatomi dan hasil. Dalam ulasan ini, kami berhasrat untuk merangkumi penemuan dalam TBI eksperimen yang menyiasat BDNF dan kajian manusia yang meneroka kesan polimorfisme BDNF untuk mengenal pasti jurang pengetahuan utama untuk mengarahkan kajian masa depan.
1.1. Faktor Neurotropik Terbitan Otak (BDNF)
BDNF adalah yang paling banyakneurotropindi dalamotak[4,5], memainkan peranan penting dalam kelangsungan hidup, pembezaan, keplastikan sinaptik, dan pertumbuhan akson neuron periferal dan pusat sepanjang masa dewasa [2,4,6]. BDNF mengantara kesannya melalui reseptor tirosin kinase pertalian tinggi (TrkB) [7]. Ekspresi peningkatan mRNA TrkB telah dikesan di tapak kecederaan berikutan kecederaan saraf tunjang dan TBI [8,9]. BDNF juga mengikat kepada reseptor pan-neurotrophin p75NTR, ahli keluarga reseptor faktor nekrosis tumor (TNFR) [10]. Reseptor p75NTR telah dicadangkan untuk mempunyai dua peranan sebagai fasilitator survival neuron yang dimediasi Trk dan sebagai pengawal selia kematian sel neuron melalui permulaan apoptosis. Sehubungan itu, salah satu kelemahan rawatan menggunakan analog BDNF ialah ia juga mempengaruhi reseptor p75NTR yang mengantara apoptosis. Oleh itu, ubat terpilih TrkB atau perencat p75NTR akan lebih bermanfaat.
1.2 BDNF Val66met Polimorfisme
Polimorfisme nukleotida tunggal BDNF (SNP) dalam rs6265 menghasilkan mutasi missense, Val66Met (196G/A), yang menyebabkan defisit dalam rembesan bergantung kepada aktiviti BDNF [11]. Mutasi Val66Met berlaku pada kira-kira 30 peratus daripada populasi di AS (meet carrier/met plus ). Apabila diterjemahkan, molekul BDNF mengandungi tiga domain penting: peptida isyarat, prodomain, dan molekul BDNF berfungsi, semuanya bertindak pada reseptor yang berbeza. BDNF matang mengikat kepada reseptor TrkB dan menggalakkan potensiasi jangka panjang (LTP), kemandirian sel dan pembentukan dendrit; manakala proBDNF mengikat p75NTR dan mengaktifkan kemurungan jangka panjang (LTD), apoptosis, dan mengurangkan kerumitan dendritik. Mekanisme dwi ini berfungsi secara antagonis dan mengawal neuroplastisitas. Mutasi Val66Met mengakibatkan pengumpulan metBDNF dalam soma manakala valBDNF terkumpul dalam vesikel tanda baca dalam dendrit. Neuron tidak boleh merembeskan metBDNF sebagai tindak balas kepada aktiviti yang mengakibatkan keplastikan terjejas dalam pembawa bertemu.

herba cistanche
2. Polimorfisme BDNF dalam Kajian Manusia
Polimorfisme BDNF yang paling banyak dikaji pada manusia ialah rs6265 (Val66Met), berhubung dengan fungsi kognitif normal, kesan pada penyakit psikiatri, neurodegeneratif, dan neuro inflamasi, dan traumatik.otakkecederaan [11–15]. Ini juga berlaku dalam TBI [16,17], walaupun SNP tambahan seperti rs71244 [18,19], rs1519480, rs7124442 [20], dan rs1153659 [21] telah dikenal pasti untuk mempengaruhi hasil selepas traumatik.otakkecederaan. SNP rs6265 BDNF menyebabkan penggantian valine kepada metionin dan kelaziman pembawa heterozigot atau homozigot metionin adalah sekitar 30 peratus daripada populasi Amerika Syarikat [22], tetapi berbeza secara global [23]. Kebanyakan kajian membandingkan pembawa valine homozigot (Met-) kepada pembawa heterozigot dan homozigot metionin (Met plus). Minoriti kajian mempunyai tiga kumpulan [17,24,25], memisahkan heterozigot bertemu tambah daripada homozigot bertemu tambah.
Di kalangan individu yang sihat (min umur 36 tahun), pembawa met-alel mempunyai ingatan episod yang lebih teruk diukur dengan ujian memori kerja n-back, serta aktiviti hippocampal yang tidak normal yang dinilai oleh MRI berfungsi (fMRI), berbanding dengan Met- [11]. ]. Keputusan yang sama telah ditunjukkan dalam kajian lain dengan individu yang sihat (min umur 30 tahun), juga mengukur memori episod dan aktiviti hippocampus dengan fMRI semasa ujian [26]. Pembawa bertemu mempunyai 25 peratus kurang pengaktifan kawasan hippocampal dan prestasi yang lebih lemah dalam mengenali maklumat "baru" dan "lama". Menariknya, terdapat tanda-tanda bahawa menjadi pembawa terpenuhi mungkin mempunyai faedah kognitif apabila penuaan. Tinjauan Mental Scotland 1947 termasuk analisis genetik dan susulan jangka panjang dan menunjukkan bahawa pembawa bertemu lebih baik mengekalkan kemahiran penaakulan bukan lisan pada usia yang lebih tua (min umur 79) [15], menunjukkan bahawa pembawa bertemu mungkin memelihara kognitif. berfungsi lebih baik daripada yang ditemui-, semasa penuaan. Faedah juga telah ditunjukkan dalam risiko mengembangkan penyakit Alzheimer di kalangan individu bukan TBI, di mana risiko lebih tinggi untuk Val-homozigot di kemudian hari tetapi sebaliknya di kalangan subjek yang lebih muda [14]. Ini selaras dengan teori met plus yang memberi kesan positif terhadap pemeliharaan fungsi kognitif pada usia yang lebih tua.
2.1. Polimorfisme dan Hasil BDNF selepas TBI Ringan dan Sederhana
Kesan polimorfisme BDNFval66met pada hasil kognitif awal selepas TBI ringan (mTBI) telah dinilai dalam dua kajian berbeza dan menunjukkan keputusan yang lebih teruk untuk pembawa bertemu. Pada susulan subakut (sebulan) selepas mTBI, kedua-dua kawalan Met plus dan kumpulan Met plus TBI mempunyai masa tindak balas yang lebih perlahan dalam kedua-dua masa tindak balas mudah (SRTRT—masa tindak balas mudah) dan kelajuan pemprosesan maklumat (diukur dengan Gordon Continuous Ujian Pemprosesan—CPT) berbanding Met-pesakit dan kawalan [17]. Ini berkait dengan kajian lain di mana peserta diuji dalam lima domain kognitif: perhatian, ingatan, bahasa, visuospatial, dan fungsi eksekutif, serta-merta selepas pemulihan dan pada enam bulan susulan [27]. Secara keseluruhan, Met- mempunyai prestasi neurokognitif yang lebih baik, tanpa sebarang perbezaan yang ketara antara mata dua masa. Walau bagaimanapun, pembawa bertemu menunjukkan prestasi yang lebih teruk pada ujian ingatan pada enam bulan, menunjukkan kemerosotan beberapa domain fungsi kognitif.
Namun begitu, dalam susulan veteran tentera selepas mTBI dalam fasa kronik (min 4.5 tahun), menilai memori dan fungsi eksekutif, kumpulan Met plus dengan TBI mempunyai keputusan yang lebih baik daripada kumpulan kawalan yang sepadan, manakala Met- mempunyai sebaliknya. keputusan [28]. Ini boleh menunjukkan bahawa kehadiran Met plus SNP menghasilkan garis asas fungsi kognitif yang lebih rendah tetapi menawarkan kualiti perlindungan kognisi selepas TBI.
Risiko untukkemerosotan sarafselepas TBI telah dibincangkan dan dinilai dalam kajian yang berbeza [29]. TBI yang teruk telah dikaitkan dengan risiko yang lebih tinggi untukkemerosotan saraftetapi dalam dekad yang lalu, pautan ini juga telah dicadangkan untuk TBI ringan [30,31]. Untuk mencari tanda awal demensia, jumlah Hippocampus dinilai dengan MRI pada individu yang mempunyai sejarah mTBI berbanding kawalan, berhubung dengan beberapa BDNF SNP. Rs1153659 alel kecil dikaitkan dengan risiko yang lebih tinggi untuk mengurangkan jumlah hippocampal selepas mTBI berbanding kawalan tetapi tidak ada perbezaan untuk rs6265 [21].
Dalam satu kajian yang menyiasat kesan tajuk dalam pemain bola sepak selama enam bulan pada remyelination yang dinilai oleh pengimejan tensor resapan (DTI), ia telah menunjukkan bahawa pembawa bertemu mempunyai pengurangan remyelination secara signifikan berbanding pemain homozigot Val [32]. Ini mungkin menjelaskan sebahagian daripada patofisiologi yang mendasari dalam hasil fungsi yang lemah berikutan mTBI berulang dalam pemain bola sepak. Mungkin terdapat perbezaan jantina seperti yang ditunjukkan oleh Larson-Depuis et al. di mana atlet wanita yang mempunyai sejarah gegaran mempunyai fungsi penciuman yang lebih baik jika mereka bertemu-pembawa berbanding dengan Val-homozigot [25]. Fungsi penciuman dicadangkan sebagai penunjuk potensi kecederaan struktur dan fungsian selepas gegaran, serta strukturotakdiketahui boleh menjana semula dan terdedah kepada BDNF.
Hasil kognitif selepas TBI adalah pelbagai faktor. Umur dan jantina mempengaruhi keputusan [18,19,33] dan keterukan dan jenisotakkecederaan akan menjejaskan kognisi. Selain itu, faktor psikiatri boleh membawa kesan kepada fungsi kognitif. Gangguan tekanan selepas trauma (PTSD) telah menjadi semakin dibincangkan sebagai kemungkinan akibat TBI [34], yang sebagai balasannya boleh memberi kesan kepada fungsi kognitif. Satu kajian melaporkan peningkatan prevalens PTSD di kalangan pesakit Met plus dengan mTBI [24]. Satu lagi faktor psikiatri yang boleh berinteraksi dengan kognisi ialah kemurungan, yang sebagai balasannya boleh menjadi akibat daripada TBI [35]. Pelajar Met plus melaporkan kejadian gejala kemurungan yang lebih tinggi selepas mTBI yang dilaporkan sendiri berbanding pelajar Met- dengan sejarah mTBI [36,37]. Perbezaannya lebih ketara dalam kalangan pelajar perempuan.
Perbezaan jantina yang berkaitan dengan gejala kemurungan dan kegelisahan telah ditangani lebih lanjut dalam kajian yang mengikuti gejala tersebut dalam sekumpulan pesakit satu dan enam minggu selepas mTBI [36]. Kajian ini menilai polimorfisme BDNF yang berbeza dan mendapati bahawa lelaki dengan alel-t, polimorfisme yang berbeza daripada val66met, mempunyai risiko yang lebih tinggi untuk kemurungan selepas enam minggu, sementara ini tidak berlaku untuk wanita. Pesakit dengan sejarah TBI ringan hingga sederhana dan kemurungan yang didiagnosis bertindak balas secara berbeza kepada Citalopram, bergantung kepada BDNF rs6265, di mana responden terbaik adalah val-homozigot [38].

faedah cistanche
2.2. Polimorfisme dan Hasil BDNF dalam TBI Teruk
Hanya satu kajian boleh dikenal pasti yang menyiasat kesan polimorfisme BDNFval66met pada pemulihan awal selepas TBI teruk [39]. Bagnato et al. menilai fungsi kognitif 53 pesakit dalam keadaan vegetatif berikutan TBI teruk menggunakan Tahap Rancho Skala Fungsi Kognitif. Ujian telah dilakukan pada 1-, 3-, 6- dan 12-bulan selepas kecederaan, dan tiada perbezaan dapat dikesan antara pembawa bertemu berbanding dengan Met-.
Terdapat beberapa kajian mengenai hasil jangka panjang berikutan teruk, menembusiotakkecederaan dalam veteran Amerika Vietnam di mana korelasi polimorfisme BDNF dan hasil kognitif telah dikaji [16,20,40]. Susulan kajian ini adalah 40 tahun selepas TB I. Dua daripadanya mengkaji kesan polimorfisme BDNF pada IQ dan fungsi eksekutif dalam veteran dengan penembusan TBI dalam korteks prefrontal (PFC). Kedua-duanya mendapati fungsi kognitif terpelihara dalam pembawa bertemu dengan TBI berbanding pembawa tidak bertemu [16,40]. Dalam kajian ketiga, kecederaan yang menembusi semua dimasukkan tanpa keutamaan PFC [20]. Dalam kajian ini, tiada perbezaan yang ketara ditemui antara kumpulan untuk SNP rs6265 tetapi dua lagi BDNF SNP mempunyai kesan yang ketara ke atas IQ, rs1519480, dan rs7124442. Ini mungkin menunjukkan bahawa terdapat kesan perlindungan polimorfisme BDNF berikutan kecederaan dan mungkin terdapat kesan sinergistik dengan kawasan anatomi yang berbeza.
Tiga kajian telah menggunakan skor risiko gen berdasarkan SNP BDNF "risiko" (rs6265 dan rs 7124442) [18,19,33], diselaraskan untuk umur, untuk menilai hasil global dan kematian selepas TBI teruk. Dua kajian menunjukkan kematian yang lebih rendah pada tahun pertama (8–365 hari) selepas TBI di kalangan penduduk yang lebih muda (<45 and=""><48 y)="" with="" the="" low="" gene="" risk="" score="" (ie="" met-="" and="" rs7124442="" t-homozygote),="" whilst="" the="" older="" population="" with="" low="" gene="" risk="" score="" had="" higher="" mortality="" [18,33].="" the="" third="" study="" had="" similar="" results="" where="" lower="" age="" had="" a="" higher="" rate="" of="" survival="" at="" six="" months="" with="" a="" low="" gene="" risk="" score,="" though="" these="" results="" were="" to="" some="" extent="" influenced="" by="" levels="" of="" csf="" cortisol="" as="" well="">
2.3. Tahap BDNF dalam CSF dan Plasma selepas TBI
Tiga kajian boleh dikenal pasti di mana tahap BDNF diukur dalam plasma dan/atau CSF. Simon et al. menganalisis tahap BDNF dalam plasma semasa kemasukan ke ICU, pada purata 6.4 jam selepas ketibaan ke hospital berikutan TBI teruk dalam 120 lelaki (Glasgow Coma Scale (GCS) 3-8). Tiada korelasi antara paras plasma BDNF dan hasil maut jangka pendek (kematian ICU vs. pelepasan ICU) atau antara terpencilotakkecederaan berbanding pelbagai trauma [41]. Dalam 12 kanak-kanak dengan tahap TBI BDNF yang teruk dalam CSF dan plasma pada 2 dan 24 jam selepas trauma, tidak ada korelasi dengan Skala Hasil Glasgow (GOS) semasa pelepasan [42], walaupun terdapat puncak mendadak BDNF selepas kepala. kecederaan dalam semua mata pelajaran. Satu lagi kajian termasuk 315 pesakit dengan TBI teruk menunjukkan hubungan antara tahap BDNF dalam CSF berhubung dengan tahap kortisol dalam CSF pada minggu pertama selepas kecederaan, dan 6-kematian bulan [19]. Begitu juga, paras CSF BDNF yang tinggi setiap hari menjadi sampel minggu pertama selepas kecederaan, dikaitkan dengan peningkatan kematian (8–365 hari selepas kecederaan), manakala kematian akut (0-7 hari) dikaitkan dengan serum rendah. tahap BDNF [33].
Kajian tentang kesan polimorfisme BDNF val66met berbeza dalam ukuran hasil, masa dan jenisotakkecederaan. Secara amnya, kajian adalah kecil dan kebanyakan populasi kajian adalah lebih kecil daripada 200 individu. Akibatnya, kajian prospektif adalah terhad dan hasilnya adalah heterogen. Prevalens bertemu/bertemu dalam populasi Kaukasia adalah rendah dan oleh itu kebanyakan kajian mengelompokkan met-heterozygote dan met-homozygote bersama-sama untuk analisis.

faedah cistanche gurun: mencegahotakkecederaan
3. TBI eksperimen
Dalam bahagian ini, kami meringkaskan pengetahuan semasa ekspresi BDNF selepas traumatikotakkecederaan (TBI) dalam model haiwan yang berbeza, serta korelasi antara pilihan rawatan TBI novel dan ekspresi BDNF, dan kesannya terhadap hasil tingkah laku. Dalam bahagian menilai ungkapan BDNF selepas TBI berbanding dengan palsu, kami memilih untuk mengecualikan kajian yang tidak menyatakan dengan jelas lokasi atau masa analisis BDNF serta yang tidak melaporkan data daripada haiwan palsu.
3.1. Model Haiwan Eksperimen
Lebih daripada sepuluh model trauma yang berbeza telah digunakan untuk mengkaji ekspresi BDNF selepas TBI (Rajah 1) dan kaedah yang paling dipilih ialah impak kortikal terkawal (CCI), diikuti oleh kecederaan perkusi cecair (FPI) dan model penurunan berat badan. Tiada kajian yang menganalisis secara khusus sama ada model trauma yang berbeza memberi kesan yang berbeza terhadap ekspresi BDNF. Model yang dipilih ditentukan oleh jenis trauma yang ingin dicontohi, contohnya, daya tumpul atau kecederaan tembus. Kami cuba membuat kesimpulan mengenai kesan jenis trauma yang berbeza terhadap ekspresi BDNF tetapi terdapat hasil yang bercanggah dalam bahan yang disemak. Sebagai contoh, Colak et al. menggunakan model impak kortikal terkawal manakala Wang et al. menggunakan model perkusi cecair dan kedua-duanya mendapati bahawa trauma meningkatkan ekspresi mRNA BDNF pada hari pertama selepas kecederaan (DPI) dalam tisu kortikal ipsilateral kepada kecederaan [43,44]. Sebaliknya, Boone et al. juga menggunakan model perkusi cecair dan mendapati penurunan ekspresi mRNA BDNF dalam hippocampus ipsilateral selepas 20 jam tetapi ekspresi tidak terjejas dengan ketara pada 4, 8, 16 dan 24 jam selepas kecederaan [45]. Ringkasnya, untuk membuat kesimpulan yang muktamad terdapat keperluan untuk kajian yang menganalisis secara khusus kesan model yang berbeza terhadap ekspresi BDNF.
Rajah 1. Model trauma dalam kajian yang disemak.
3.2. Kawasan Anatomi Analisis BDNF
Dalam bahan yang disemak, kawasan anatomi yang dianalisis sangat berbeza. Untuk membandingkan dan memeriksa trend dalam data yang diterbitkan, kawasan anatomi telah dikumpulkan bersama (Rajah 2). Kajian yang menganalisis kawasan yang berbeza, contohnya, kedua-dua ipsilateral dan kontralateral hippocampus (HC), dikira secara berasingan untuk setiap rantau yang dianalisis. Ekspresi BDNF paling banyak dianalisis dalam hippocampus ipsilateral dan korteks ipsilateral, dalam 36
dan 31 kajian, masing-masing. Dalam 7 kajian, hippocampi ipsilateral dan kontralateral digabungkan untuk pemeriksaan biokimia dan dilabelkan "HC dua hala".
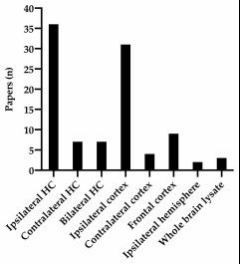
Rajah 2. Kawasan anatomi dianalisis dalam bahan yang disemak.
3.3. Penilaian Ungkapan BDNF
Kedua-dua mRNA dan ekspresi protein BDNF dinilai. Kaedah yang paling biasa untuk analisis mRNA ialah hibridisasi in situ dan tindak balas rantai polimerase masa nyata kuantitatif (qPCR). Untuk pengiraan protein BDNF, Western blot dan ujian imunosorben berkaitan enzim (ELISA) biasanya digunakan (Jadual A2). Dalam kebanyakan bahan yang disemak, ekspresi protein BDNF tidak dinyatakan secara eksplisit kepada matang, pro atau praBDNF. Apabila tidak dinyatakan sebaliknya, kami menganggap bahawa kajian itu merujuk kepada jumlah ekspresi protein BDNF. Selain itu, melainkan dinyatakan sebaliknya, kajian itu meneliti tisu tikus atau tikus.
3.3.1. Hippocampus
Ekspresi mRNA BDNF dalam hippocampus ipsilateral telah diperiksa pada 16 titik masa yang berbeza dan ekspresi protein BDNF dalam hippocampus ipsilateral telah diperiksa pada 23-titik masa (2 h- 56 d) (Rajah 3a). Tiga daripada kajian melaporkan peningkatan ekspresi mRNA BNDF dalam 1 hingga 6 jam pertama selepas kecederaan [44,46,47], manakala satu melaporkan penurunan ekspresi mRNA pada 20 jam selepas trauma dalam kedua-dua kumpulan TBI dan sham [45]. Pada semua titik masa berikutnya, ekspresi mRNA BDNF dalam hippocampus ipsilateral dilaporkan menurun atau tidak terjejas berbanding dengan palsu (Rajah 3a) [9,47-52]. Menariknya, ekspresi protein BDNF tidak menunjukkan sebarang ekspresi yang meningkat dengan ketara pada hari pertama selepas trauma dan menunjukkan ekspresi menurun atau tidak diubah pada minggu-minggu berikutnya (Rajah 3b). Satu kajian melaporkan ungkapan yang tidak terjejas dengan ketara dalam beberapa jam selepas trauma tetapi mendapati peningkatan ekspresi protein pada 26 jam selepas kecederaan [46]. Ekspresi protein BDNF dalam hippocampus ipsilateral telah berulang kali dilaporkan sebagai tidak terjejas dengan ketara oleh trauma pada 5 jam selepas kecederaan serta 1, 7, 11, 15, 21, 26, dan 37 DPI. Walau bagaimanapun, beberapa kajian melaporkan penurunan ekspresi protein pada 4, 7, 8, 10, 13, 14, dan 28 DPI [53-69]. Data ungkapan dari setiap tarikh biasanya daripada satu kajian setiap tarikh, serta hampir secara eksklusif daripada trauma CCI atau FPI. Tiada perbezaan yang jelas antara kumpulan trauma daripada data yang tersedia.

Rajah 3. Gambaran keseluruhan bilangan titik masa di manaberasal dari otak neurotropikekspresi faktor (BDNF) telah diperiksa dalam bahan yang disemak, dan sama ada TBI meningkat dengan ketara, menurun atau tidak mengubah ekspresi BDNF dengan ketara berbanding haiwan yang cedera. ( a ) Ekspresi mRNA BDNF dalam hippocampus ipsilateral. ( b ) Ekspresi protein BDNF dalam hippocampus ipsilateral. ( c ) Ekspresi mRNA BDNF dalam hippocampus kontralateral. ( d ) Ekspresi protein BDNF dalam hippocampus kontralateral. (e) Ekspresi mRNA BDNF dalam korteks ipsilateral (f) ekspresi protein BDNF dalam korteks ipsilateral.
Hippocampus kontralateral kepada kecederaan dianalisis pada titik enam masa untuk ekspresi mRNA BDNF dan tiga untuk ekspresi protein BDNF, antara 1 jam hingga 56 hari. Rostami et al. melaporkan bahawa ekspresi mRNA BDNF meningkat pada 1, 3, dan 14 hari selepas trauma dalam hippocampus kontralateral, tetapi tidak pada fasa kronik yang diukur pada 56 hari selepas kecederaan [9]. Pada hari pertama selepas trauma, Yang et al. melaporkan peningkatan ekspresi mRNA BDNF pada 1, 3, dan 5 jam selepas kecederaan. Dua kajian mendapati bahawa ekspresi protein BDNF tidak terjejas dengan ketara oleh trauma pada titik masa 7, 21 [58], dan 26 DPI [68].
3.3.2. Korteks
Korteks ipsilateral memaparkan corak ekspresi yang sama seperti hippocampus ipsilateral. Semasa hari pertama selepas kecederaan, ekspresi mRNA BDNF secara eksklusif dilaporkan meningkat [47,70]. Kobori et al. melaporkan peningkatan ekspresi mRNA BDNF menggunakan rt-PCR pada 2, 6, dan 24 jam selepas kecederaan, tetapi tiada perubahan yang ketara pada hari 3 dan 14 [71]. Seperti yang dilihat dalam Rajah 3e-f, peningkatan awal dalam mRNA BDNF ipsilateral tidak disertai dengan peningkatan yang menentukan dalam ekspresi protein BDNF. Sebaliknya, empat kajian melaporkan bahawa ekspresi protein BDNF telah menurun pada hari pertama, dan sebaliknya menurun atau tidak diubah dengan ketara oleh trauma pada titik masa 4, 7, 8, 25, 28, 30, dan 35 DPI [57,69,72- 87]. Pengecualian adalah Cekic et al. yang mendapati bahawa CCI mendorong peningkatan protein BDNF matang selepas 24 jam dan 7 hari [88], serta Nagatomo-Combs et al. yang menganalisis bilangan sel yang mengekspresikan protein BDNF dalam monyet rhesus pada titik masa yang lebih lama selepas trauma dan mendapati peningkatan bilangan sel yang mengekspresikan BDNF pada 1, 6, dan 12 bulan selepas kecederaan [89].
Sekali lagi, bahagian kontralateral tidak diperiksa dengan baik. Corne et al. memeriksa ekspresi mRNA kortikal dalam lobus parietal kontralateral pada 21 hari selepas kecederaan dan melaporkan penurunan semua ekson BDNF dalam kumpulan TBI berbanding sham [90], manakala Yang et al. mendapati tiada perubahan ketara dalam mRNA BDNF secara khusus dalam neokorteks kontralateral pada 1, 3, dan 5 jam selepas kecederaan hentaman kortikal sisi berbanding haiwan yang cedera palsu [47].
Untuk meringkaskan, beberapa kajian mendapati bahawa ekspresi mRNA BDNF meningkat dalam hippocampus ipsilateral dan korteks dalam 1-2 hari pertama selepas kecederaan dan bahawa mRNA BDNF meningkat dalam hippocampus kontralateral pada hari 1-14 selepas kecederaan. Peningkatan dalam mRNA BDNF ini tidak disertai dengan peningkatan yang jelas dalam protein BDNF dalam korteks mahupun hippocampi, namun, data masih tidak mencukupi untuk membuat kesimpulan yang pasti.

batang cistanche
3.4. Ujian Tingkah Laku
Beberapa kajian yang mengkaji korelasi antara ekspresi BDNF dan TBI melakukan ujian tingkah laku untuk menilai hasil berfungsi, seperti yang dilihat dalam Rajah 4. Dalam bahan yang disemak, kaedah penilaian fungsi yang paling biasa adalahNeurologiSkor Keterukan (NSS), yang merangkumi gabungan ujian motor, deria, refleks dan imbangan, serta Morris Water Maze (MWM), menilai memori spatial. Pengecaman objek baru, memeriksa pengecaman objek bukan spatial, rotarod, menilai imbangan dan koordinasi, Ujian medan terbuka, menilai tingkah laku dan kebimbangan lokomotor, Elevated Plus Maze, menilai tahap kebimbangan dan akhirnya, ujian Beam walk, yang memeriksa keseimbangan, digunakan dalam lebih daripada 5 kajian yang disemak. Kumpulan yang dipanggil "Lain-lain" termasuk ujian yang hanya digunakan dalam satu kajian, seperti ujian penggunaan sukrosa, ujian hayunan dan skor rampasan tonik-klonik. Penerangan yang lebih dekat mengenai ujian tingkah laku akan diikuti dalam bahagian seterusnya serta dalam Jadual A1.

Rajah 4. Ujian tingkah laku dianalisis dalam bahan yang disemak.
3.5. Rawatan TBI
Sebanyak 73 kajian menggunakan pelbagai intervensi untuk mengkaji kesannya terhadap BDNF-
ekspresi dan hasil fungsian berikutan TBI, seperti yang dilihat dalam Rajah 5. Yang paling biasa disiasat ialah kesan senaman dan diet, diikuti dengan rawatan kortikoid sel stem dan gonado. Untuk menyemak semua rawatan yang tersedia dalam traumatikotakkecederaan adalah di luar skop kajian ini, dan kami telah memberi tumpuan kepada mengkaji semula senaman, diet, dan rawatan sel stem serta campur tangan yang mempengaruhi laluan intraselular berikutan pengaktifan reseptor BDNF.

3.5.1. Senaman
Senaman sebagai kaedah terapeutik dalam traumatikotakkecederaan telah diperiksa dalam 14 kajian. Apa yang membentuk senaman berbeza antara kajian, tetapi kaedah yang paling biasa digunakan ialah roda larian. Beberapa kajian berbeza antara senaman sukarela dan tidak sukarela, dan beberapa artikel tidak mentakrifkan dengan tepat jenis senaman yang dilakukan. Daripada 14, 11 kajian itu mendapati bahawa sama ada senaman pra-atau selepas trauma meningkatkan ekspresi protein BDNF serebrum dalam hippocampus ipsilateral dan kontralateral serta dalam korteks ipsilateral, berbanding dengan haiwan yang tidak bersenam [58,59,62- 64,66–69,71,78,91–93]. Dua kajian mendapati bahawa ekspresi BDNF tidak berubah dengan ketara pada tikus yang terdedah kepada senaman selepas kecederaan perkusi cecair pada 7 atau 11 hari selepas kecederaan, masing-masing [63,78]. Akhirnya, Wu et al. mendapati bahawa senaman digabungkan dengan diet yang diperkaya dengan asid docosahexaenoic, fosfolipid membran plasma, meningkatkan ekspresi protein BDNF berbanding haiwan tanpa diet diperkaya dan haiwan tidak aktif. Kebanyakan kajian mendapati bahawa senaman juga meningkatkan hasil berfungsi selepas kecederaan. Satu kajian menggunakan sistem roda larian pengesan inframerah dan melatih tikus selama tiga hari sebelum pembedahan dan tiga minggu selepas itu. Mereka mendapati bahawa latihan itu meningkatkan ingatan jangka pendek yang memburukkan ketakutan dan ingatan spatial yang diuji oleh ujian pengelakan pasif dan ujian Y-Maze [69]. Kajian yang sama juga meneliti gen HSP20, gen yang mengekspresikan protein kejutan haba 20 yang merupakan pendamping yang sebelum ini diketahui dinyatakan selepas tekanan tisu dan menjadi pelindung dalam contohnya, penyakit Alzheimer. Mereka mendapati bahawa pembungkaman gen HSP20 membatalkan peningkatan yang disebabkan oleh senaman. Tiga kajian yang mengkaji senaman mendapati korelasi antara ekspresi protein BDNF yang lebih baik (dan satu kajian mendapati bahawa senaman meningkatkan ekspresi mRNA BDNF) dan fungsi kognitif yang lebih baik dalam ujian Morris Water Maze [64,67,68,71]. Griesbach et al. menunjukkan bahawa tikus yang bersenam menunjukkan prestasi yang lebih baik dalam ujian maze air Morris selepas kecederaan berbanding dengan tikus yang tidak bersenam dan tikus yang cedera yang menerima antibodi TrkB-IgG yang tidak aktif tidak mendapat manfaat daripada senaman, seterusnya mencadangkan bahawa senaman memberikan kesan pemulihannya melalui laluan BDNF. [67].
Da Silva Fiorin et al. dan Zhao et al. adalah satu-satunya yang mengkaji kesan senaman pra-traumatik. da Silva Fiorin et al. mendapati bahawa walaupun FPI sahaja tidak mempunyai kesan yang ketara pada ekspresi protein BDNF, senaman fizikal sebelum ini menyebabkan peningkatan dalam ekspresi protein BDNF dalam hippocampus pada 1 dan 14 DPI. Zhao et al. mendapati bahawa senaman roda berjalan selama 4 minggu sebelum trauma meningkatkan ekspresi mRNA BDNF dalam korteks ipsilateral kedua-dua haiwan palsu dan cedera berbanding haiwan yang tidak bersenam. Mereka juga mendapati bahawa senaman pra-traumatik meningkatkan fungsi motor dalam ujian berjalan rasuk dan fungsi kognitif dalam maze air Morris dan ujian pengecaman objek baru.
Griesbach et al, menggunakan senaman roda sukarela dan memeriksa hasil kefungsian selepas perkusi cecair sisi dan mendapati tiada kesan yang ketara ke atas kerosakan motor kasar. Shen et al. memeriksa model latihan intensiti yang berbeza dan memeriksa hasil fungsi selepas kesan kortikal terkawal yang teruk dan mendapati bahawa walaupun tiada perbezaan yang ketara antara kumpulan trauma dalamNeurologiSkor Defisit, haiwan senaman intensiti rendah menunjukkan prestasi yang lebih baik dalam MWM berbanding haiwan senaman kawalan dan intensiti tinggi. Griesbach et al. menggunakan model kecederaan perkusi cecair sisi dengan senaman roda sukarela dan mendapati tiada kesan senaman yang ketara pada ekspresi BDNF mahupun keputusan ujian rasuk berjalan [59,68,78]. Hicks et al. mendapati bahawa kecederaan perkusi cecair menurunkan fungsi dengan ketara dalam NSS dan MWM, dan senaman selepas trauma meningkatkan ekspresi protein BDNF tetapi tidak mempunyai kesan yang ketara pada NSS atau MWM [92].
Sila klik di sini untuk Bahagian 2

