LNK Farnesyltransferase Inhibitor-754 Melemahkan Distrofi Akson Dan Mengurangkan Patologi Amyloid dalam Tikus Bahagian 4
Sep 26, 2023
LNK‑754 dan lonafarnib meningkatkan pemerdagangan endolisosomal akson dalam neuron berbudaya
Untuk menyiasat mekanisme LNK-754 untuk mengurangkan pengumpulan LAMP1, BACE1 dan LT dalam neurit distrofik dalam tikus 5XFAD, kami melakukan kajian in vitro menggunakan neuron kultur primer tikus jenis liar. Kami mula-mula menilai corak pengedaran organel endolisosomal dalam neuron yang dirawat dengan kenderaan, LNK-754, atau lonafarnib oleh mikroskopi imunofluoresensi confocal. Dalam neuron yang dirawat kenderaan, vesikel pendarfluor LAMP1 tertumpu kebanyakannya dalam badan sel dan neurit proksimal, manakala dalam neuron LNK-754 dan lonafarnib yang dirawat, vesikel LAMP1 meningkat di kawasan neurit proksimal dan distal berbanding dengan neuron yang dirawat kenderaan ( Rajah 6A-F).
Sama seperti keputusan in vivo kami dan dalam persetujuan dengan laporan sebelumnya [9], peningkatan jumlah LAMP1 juga terdapat dalam LNK-754 dan kultur yang dirawat lonafarnib (Rajah 6F-H). Rawatan Lonafarnib dengan ketara meningkatkan jumlah penyetempatan LAMP1 dan LAMP1 kepada neurit, manakala arah aliran diperhatikan untuk rawatan LNK-754 (Rajah 6D, F). LAMP1 secara tidak spesifik menandakan pelbagai vesikel endosom dan autofagik, jadi kami seterusnya menganalisis penyetempatan dan pengasidan endosom dan lisosom lewat dalam kultur neuron hidup yang dirawat dengan LysoSensor Green, pewarna pendarfluor yang menunjukkan peningkatan yang bergantung kepada pH dalam intensiti pendarfluor dalam petak berasid.
Neurit adalah salah satu struktur berfungsi penting dalam sel saraf, yang boleh menghantar isyarat saraf dan berkomunikasi dengan sel lain. Dalam neurit, LAMP1 adalah protein membran penting yang mengambil bahagian dalam proses pengangkutan sistem membran intraselular dan mengambil bahagian dalam pembentukan autophagy dan vesikel. Selain itu, kajian menunjukkan LAMP1 juga berkait rapat dengan imuniti.
Beberapa kajian mendapati LAMP1 memainkan peranan penting dalam penyakit seperti tumor, jangkitan dan keradangan. Ekspresi LAMP1 berkait rapat dengan pencerobohan tumor, metastasis, dan prognosis. Pada masa yang sama, LAMP1 juga boleh mengambil bahagian dalam tindak balas imun badan. Penyelidik mendapati bahawa LAMP1 boleh menggalakkan pengaktifan sel T dan sel pembunuh semulajadi dan meningkatkan keupayaan membunuh mereka. Selain itu, LAMP1 juga boleh menggalakkan pembersihan badan daripada patogen dan meningkatkan tindak balas imun.
Selain itu, LAMP1 juga berkaitan dengan kejadian beberapa penyakit autoimun. Sebagai contoh, tahap ekspresi LAMP1 meningkat dengan ketara dalam penyakit autoimun seperti lupus erythematosus sistemik. Di samping itu, penyelidik juga mendapati bahawa sesetengah pesakit dengan penyakit autoimun juga mempunyai tahap antibodi anti-LAMP1 yang lebih tinggi, menunjukkan bahawa LAMP1 mungkin berkaitan dengan kejadian tindak balas autoimun.
Secara ringkasnya, peranan LAMP1 dalam neurit tidak terhad kepada fungsi sistem saraf tetapi juga termasuk tindak balas imun badan. Walaupun penyelidikan berkaitan LAMP1 masih di peringkat awal, ia mungkin menjadi sasaran baharu untuk mencegah dan merawat beberapa penyakit pada masa hadapan. Kajian lanjut mengenai hubungan antara LAMP1 dan imuniti akan memberikan idea dan peluang baharu untuk pembangunan ubat baharu. Dapat dilihat bahawa kita perlu meningkatkan daya ingatan. Cistanche deserticola boleh meningkatkan ingatan dengan ketara, kerana Cistanche deserticola juga boleh mengawal keseimbangan neurotransmitter, seperti meningkatkan tahap asetilkolin dan faktor pertumbuhan. Bahan-bahan ini sangat penting untuk ingatan dan pembelajaran. Di samping itu, daging juga boleh meningkatkan aliran darah dan menggalakkan penghantaran oksigen, yang dapat memastikan otak menerima nutrien dan tenaga yang mencukupi, sekali gus meningkatkan daya hidup dan daya tahan otak.

Klik Tahu untuk meningkatkan ingatan jangka pendek
Jumlah keamatan pendarfluor Hijau LysoSensor tidak berubah dalam neuron yang dirawat dengan kenderaan, LNK-754 atau lonafarnib (Rajah 6I, J). Selaras dengan penemuan kami untuk LAMP1, penyetempatan vesikel LysoSensor meningkat dalam neurit distal LNK-754 atau kultur yang dirawat lonafarnib (Rajah 6I, anak panah).
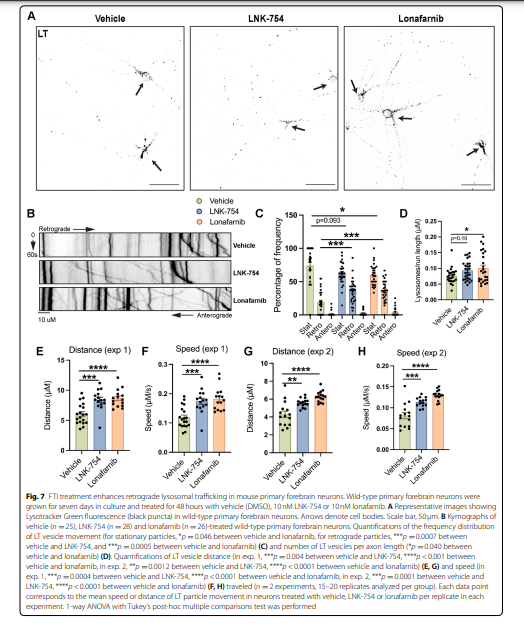
Peratusan besar vesikel LAMP1-positif telah disetempatkan kepada neurit proksimal dan distal dalam neuron yang dirawat FTI, menunjukkan bahawa perencatan FTase menjejaskan motilitas organel endolisosomal. Kami menilai kesan rawatan FTI ke atas dinamik endosom dan lisosom lewat melalui pengimejan selang masa bagi kultur neuron primer jenis liar hidup yang diwarnai dengan LT (Rajah 7A).
Analisis Kymograph bagi vesikel LT axonal mendedahkan bahawa, di bawah semua keadaan rawatan, kebanyakan vesikel LT axonal adalah pegun, atau bergerak dalam halaju rendah, arah retrograde (Rajah 7B). Walau bagaimanapun, terdapat perubahan yang kuat dalam peratusan vesikel LT akson pegun, retrogred dan anterogred dalam LNK-754 dan neuron yang dirawat lonafarnib. Peratusan vesikel LT retrograde dalam LNK-754 (36%) atau lonafarnib (36%) neuron yang dirawat adalah jauh lebih tinggi daripada neuron yang dirawat kenderaan (19%) manakala peratusan vesikel LT pegun dalam LNK{{7 }} (62%) atau lonafarnib (60%) neuron yang dirawat adalah lebih rendah berbanding dengan neuron yang dirawat kenderaan (74%) (Rajah 7C).
Peningkatan ketara dalam bilangan vesikel LT setiap panjang akson diperhatikan dalam neuron yang dirawat lonafarnib dan trend diperhatikan untuk rawatan LNK-754 (Rajah 7D), seperti dalam taburan LAMP1 (Rajah 6A-D). ) dan LysoSensor (Rajah 6I, J). Jarak yang dilalui oleh vesikel LT meningkat dengan ketara dalam LNK-754 dan neuron yang dirawat lonafarnib (Rajah 7E, G) dan halaju purata vesikel LT adalah lebih pantas dengan ketara dalam LNK{{10}} (0.17μm/s) dan lonafarnib (0.18μm/s) merawat neuron berbanding neuron yang dirawat kenderaan (0.11μm/s) (Rajah 7F, H; filem S1, S2, S3 ). Bersama-sama dengan keputusan kami daripada tikus 5XFAD yang dirawat FTI, data ini menyokong peranan FTase dalam mengawal selia penjanaan dan motilitas akson endosom dan lisosom lewat.
Perbincangan
Banyak penyakit neurodegeneratif dicirikan oleh sistem lisosom terjejas dan pembentukan agregat protein khusus penyakit. Otak AD khususnya menunjukkan disfungsi lisosom yang meluas dan boleh dibezakan daripada penyakit neurodegeneratif lain dengan pengumpulan organel autofagik dan endolisosomal dalam neurit distrofik yang diperbesarkan mengelilingi plak amiloid [54].
FTI adalah calon terapeutik yang menjanjikan untuk digunakan semula ke arah merawat penyakit neurodegeneratif yang berkongsi patologi disfungsi lisosom dan pengumpulan protein. Dengan meningkatkan fungsi lisosom, FTI boleh mempunyai kesan terapeutik yang ketara pada neurit distrofik dalam otak AD. Walau bagaimanapun, sehingga kini, kesan FTI terhadap patologi A dan distrofi aksonal masih belum diuji secara in vivo.

Kami menentukan kesan FTI penembus otak LNK754 dan lonafarnib pada patologi berkaitan AD dalam model tetikus 5XFAD dan membentangkan data baharu yang menunjukkan bahawa rawatan kronik tikus 5XFAD dengan LNK-754 mengurangkan beban plak amiloid dan melemahkan pembentukan neurit distrofik. Walaupun bukan fokus langsung dalam kajian ini, rawatan LNK-754 dan lonafarnib juga mengurangkan hiperfosforilasi tau dalam otak tikus 5XFAD. Berbeza dengan penemuan kami untuk LNK-754, tikus 5XFAD yang dirawat lonafarnib hanya menunjukkan sedikit peningkatan dalam patologi ADrelevan, dan secara konsisten, penanda perencatan FTase kebanyakannya tidak berubah dalam otak tikus lonafarnib.
LNK-754 dan lonafarnib kedua-duanya berkesan secara in vitro; bilangan dan halaju organel endolisosomal axonal yang diperdagangkan ke arah retrograde telah meningkat secara mendadak dalam neuron primer kultur hidup. LNK-754 dan lonafarnib juga meningkatkan tahap penanda endolisosomal LAMP1 dalam kultur neuron primer dan otak tikus 5XFAD. Tus, rawatan FTI merangsang biogenesis endolisosomal dan pemerdagangan aksonal retrograde endosom lewat dan lisosom secara in vitro, yang mungkin telah memperlahankan degenerasi akson dan menghalang pembentukan neurit dystrophik dan pemendapan plak dalam tikus 5XFAD. Terutama, LNK-754 mengurangkan pengumpulan BACE1 dalam neurit distrofik dan menyekat laluan suapan ke hadapan distrofi aksonal, generasi A 42 dan pemendapan plak. Keputusan kami bersetuju dengan laporan sebelumnya yang menunjuk kepada FTase sebagai sasaran terapeutik untuk merawat proteinopati dan mencadangkan bahawa FTI menyasarkan neurit distrofik dengan meningkatkan fungsi lisosom dan menggalakkan pemerdagangan endolisosom.
Kami membandingkan FTI penembus otak LNK-754 dan lonafarnib kerana kedua-duanya diketahui mengaktifkan lisosom dan autofagi dalam model tetikus proteinopati dan telah disiasat secara klinikal untuk rawatan kanser [8, 9, 41, 55–57]. Lonafarnib sangat diminati kerana ia mengurangkan kemasukan tau dengan ketara [9], diluluskan oleh FDA untuk rawatan progeria, dan mempunyai profil keselamatan dan kejadian buruk yang diketahui pada manusia [57]. Namun begitu, kami mendapati bahawa LNK{10}} jauh lebih berkesan daripada lonafarnib dalam memperbaik patologi AD tetikus 5XFAD.
Bukti bahawa kedua-dua LNK {{0}} dan lonafarnib melintasi halangan otak darah telah diperoleh daripada ujian kanser klinikal manusia [41, 57] tetapi perbandingan kebolehtelapan LNK-754 dan lonafarnib otak darah dalam Tikus 5XFAD masih belum dilakukan, jadi boleh dibayangkan lonafarnib tidak melepasi halangan otak darah secekap LNK-754. Percanggahan antara LNK-754 dan lonafarnib juga mungkin disebabkan oleh perbezaan potensi LNK-754 dan lonafarnib, kerana perencatan IC50 untuk H-Ras ialah 0.57nM untuk LNK-754 [41] dan 1.9nM untuk lonafarnib [51]. Kami dengan mudah mengesan perubahan dalam penanda perencatan FTase yang diketahui dalam otak tikus 5XFAD yang dirawat LNK754-tetapi tidak pada tikus lonafarnib, menyokong idea bahawa dos lonafarnib yang lebih tinggi mungkin diperlukan untuk mencapai kesan terapeutik.


Dos FTI yang tinggi diperlukan untuk menyekat fanesilasi Ras secara maksimum serta protein substrat CAAX FTase kanonik yang lain. Rejimen rawatan dos rendah (1mg/kg/hari) diikuti dalam kajian ini kerana bukti menunjukkan bahawa dos FTI yang rendah boleh mengaktifkan substrat protein bukan kanonik yang terlibat dalam laluan pelepasan protein [8, 28]. Tambahan pula, rawatan dos rendah pada pesakit boleh mengelakkan kesan sampingan yang biasanya dilihat dengan perencatan Ras yang tinggi. Rawatan LNK-754 (0.9mg/kg/hari) mengurangkan -syn dalam otak tikus transgenik PD dan peningkatan aktiviti lisosom melebihi paras asas dalam tikus jenis liar [8]. Sebaliknya, rawatan sekejap lonafarnib oleh gavage oral pada dos yang jauh lebih tinggi (80mg/kg/hari) adalah perlu untuk menghalang pengagregatan tau [9].
Dos lonafarnib yang lebih tinggi mungkin diperlukan untuk meningkatkan kedua-dua fungsi endolisosomal dan pemerdagangan aksonal kerana kami mendapati paras LAMP1 yang tinggi dalam otak tikus yang dirawat lonafarnib tetapi kesan minimum terhadap distrofi dan beban plak. Kami menguji hanya satu dos FTI, dan kajian lanjut akan diperlukan untuk menentukan dos dan laluan pentadbiran yang diperlukan untuk mencapai pengurangan optimum A dan patologi neurit distrofik. Kesan in vitro LNK-754 dan lonafarnib adalah konsisten, menunjukkan bahawa lonafarnib akan menjana fenotip serupa dalam tikus 5XFAD jika aktiviti perencat yang setanding pada FTase dicapai.
Ada kemungkinan bahawa pendedahan dadah dalam kultur sel lebih serupa untuk kedua-dua sebatian, berbanding model in vivo.
Jika perencatan FTase yang setanding berlaku dalam vivo, kemungkinan lain ialah LNK-754 dan lonafarnib mengubah proteom berfarnesilasi dalam otak 5XFAD dengan cara yang berbeza. Ini telah diperhatikan dalam garisan sel leukemia, di mana perbezaan yang jelas dalam protein terfarnesilasi dilaporkan selepas rawatan dengan FTI BMS241,662 dan L-778,123 [24]. Selain itu, kajian ini menunjukkan corak unik fanesilasi dalam garisan sel yang berbeza, menunjukkan bahawa proteom berfarnesilasi tertentu boleh wujud dalam setiap jenis sel, yang boleh memburukkan lagi perbezaan kecil dalam perencatan farnesilasi protein antara LNK-754 dan lonafarnib. Oleh itu, ada kemungkinan bahawa protein farnesylated secara khusus dihalang oleh LNK754, tetapi bukan lonafarnib, bertanggungjawab untuk pengantara pengurangan plak dan distrofi.

Kemungkinan alternatif, walaupun tidak mungkin [58], adalah perencatan sasaran geranil-geranil transferase (GGTase) oleh LNK-754 atau lonafarnib boleh mengakibatkan perencatan pembezaan substrat yang dikawal oleh GGTase. Akhir sekali, laluan pranilasi untuk substrat yang terlibat dalam pengurangan plak boleh diaktifkan dalam tikus yang dirawat lonafarnib tetapi bukan tikus LNK-754. Berkemungkinan perencatan serentak berbilang substrat oleh LNK-754 membawa kepada pengurangan plak dalam tikus 5XFAD dan sebahagian atau semua substrat ini tidak dihalang dalam tikus lonafarnib. Untuk mengenal pasti mekanisme substrat berfarnesilasi dalam mengawal pertumbuhan plak dan pembenihan, eksperimen masa depan harus dilakukan untuk mengenal pasti substrat mana yang paling berkurangan di kawasan otak hippocampal dan kortikal, dan mengaitkan dengan penurunan beban plak dan distrofi dalam otak LNK-754 dan lonafarnib merawat tikus 5XFAD.
Satu trend telah diperhatikan sepanjang kajian kronik kami di mana perbezaan ketara ditemui antara kenderaan dan LNK-754 dalam korteks dan antara lonafarnib dan LNK-754 dalam hippocampus. Kami melihat penurunan ketara dalam plak dan kawasan otak kortikal distrofi antara kenderaan dan tikus yang dirawat LNK-754, manakala perbezaan ketara antara LNK-754 dan lonafarnib ditemui dalam hippocampus. Patologi amiloid bermula pada lapisan 5 neuron kortikal dan paling teruk di kawasan otak ini [36] jadi kami mengesyaki ini disebabkan oleh bilangan plak yang rendah dalam hippocampus dan kebolehubahan dalam beban plak dalam tikus 5XFAD. Kami menjangkakan bahawa keputusan kami akan mencapai kepentingan statistik antara LNK754 dan kenderaan untuk semua hasil dengan meningkatkan panjang rawatan atau menilai tikus pada usia lanjut apabila lebih banyak plak akan ditemui di hippocampus. Walau bagaimanapun, mekanisme yang berbeza mungkin berlaku antara hippocampus dan korteks dalam tikus-754-LNK yang dirawat. Sebagai contoh, perbezaan dalam tahap fisiologi FTase dalam sel yang tertumpu di hippocampus berbanding dengan korteks, atau ekspresi pembezaan substrat FTase mungkin wujud antara hippocampus dan korteks.
Untuk menyiasat mekanisme LNK-754 untuk mengurangkan patologi amiloid dalam tikus 5XFAD, kami menumpukan kajian kami secara khusus pada neurit distrofik. Neurit distrofik mengandungi tahap LAMP1 dan BACE1 yang tinggi dan menyumbang dengan ketara kepada pemendapan plak ekstraselular dan distrofi aksonal, mengakibatkan kehilangan sinaptik, neurodegenerasi, dan defisit kognitif [14, 16, 18]. Dengan menilai berbilang penanda neurit distrofik, termasuk LAMP1, BACE1 dan LT, kami mendapati bahawa plak bersaiz sama mempunyai lebih sedikit distrofi pada tikus LNK-754 berbanding tikus yang dirawat dengan kenderaan atau lonafarnib. Pengurangan sederhana dalam nisbah LAMP1:A 42 setiap plak diperhatikan berbanding dengan penurunan yang lebih besar bagi penanda neurit distrofik lain dalam tikus yang dirawat LNK{13}}, mungkin kerana sebahagian daripada LAMP1 yang dikaitkan dengan plak terdapat dalam mikroglia [59 ].
LT terkumpul dalam distrofi di sekeliling plak dalam tisu otak tikus hidup (Rajah 4A), menunjukkan bahawa endosom dan lisosom lewat yang sangat berasid terdapat dalam neurit distrofik. Tambahan pula, kami menunjukkan bahawa rawatan LNK-754 mempunyai kesan dramatik terhadap penurunan nisbah LT: TR, berbanding nisbah LAMP1:A 42. Berdasarkan penemuan kami dengan pewarnaan LT, kami membuat hipotesis bahawa subset LAMP 1-vesikel positif yang dikurangkan dalam LNK-754 tikus yang dirawat secara kronik ialah endosom dan lisosom lewat berasid.
Paling penting, LNK-754 menghalang pengumpulan abnormal BACE1 dalam distrofi. Menghalang aktiviti BACE1 dalam neurit distrofik pada peringkat awal pemendapan A menyekat pembentukan plak baharu, dan bukannya pertumbuhan plak asal [18], jadi mekanisme serupa boleh berlaku pada tikus yang dirawat LNK-754. Dalam model tetikus APP/PS1, dataran neurit distrofik selepas plak mencapai jejari 10μm, yang boleh dijelaskan oleh kehilangan akson lengkap yang seimbang dengan penjanaan neurit distrofik [18]. Korelasi positif antara LAMP1 dan beban plak selepas rawatan LNK-754 kronik dan saiz LT dan plak selepas rawatan LNK-754 akut, boleh disebabkan oleh peralihan dalam keseimbangan kehilangan dan penjanaan distrofi, peningkatan dalam bilangan atau saiz akson dan neuron yang berdaya maju di sekeliling plak, atau penurunan dalam banyaknya plak besar.
Penemuan utama kajian kami ialah LNK-754 dan lonafarnib secara dramatik mempertingkatkan pemerdagangan aksonal retrograde bagi petak endolisosomal. Telah dilaporkan bahawa FTI, termasuk lonafarnib, meningkatkan asetilasi MT dan kestabilan dalam talian sel kanser [31, 32, 60]. Oleh itu, pemerdagangan petak endolisosomal yang dipertingkatkan dalam kajian kami berpotensi dimediasi melalui substrat yang bertanggungjawab untuk kesan penstabilan MT bagi FTI. Menariknya, kesan sinergistik antara agen penstabil MT tradisional dan FTI telah didokumenkan dengan baik dalam tetapan kanser [32, 33, 61], yang menimbulkan kemungkinan menarik bahawa rawatan yang sama boleh menghalang pembentukan neurit distrofik dalam otak AD. Kesan tambahan untuk meningkatkan kapasiti degradasi lisosom dan pemerdagangan petak ini berkemungkinan menggalakkan penyasaran BACE1 kepada lisosom matang untuk degradasi.
Perlu diperhatikan bahawa rawatan akut dengan LNK-754 melemahkan neurit distrofik dalam tikus 5XFAD berumur dan meningkatkan pembelajaran dan ingatan spatial dalam tikus hAPP/PS1. Ini menyokong dua peranan FTI dalam rawatan AD, dengan menghalang generasi A dan melindungi daripada neurit distrofik dan penurunan kognitif selepas pemendapan plak lanjutan. Selaras dengan ini, haplodeficiency FTase khususnya dalam tikus APP/PS1 menyelamatkan kemerosotan kognitif, manakala kekurangan FTase atau GGTase kedua-duanya mengurangkan pemendapan A [62]. Selanjutnya, tahap farnesilation telah ditunjukkan untuk mengawal keplastikan sinaptik dan ketumpatan tulang belakang dalam hirisan hippocampal dalam tikus jenis liar [63], jadi protein farnesylated secara khusus boleh mengubah keplastikan sinaptik dan kestabilan mikrotubulus, dan substrat ini boleh berfungsi secara bebas daripada substrat berprenilasi lain yang mempengaruhi pemendapan plak.
Walaupun kami membuat hipotesis bahawa substrat berfarnesilasi mengawal kestabilan mikrotubulus dan fungsi endolyosom meningkatkan neurit distrofik dan tingkah laku menyelamat dalam tetikus APP/PS1, mekanisme lain adalah mungkin. Sebagai contoh, Rhes ialah GTPase kecil yang mengalami farnesylation dan diketahui menyebabkan autophagy [64]. Rhes mengantarkan peningkatan tingkah laku dalam tikus transgenik tau dengan menurunkan tahap fosfo-tau [9], dan begitu juga Rhes boleh bertanggungjawab untuk meningkatkan ingatan dalam tetikus hAPP/PS1 yang dirawat LNK754 dengan mengurangkan fosforilasi tau (cth, p-tau ser404), seperti yang diperhatikan dalam LNK-754 merawat tikus 5XFAD, secara bebas daripada peningkatan neurit distrofik.
Farneslyation adalah penting untuk berfungsi dengan baik pelbagai protein yang berkaitan secara fisiologi yang boleh bertanggungjawab untuk mengantarkan kesan berfaedah yang diperhatikan dalam kajian kami. Lebih daripada 32 substrat berfarnesilasi baru-baru ini dikenal pasti melalui pelabelan metabolik dalam garisan sel endothelial manusia [65], dan dalam satu lagi kajian baru-baru ini, 11 protein berfarnesilasi telah diperkayakan dalam tikus kalah mati FTase khusus-neuron-forebrain [63]. Keluarga utama protein yang terjejas dalam neuron otak depan oleh farnesilation ialah Ras GTPases [63], yang mengantara banyak fungsi selular termasuk pemerdagangan endosomal. Protein Ras terlibat dalam patogenesis AD; dalam tisu otak postmortem pesakit dengan AD dan gangguan kognitif ringan, peningkatan pengaktifan isyarat Ras berkorelasi dengan patologi amiloid dan tahap peningkatan molekul isyarat hilirannya ERK [30].
Tambahan pula, ahli keluarga Ras Rhes dikenal pasti sebagai sasaran lonafarnib untuk mengaktifkan lisosom dan mengurangkan agregat tau mutan [9]. Transkripptomik kalah mati FTase neuron dalam tikus APP/PS1 mengenal pasti isyarat mTORC1 dan promosi pemprosesan bukan amyloidogenik sebagai penyumbang utama kepada kesan berfaedah pada kognisi dan patologi amiloid, mungkin dimediasi melalui pengurangan isyarat Ras atau Rheb [30]. Perubahan dalam aktiviti Rhes atau Rheb boleh mengurangkan beban A dalam tikus 5XFAD, walaupun tidak mungkin Ras telah dinyahaktifkan sepenuhnya pada kepekatan LNK-754 dan lonafarnib yang digunakan dalam kajian ini. Beberapa substrat non-Ras FTase bukan kanonik sebaliknya boleh mengantara kesan yang diperhatikan. Sebagai contoh, protein SNARE ykt6 meningkatkan pemerdagangan hidrolase lisosom dan boleh menggalakkan fungsi lisosom [8]. Kesan FTase langsung juga boleh bertanggungjawab, kerana FTase boleh mengikat mikrotubulus secara langsung dan menjejaskan aktiviti deacetylase histon HDAC6, dengan itu menghalang deasetilasi tubulin [33].
Kesimpulan
Penyelarasan isyarat FTase dan farnesylation protein nampaknya merupakan peristiwa permulaan awal dalam patogenesis AD [30]. Dalam kajian ini, kami mengambil pendekatan farmakologi untuk menghalang FTase dalam vivo dalam model tetikus 5XFAD. Dalam model tetikus synucleinopathies dan tauopathies, agregat protein toksik telah dibersihkan secara langsung oleh degradasi lisosom yang dipertingkatkan yang disebabkan oleh rawatan FTI [8, 9]. Sebaliknya, kami membuat hipotesis bahawa generasi A telah dihalang melalui mekanisme tidak langsung yang mempertingkatkan pemerdagangan aksonal menghalang pembentukan neurit distrofik dan ketinggian BACE1. Selepas bermulanya patologi plak, rawatan LNK-754 jangka pendek mengurangkan neurit distrofik dalam tikus 5XFAD dan meningkatkan ingatan serta tingkah laku pembelajaran ruang dalam tikus hAPP/PS1.

Keputusan kami menyediakan kajian bukti konsep terhadap penggunaan FTI untuk mencegah pengumpulan A dan menambah kepada badan kerja yang besar yang telah menunjukkan penurunan genetik FTase meningkatkan patologi amiloid dan menyelamatkan fungsi kognitif dalam model tetikus AD [30, 62, 66 ]. Substrat FTase khusus dan laluan hiliran yang bertanggungjawab untuk fenotip yang diperhatikan dalam kajian kami harus dijelaskan lebih lanjut dalam kajian masa depan. Menurunkan pembentukan BACE1 dalam neurit distrofik dengan rawatan FTI boleh melambatkan pemendapan A 42 sambil menawarkan strategi terapeutik yang mengelakkan kesan sampingan sasaran yang biasanya dilihat apabila menggunakan perencat BACE1 [67, 68]. Tambahan pula, mengurangkan beban plak amiloid di otak mungkin akan meramalkan manfaat klinikal pesakit AD [67], dan oleh itu, FTI boleh mempunyai implikasi terapeutik yang penting untuk AD.


Ucapan terima kasih
Kami mengucapkan terima kasih kepada D. Kirchenbuechler, P. Dluhy, dan C. Arvanitis dari Pusat Mikroskopi Lanjutan di Northwestern University untuk nasihat pakar tentang kuantifikasi imej imunofluoresensi dan perbincangan yang berguna, dan sokongan pembiayaan daripada NIH R01 AG030142. Akhir sekali, kami mengucapkan terima kasih kepada S. Kemal dan J. Popovic dari makmal Vassar atas kepakaran dan bantuan mereka masing-masing dengan eksperimen pengimejan langsung dan perfusi tetikus.
Butiran Pengarang
Jabatan Neurologi Ken dan Ruth Davee, Northwestern University Feinberg School of Medicine, Chicago, IL 60611, Amerika Syarikat. 2 BioEnergetics, Boston, MA 02115, Amerika Syarikat. 3 Bial Biotech, Cambridge, MA 02139, Amerika Syarikat. 4 Jabatan Neurologi, Sekolah Perubatan Harvard, Cambridge, MA 02139, Amerika Syarikat. 5 Pusat Mesulam untuk Neurologi Kognitif dan Penyakit Alzheimer, Northwestern University Feinberg School of Medicine, Chicago, IL 60611, Amerika Syarikat.
Rujukan
1. Hardy J, Allsop D. Pemendapan amiloid sebagai peristiwa utama dalam etiologi penyakit Alzheimer. Trends Pharmacol Sci. 1991;12(10):383–8.
2. Hardy J, Selkoe DJ. Hipotesis amiloid penyakit Alzheimer: kemajuan dan masalah di jalan menuju terapeutik. Sains. 2002;297(5580):353–6.
3. Selkoe DJ. Patologi molekul penyakit Alzheimer. Neuron. 1991;6(4):487–98.
4. Liu PP, Xie Y, Meng XY, Kang JS. Sejarah dan kemajuan hipotesis dan ujian klinikal untuk penyakit Alzheimer. Sasaran Transduksi Isyarat Di sana. 2019;4:29.
5. Sevigny J, Chiao P, Bussière T, Weinreb PH, Williams L, Maier M, et al. Antibodi aducanumab mengurangkan plak A dalam penyakit Alzheimer. alam semula jadi. 2016;537(7618):50–6.
6. Cuddy LK, Prokopenko D, Cunningham EP, Brimberry R, Song P, Kirchner R, et al. A -percepatan neurodegenerasi yang disebabkan oleh Alzheimer 's-related. Sci Transl Med. 2020;12(563):eaaz2541.
7. Cummings J, Lee G, Ritter A, Sabbagh M, Zhong K. Talian pembangunan ubat penyakit Alzheimer: 2020. Alzheimers Dement (NY). 2020;6(1):e12050.
8. Cuddy LK, Wani WY, Morella ML, Pitcairn C, Tsutsumi K, Fredriksen K, et al. Pelepasan selular yang disebabkan oleh tekanan dimediasi oleh protein SNARE ykt6 dan diganggu oleh -Synuclein. Neuron. 2019;104(5):869–84.e11.
9. Hernandez I, Luna G, Rauch JN, Reis SA, Giroux M, Karch CM, et al. Perencat farnesyltransferase mengaktifkan lisosom dan mengurangkan patologi tau pada tikus dengan tauopati. Sci Transl Med. 2019;11(485):eaat3005.
10. Mazzulli JR, Zunke F, Tsunemi T, Toker NJ, Jeon S, Burbulla LF, et al. Pengaktifan -Glucocerebrosidase mengurangkan patologi -Synuclein dan memulihkan fungsi lisosom dalam neuron otak tengah pesakit Parkinson. J Neurosci. 2016;36(29):7693–706.
11. Nixon RA. Peranan autophagy dalam penyakit neurodegeneratif. Nat Med. 2013;19(8):983–97. 12. Bonam SR, Wang F, Muller S. Lysosomes sebagai sasaran terapeutik. Nat Rev Drug Discov. 2019;18(12):923–48.
For more information:1950477648nn@gmail.com






