Kemodiversiti Sampel Propolis Dikumpul di Pelbagai Kawasan Benin Dan Congo: Pemprofilan Kromatografi Dan Pencirian Kimia Berpandukan Dereplikasi 13C NMR Bahagian 2
Jun 06, 2023
3.3 Komposisi kimia CG
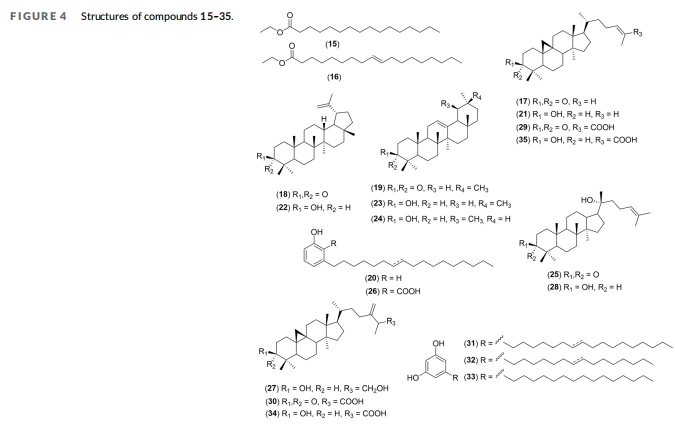
Untuk CG, EEP dari Congo, GC-MS tidak cukup berkesan untuk mengenal pasti secara langsung semua juzuk yang berbeza tetapi membenarkan kami mencirikan beberapa kelas kimia, termasuk ester lemak, derivatif fenol dan resorsinol, dan triterpenoid. Maklumat struktur ini mendorong kami untuk menggunakan dereplikasi berasaskan 13C NMR menggunakan DB tersuai, iaitu, DB4 dan DB5. Oleh itu, kromatografi kilat dilakukan pada CG EEP dan pecahan dikumpulkan menggunakan TLC dengan pendedahan vanillin sulfurik (rujuk Rajah SI-24). Dereplikasi 13C NMR dengan perisian MixONat dilakukan pada pecahan yang berbeza menggunakan DB4 dan DB5, diikuti dengan perbandingan dengan literatur untuk pengesahan. Selain itu, data GC-MS membenarkan kami menentukan MW NP utama, yang digunakan dengan perisian MixONat untuk memperbaiki hipotesis struktur (Jadual 4, Rajah 4).
Glikosida cistanche juga boleh meningkatkan aktiviti SOD dalam tisu jantung dan hati, dan dengan ketara mengurangkan kandungan lipofuscin dan MDA dalam setiap tisu, dengan berkesan menghilangkan pelbagai radikal oksigen reaktif (OH-, H₂O₂, dll.) dan melindungi daripada kerosakan DNA yang disebabkan oleh OH-radikal. Glikosida phenylethanoid cistanche mempunyai keupayaan penghapusan radikal bebas yang kuat, keupayaan pengurangan yang lebih tinggi daripada vitamin C, meningkatkan aktiviti SOD dalam penggantungan sperma, mengurangkan kandungan MDA, dan mempunyai kesan perlindungan tertentu pada fungsi membran sperma. Polisakarida cistanche boleh meningkatkan aktiviti SOD dan GSH-Px dalam eritrosit dan tisu paru-paru tikus senescent eksperimen yang disebabkan oleh D-galaktosa, serta mengurangkan kandungan MDA dan kolagen dalam paru-paru dan plasma, dan meningkatkan kandungan elastin, mempunyai kesan penghapusan yang baik pada DPPH, memanjangkan masa hipoksia pada tikus senescent, meningkatkan aktiviti SOD dalam serum, dan melambatkan degenerasi fisiologi paru-paru dalam tikus senescent secara eksperimen Dengan degenerasi morfologi selular, eksperimen telah menunjukkan bahawa Cistanche mempunyai keupayaan antioksidan yang baik. dan berpotensi menjadi ubat untuk mencegah dan merawat penyakit penuaan kulit. Pada masa yang sama, echinacoside dalam Cistanche mempunyai keupayaan yang ketara untuk menghilangkan radikal bebas DPPH dan boleh menghilangkan spesies oksigen reaktif, menghalang degradasi kolagen yang disebabkan oleh radikal bebas, dan juga mempunyai kesan pembaikan yang baik pada kerosakan anion radikal bebas timin.

Klik pada Di Mana Saya Boleh Beli Cistanche
【Untuk maklumat lanjut: david.deng@wecistanche.com / WhatApp:86 13632399501】
Seperti yang dijangkakan, ester lemak seperti etil ester asid palmitik (15) dan etil ester asid oleik (16), sebatian CG yang paling meruap, telah disahkan dalam CG_F2 sebanyak 1 H NMR seperti yang dihipotesiskan oleh GC-MS . Untuk CG_F3, dereplikasi 13C NMR menggunakan perisian MixONat dengan triterpenes DB4 memberikan lebih daripada 50 sebatian dengan skor padanan lebih tinggi daripada 0.90. Spektrum 13C NMR CG_F3 mendedahkan campuran beberapa derivatif triterpena (dengan MW pada 424 untuk semua yang dicadangkan oleh GC-MS) termasuk satu major dan dua derivatif kecil. Selepas pengesahan data 13C NMR dalam literatur, kompaun utama dikenal pasti sebagai sikloartenon71,72 (17, kedudukan 1, skor 0.90, penapis MW pada 424 Da, Rajah SI{{26 }} dan SI-36) dan dua yang kecil sebagai lupenone73,74 (18, pangkat 4, skor 0.87) dan -amyrenone75 (19, pangkat 31, skor {{6{{9 {{1{112}}1}}}}}}.83, Angka SI{{40}} dan SI-36). Begitu juga, dalam pecahan CG_F8, kami menemui campuran alkohol yang sepadan seperti cycloartenol76 (21, kedudukan 7, skor 0.90, Angka SI-39 dan SI{{50}}) sebagai NP utama dan lupeol77 (22) dan -amyrin78 (23) sebagai yang kecil (pangkat 1, skor 0.97 dan pangkat 34, skor {{19{ {204}}}}.83, penapis MW pada 426 Da; Angka SI-41 dan SI-42). Isomer 23, -amyrin (24), juga dikenal pasti terutamanya berdasarkan data 13C NMR (perbandingan dengan data literatur oleh data Seo et al.78 dan GC-MS (MW 426). Kesemua derivatif triterpena keton dan alkohol ini telah pun dikenali dalam propolis.37,38,42,54,79 Untuk CG_F5, kerana analisis GC-MS menunjukkan sebatian utama pada 13.1 min dengan profil terbitan fenol (Jadual 1), penyahreplikasian 13C NMR dengan alk (en)yl resorcinol_phenol DB5 dengan betul mengenal pasti m-heptadecenylphenol80 (20, kedudukan 1, skor 0.87 (Angka SI- 37 dan SI-38) telah diterangkan dalam propolis Cameroon.37 Dalam pecahan CG_F10, Triterpenes DB4 dengan tepat menyerlahkan dipterocarpol81 (25, kedudukan 1, skor 0.93, MW 442, Angka SI-43 dan SI-44) yang diterangkan sebelum ini dalam propolis dari Thailand82 dan Alk(en )yl resorcinol_phenol DB5 mencadangkan 6-asid heptadecenylsalicylic (26, kedudukan 1, skor 0.92, MW 374, Angka SI-43 dan SI-45). Mengenai kedua-dua NP ini , MW mereka tidak sepadan dengan yang ditentukan oleh GC-MS. Ini boleh dijelaskan oleh suhu tinggi yang digunakan dalam kaedah GC-MS: Kompaun 25 mungkin kehilangan molekul air melalui dehidrasi (m/z 424 [M 18]) manakala 26 mungkin kehilangan molekul karbon dioksida melalui penyahkarboksilan (m/ z 330 [M-44]). Untuk pecahan CG_F12 berikut, proses nyahreplikasi menggunakan Triterpenes DB4 mencadangkan banyak sebatian dengan skor tinggi. Menggunakan penapis MW pada 442 Da, dipterokarpa (25) sudah ditemui dalam CG_F10 (kedudukan 20, skor 0.90, Angka SI-46 dan SI-47) dan 24- metilena siklobutana-3 ,26-diol83 (27, kedudukan 3, skor 0.97, penapis MW pada 456 Da, Angka SI-46 dan SI-48) telah dikenal pasti. Dalam pecahan CG_F15, dammarenediol II (28) telah dihipotesiskan dengan betul oleh MixONat dan Triterpenes DB4 menggunakan penapis MW pada 444 Da (kedudukan 1, skor 1, Angka SI-49 dan SI{{156} };GC-MS: m/z 426 [M-18]) dan disahkan oleh data 13C NMR.84 Menggunakan pendekatan yang sama, pecahan terakhir ini ditunjukkan mengandungi dua triterpenoid lain, iaitu asid mangiferin (29, kedudukan 10, skor 0.87, penapis MW pada 454 Da, Angka SI-49 dan SI-51) dan asid embrio (30, kedudukan 1, skor 0.94, penapis MW pada 468 Da, Angka SI{{174 }} dan SI-52) sudah ditemui dalam propolis dari Nigeria40 dan Brazil.85 Asid karboksilik ini tidak dikesan oleh GC-MS kerana kekurangan kemeruapannya (ikatan hidrogen antara molekul disebabkan oleh fungsi asid karboksilik). Begitu juga, dalam CG_F18, dua asid triterpenoid lain telah dikenal pasti, iaitu, asid embolik (34, kedudukan 1, skor 0.87, penapis MW pada 470 Da, Angka SI{{186}} dan SI-56) dan asid mangerolik (35, kedudukan 9, skor 0.80, penapis MW pada 456 Da, Angka SI-55 dan SI-57) turut diterangkan oleh Silva et al. di Brazil.85 Dalam pecahan kedua terakhir CG_F16, 13C NMR dereplikasi dengan Alk(en)yl resorcinol_fenol DB5 dengan tepat mencadangkan lipid resorcinolic, iaitu, heptadecenylresorcinol86 (31, kedudukan 1, skor 0. , Angka SI-53 dan SI-54) dikaitkan dengan dua derivatif resorsinol lain yang dikenal pasti sebagai pentadesenilresorcinol87 (32, MW 318) dan pentadecylresorcinol88 (33, MW 320). Semuanya sebelum ini diasingkan dalam propolis Cameroon37 dan Mexico.89 13Data C NMR 17–35 tersedia dalam maklumat sokongan.


Untuk sampel propolis Congo ini, kebanyakan triterpenoid dan juga lipid resorcinolic mungkin berasal daripada M. indica. 83,89,90
3.4 Penilaian antioksida dan anti-AGE
Penilaian aktiviti antioksidan dan anti-AGE BC1, BC2, dan CG EEPs mendedahkan bahawa hanya BC1 EEP menunjukkan aktiviti antioksidan yang baik (1,172 ± 97 μmol TE/g), dua kali lebih tinggi daripada ekstrak rosemary etanol (E392). Aktiviti ini adalah mengenai jumlah kandungan fenolik yang tinggi (297.0 ± 15.6 mg GAE/g) setanding dengan EEP jenis poplar yang kebanyakannya ditemui di Eropah, Amerika Utara atau China.19 Walau bagaimanapun, analisis kimia bagi BC1 EEP mendedahkan phenanthrenes dan polifenol stilbenoid, termasuk combretastatin B-2 (7), stilbene dihydro. Derivatif tersebut telah pun diterangkan oleh Inui et al. pada 202158 di propolis Senegal menunjukkan aktiviti anti-radang yang ketara, dengan sebatian 4, 6, dan 7 adalah yang paling aktif. Dihydrophenanthrene 6-methoxycoelonin (3) juga telah digambarkan sebagai memaparkan kesan sitotoksik terhadap lima garisan sel kanser manusia (786-0, MCF-7, Hep2, UACC-62 dan NCI/ADR-RES) dengan aktiviti luar biasa terhadap sel UACC-62 (IC50 2.59 μM).91 Fenantrina 6 juga terkenal dengan aktiviti sitotoksik sederhananya terhadap KB, MCF-7 , dan sel K562 dan aktiviti perencatannya yang kuat pada CDK1/siklin B (IC50 0.07 μM).92 Dihydrophenanthrenes daripada spesies Combretum seperti combretastatin juga sebelum ini digambarkan sebagai perencat pertumbuhan sel59: Empat jenis combretastatin boleh dibezakan , iaitu, jenis stilbene (combretastatin A), jenis dihydro stilbene (combretastatin B), jenis phenanthrene (combretastatin C), dan combretastatin jenis makrolakton kitaran (combretastatin D). Antaranya, combretastatin A (A-4, tetapi juga A-1 dan A-2) mempamerkan aktiviti anti-tumor tertinggi.93,94 Oleh itu, nampaknya terbaik untuk menggunakan propolis antioksidan sedemikian mengandungi phenanthrene, dihydrophenanthrene, dan derivatif combretastatin dengan berhati-hati. Ia mengesahkan kepentingan penentuan awal komposisi kimia propolis sebelum digunakan dalam produk makanan dan kesihatan.

Di antara semua ekstrak propolis yang digunakan dalam kajian ini, hanya BC2 EEP mempamerkan aktiviti anti-AGE sederhana (IC50 0.70 mg/ml) berbanding ekstrak etanol S. japonicum, terkenal dengan tingginya. aktiviti anti-AGE19 (rujuk Jadual SI.1). Seperti yang dijangkakan, semua derivatif flavanone yang telah dimurnikan menunjukkan aktiviti yang baik (IC50 0.20–0.26 mM; Jadual SI-1) hampir dengan nilai rujukan (Quercetin IC50 0.20 mM) kecuali untuk 13 (IC50 0.60 mM). Aktiviti anti-AGE yang lebih tinggi sebelum ini dilaporkan untuk EEP Perancis (IC50 0.05 mg/ml) dengan tahap derivatif triterpene yang jauh lebih rendah dan jumlah derivatif pinobanksine yang tinggi.19
Kesimpulannya, dalam kerja ini, GC-MS atau HPLC-DAD-MS pertama kali digunakan untuk mengenal pasti kelas NP yang berbeza dan menentukan MW mereka. Kemudian dereplikasi berasaskan NMR 13C menggunakan perisian MixONat dengan DB tersuai membolehkan kami mencirikan NP utama daripada pecahan dengan jelas. Sebagai tambahan kepada triterpenoid utama, BC1, sampel propolis yang berasal dari pusat Benin, mempamerkan komposisi asal dengan tahap derivatif dihydrophenanthrene, phenanthrene, dan bis benzyl yang tinggi, beberapa daripadanya dikenal pasti buat kali pertama dalam propolis. Sesetengah polifenol antioksidan ini mungkin sitotoksik dan mengingatkan kita tentang keperluan untuk analisis sistematik propolis sebelum digunakan dalam makanan dan produk kesihatan, terutamanya untuk propolis yang kurang dikenali dari kawasan tropika. Antara ekstrak lain kepunyaan propolis jenis Macaranga, BC2, yang dikumpul di kawasan yang sama, mengandungi prenyl dan geranyl flavanones dengan aktiviti anti-AGE. Propolis dari Congo mengandungi NP yang berkemungkinan besar dikaitkan dengan sumber botani M. indica: triterpenoid jenis cyclobutane dan lipid resorcinolic. Siasatan lanjut akan dilakukan untuk mengaitkan komposisi fitokimia sampel propolis Benin dan Congo dengan flora tempatan dan untuk menilai sifat anti-kulat atau anti-bakteria mereka.

PENGAKUAN
Penulis mengucapkan terima kasih kepada Dr. Ingrid Freuze dari "Plateau Astral" di Fakulti Sains di Angers untuk analisis LC-MS.
PENGAKUAN SOKONGAN KEWANGAN
Penulis mengucapkan terima kasih kepada Yayasan Sains Antarabangsa (IFS) (Grant I-3-E-5720-2) dan Jawatankuasa Kerjasama Saintifik dan Teknologi (COMSTECH) atas sokongan kewangan mereka.
PENYATA KESEDIAAN DATA
Semua data bertanda SI disertakan dalam bahagian maklumat tambahan.

RUJUKAN
1. Simone-Finstrom M, Borba RS, Wilson M, Spivak M. Propolis mengatasi beberapa ancaman kepada kesihatan lebah madu. Serangga. 2017;8(2):46.
2. Harfouch RM, Mohammad R, Suliman H. Aktiviti antibakteria ekstrak propolis Syria terhadap beberapa jenis bakteria secara in vitro. Dunia J Pharm Sci. 2017;6(2):42-46.
3. Gavanji S, Larki B. Kesan perbandingan propolis lebah madu dan beberapa ekstrak herba pada Candida albicans. Chin J Integr Med. 2017; 23(3):201-207.
4. Wagh VD. Propolis: produk lebah ajaib dan potensi farmakologinya. Adv Pharm Sci. 2013;2013:308249.
5. Ahangari Z, Naseri M, Vatandoost F. Propolis: komposisi kimia dan aplikasinya dalam endodontik. Iran Endod J. 2018;13(3):285-292.
6. Anjum SI, Ullah A, Khan KA, et al. Komposisi dan sifat fungsi propolis (gam lebah): ulasan. Saudi J Biol Sci. 2019;26(7):1695- 1703.
7. Drescher N, Klein AM, Schmitt T, Leonhardt SD. Petunjuk tentang gam lebah: pandangan baharu tentang sumber dan faktor yang mendorong pengambilan resin dalam lebah madu (Apis mellifera). PLoS SATU. 2019;14(2):e0210594.
8. Toreti VC, Sato HH, Pastore GM, Park YK. Kemajuan Terkini Propolis untuk Komposisi Biologi dan Kimia serta asal botaninya. Med Altern Pelengkap Berasaskan Evid. 2013;2013:e697390.
9. Oruç HH, Sorucu A, Ünal HH, Aydin L. Kesan musim dan ketinggian pada tahap sebatian fenolik tertentu yang aktif biologi dan penyeragaman separa propolis. Ankara Üniv Vet Fak Derg. 2017;64(1):13- 20.
10. Cardinault N, Cayeux MO, du Sert PP. La propolis: asal, komposisi dan propriétés. Phytotherapie. 2012;10(5):298-304.
11. Boisard S, Le Ray AM, Landreau A, et al. Metabolit antikulat dan antibakteria daripada Propolis jenis poplar Perancis. Med Altern Pelengkap Berasaskan Evid. 2015;2015:e319240.
12. Christov R, Trusheva B, Popova M, Bankova V, Bertrand M. Komposisi kimia propolis dari Kanada, aktiviti antiradikalnya dan asal tumbuhan. Nat Prod Res. 2006;20(6):531-536.
13. Trusheva B, Popova M, Koendhori EB, Tsvetkova I, Naydenski C, Bankova V. Propolis Indonesia: komposisi kimia, aktiviti biologi, dan asal botani. Nat Prod Res. 2011;25(6):606-613.
14. Popova M, Trusheva B, Cutajar S, et al. Pengenalpastian asal tumbuhan bagi biomarker botani propolis jenis Mediterranean. Nat Prod Commun. 2012;7(5):569-570.
15. Freires IA, de Alencar SM, Rosalen PL. Perspektif farmakologi tentang penggunaan Propolis merah Brazil dan sebatian terpencilnya terhadap penyakit manusia. Eur J Med Chem. 2016;110:267-279.
16. Soboˇcanec S, ˇ Sverko V, Balog T, et al. Sifat oksidan/antioksida Propolis asli Croatia. J Agric Food Chem. 2006;54(21):8018- 8026.
17. Hochheim S, Guedes A, Faccin-Galhardi L, et al. Penentuan profil fenolik oleh HPLC-ESI-MS/MS, aktiviti antioksidan, sitotoksisiti in vitro, dan aktiviti anti-herpetik propolis daripada lebah asli Brazil Melipona quadrifasciata. Ladang Rev Bras. 2019;29(3):339- 350.
18. Alaribe CS, Esposito T, Sansone F, et al. Propolis Nigeria: komposisi kimia, aktiviti antioksidan, dan perencatan -amilase dan -glucosidase. Nat Prod Res. 2019;0(18):1-5.
19. Boisard S, Le Ray AM, Gatto J, et al. Komposisi kimia, aktiviti antioksidan dan anti-AGEs Propolis jenis poplar Perancis. J Agric Food Chem. 2014;62(6):1344-1351.
20. Francin M, Freires IA, Lazarini JG, et al. Penggunaan propolis Brazil untuk penemuan dan pembangunan ubat anti-radang novel. Eur J Med Chem. 2018;153:49-55.
21. Hassiba R, Wided K, Mesbah L, et al. Propolis Algeria mempotensikan kesan antikanser pengantara doxorubicin terhadap saluran sel kanser PANC{2}} pankreas manusia melalui penahanan kitaran sel, induksi apoptosis dan perencatan P-glikoprotein. Ejen Antikanser Med Chem. 2018; 18(3):375-387.
22. Xuan H, Li Z, Yan H, et al. Aktiviti antitumor Propolis Cina dalam sel MCF-7 dan MDA-MB-231 kanser payudara manusia. Med Altern Pelengkap Berasaskan Evid. 2014;2014:e280120.
23. Silva FRG, Matias TMS, Souza LIO, et al. Pemeriksaan fitokimia dan aktiviti antibakteria, antikulat, antioksidan dan antitumor in vitro propolis merah Alagoas. Braz J Biol. 2018;79(3):452-459.
24. Chen YW, Ye SR, Ting C, Yu YH. Aktiviti antibakteria propolis daripada propolis hijau Taiwan. J Makanan Ubat Dubur. 2018;26(2):761- 768.
25. Afrouzan H, Tahghighi A, Zakeri S, Es-haghi A. Komposisi kimia dan aktiviti antimikrob Propolis Iran. Iran Biomed J. 2018; 22(1):50-65.
26. Thamnopoulos IAI, Michailidis GF, Fletouris DJ, Badeka A, Kontominas MG, Angelidis AS. Aktiviti perencatan propolis terhadap listeria monocytogenes dalam susu yang disimpan di bawah penyejukan. Mikrobiol Makanan. 2018;73:168-176.
27. Yildirim A, Duran GG, Duran N, et al. Aktiviti antivirus Hatay Propolis terhadap replikasi virus herpes simplex jenis 1 dan jenis 2. Med Sci Monit. 2016;22:422-430.
28. Silva RPD, Machado BAS, de Barreto G, et al. Antioksidan, antimikrobial, antiparasit, dan sifat sitotoksik pelbagai ekstrak propolis Brazil. PLoS SATU. 2017;12(3):e0172585
29. Takeda K, Nagamatsu K, Okumura K. Derivatif propolis larut air menambah aktiviti sitotoksik sel pembunuh semulajadi. J Ethnopharmacol. 2018;218:51-58.
30. Hegazi AG, Abd El Hady FK, Abd Allah FAM. Komposisi kimia dan aktiviti antimikrob propolis Eropah. Z Naturforsch. 2000; 55(1-2):70-75.
31. Bankova V, Popova M, Bogdanov S, Sabatini AG. Komposisi kimia propolis Eropah: keputusan yang dijangka dan tidak dijangka. Z Naturforsch. 2002;57(5-6):530-533.
32. Isidorov VA, Buczek K, Zambrowski G, Miastkowski K, Swiecicka I. Kajian in vitro mengenai aktiviti antimikrob propolis Eropah terhadap larva Paenibacillus. Apidologi. 2017;48(3):411-422.
33. AL-Ani I, Zimmermann S, Reichling J, Wink M. Aktiviti antimikrob Propolis Eropah yang dikumpulkan dari pelbagai asal geografi sahaja dan digabungkan dengan antibiotik. Ubat-ubatan. 2018;5(1):2.
34. Bueno-Silva B, Marsola A, Ikegaki M, Alencar SM, Rosalen PL. Kesan musim pada propolis merah Brazil dan sumber botaninya: komposisi kimia dan aktiviti antibakteria. Nat Prod Res. 2017; 31(11):1318-1324.
35. da Regueira-Neto M, Tintino SR, Rolon M, et al. Aktiviti antitrypanosomal, antileishmanial dan sitotoksik propolis merah Brazil dan resin tumbuhan Dalbergia ecastaphyllum (L) Taub. Toksik Kimia Makanan. 2018;119:215-221.
36. Rufatto LC, Luchtenberg P, Garcia C, et al. Propolis merah Brazil: komposisi kimia dan aktiviti antibakteria ditentukan menggunakan pecahan berpandukan bio. Mikrobiol Res. 2018;214:74-82.
37. Kardar MN, Zhang T, Coxon GD, Watson DG, Fearnley J, Seidel V. Pencirian triterpena dan lipid fenolik baharu dalam propolis Cameroon. Fitokimia. 2014;106:156-163.
38. Sakava P, Talla E, Chelea M, et al. Pentacyclic triterpenes dan ekstrak mentah dengan aktiviti antimikrob dari sampel propolis coklat Cameroon. J Appl Pharm Sci. 2014;4(7):1-9.
39. Talla E, Tamfu AN, Gade IS, et al. Mono-eter baharu gliserol dan triterpena dengan aktiviti penghapusan radikal DPPH daripada propolis Cameroon. Nat Prod Res. 2017;31(12):1379-1389.
40. Omar R, Igoli JO, Zhang T, et al. Pencirian kimia sampel Propolis Nigeria dan aktivitinya terhadap Trypanosoma brucei. Sci Rep. 2017;7(1):923.
41. Tamfu AN, Sawalda M, Fotsing MT, et al. Isoflavon baharu dan konstituen lain daripada propolis Cameroon dan penilaian potensi anti-radang, antikulat dan antioksidannya. Saudi J Biol Sci. 2020;27(6):1659-1666.
42. Papachroni D, Graikou K, Kosalec I, Damianakos H, Ingram V, Chinou I. Analisis fitokimia dan penilaian biologi sampel Propolis Afrika terpilih dari Cameroon dan Congo. Nat Prod Commun. 2015;10(1):67-70.
43. Bruguière A, Derbré S, Dietsch J, et al. MixONat, perisian untuk Dereplikasi campuran berdasarkan Spektroskopi 13C NMR. Kimia Dubur. 2020;92(13):8793-8801.
44. Bruguière A, Derbré S, Bréard D, Tomi F, Nuzillard JM, Richomme P. 13C NMR Dereplikasi menggunakan perisian MixONat: panduan praktikal untuk menguraikan campuran produk semula jadi. Planta Med. 2021;87(12–13): 1061-1068.
45. Silva-Castro LF, Derbré S, Le Ray AM, Richomme P, García-Sosa K, Peña-Rodriguez LM. Menggunakan dereplikasi 13C-NMR untuk membantu dalam mengenal pasti xanthone yang terdapat dalam ekstrak kulit batang Calophyllum brasiliense. Phytochem Dubur. 2021;32(6):1102-1109.
46. Nuzillard JM. Pangkalan data produk semula jadi tertumpu taksonomi untuk Karbon-13 Dereplikasi berasaskan NMR. Analytica. 2021;2(3):50-56.
47. Pencari Sains.
48. TERATAI: PRODUK semulajadi berlaku pangkalan data.
49. Lianza M, Leroy R, Machado Rodrigues C, et al. Tiga tonggak Dereplikasi produk semulajadi. Alkaloid daripada mentol Urceolina peruviana (C. Presl) JF Macbr. Sebagai kes ujian awal. Molekul. 2021;26(3):637.
50. Nuzillard J, Leroy R, Kuhn S. Ramalan karbon-13 data NMR Produk Asli (PNMRNP).
51. Boisard S, Shahali Y, Aumond MC, et al. Aktiviti anti-AGE propolis jenis poplar: mekanisme tindakan sebatian fenolik utama. Int J Food Sci Technol. 2020;55(2):453-460.
52. Séro L, Sanguinet L, Blanchard P, et al. Menala 96-ujian berasaskan pendarfluor plat mikrotiter telaga untuk mengenal pasti perencat AGE dalam ekstrak tumbuhan mentah. Molekul. 2013;18(11):14320-14339.
53. Derbré S, Gatto J, Pelleray A, Coulon L, Séraphin D, Rihomme P. Mengautomasikan 96-ujian plat mikrotiter telaga untuk mengenal pasti perencat atau inducer AGEs: aplikasi untuk penyaringan perpustakaan sebatian semula jadi yang kecil. Kimia Bioanal Dubur. 2010;398(4):1747-1758.
54. Boisard S, Huynh THT, Escalante-Erosa F, Hernández-Chavez LI, Peña-Rodríguez LM, Richomme P. Komposisi kimia luar biasa propolis Mexico yang dikumpul di Quintana Roo, Mexico. J Apic Res. 2015;54(4):350-357.
55. Zhang T, Omar R, Siheri W, et al. Analisis kromatografi dengan pengesan berbeza dalam pencirian kimia dan dereplikasi propolis Afrika. Talanta. 2014;120:181-190.
56. Katerere DR, Grey AI, Nash RJ, Waigh RD. Penyiasatan fitokimia dan antimikrob bagi stilbenoid dan flavonoid yang diasingkan daripada tiga spesies Combretaceae. Fitoterapia. 2012;83(5):932-940.
57. Leong YW, Kang CC, Harrison LJ, Powell AD. Phenanthrenes, dihydrophenanthrenes, dan bibenzyls daripada orkid Bulbophyllum vaginatum. Fitokimia. 1997;44(1):157-165.
58. Inui S, Hosoya T, Yoshizumi K, Sato H, Kumazawa S. Sifat fitokimia dan anti-radang propolis Senegal dan sebatian terpencil. Fitoterapia. 2021;151:104861.
59. Pettit GR, Singh SB, Niven ML, Schmidt JM. Dihydrophenanthrene dan phenanthrene yang menghalang pertumbuhan sel dari pokok Afrika Combretum caffrum. Boleh J Chem. 1988;66(3):406-413.
60. Lu D, Liu J, Li P. Dihydrophenanthrenes daripada batang dan daun Dioscorea nipponica Makino. Nat Prod Res. 2010;24(13):1253-1257.
61. Letcher RM, Nhamo LRM. Juzuk kimia Combretaceae. Bahagian I. menggantikan phenanthrenes dan 9,10-dihydrophenanthrenes daripada kayu inti Combretum apiculatum. J Chem Soc C. 1971;18):3070-3076:3070.
62. Letcher RM, Nhamo LRM. Juzuk kimia Combretaceae. III. Fenanthrenes digantikan, 9,10-dihydrophenanthrenes, dan bibenzyls daripada kayu inti Combretum silicids. J Chem Soc, Perkin Trans 1 (1972–1999). 1972;23:2941-2946.
63. Chen Y, Cai S, Deng L, et al. Pengasingan dan penulenan 9,10-dihydrophenanthrenes dan bibenzyls daripada Pholidota chinensis oleh kromatografi arus balas berkelajuan tinggi. J Sep Sci. 2015;38(3): 453-459.
64. Ghosal S, Kumar Y, Singh S, Ahad K. Biflorin, chromone-C-glucoside daripada Pancratium biflorum. Fitokimia. 1983;22(11):2591-2593.
65. Zhang Y, Chen Y. Isobiflorin, chromone C-glucoside daripada cengkih (Eugenia caryophyllata). Fitokimia. 1997;45(2):401-403.
66. Omar RMK, Igoli J, Grey AI, et al. Pencirian kimia propolis merah Nigeria dan aktiviti biologinya terhadap Trypanosoma Brucei. Phytochem Dubur. 2016;27(2):107-115.
67. Inui S, Shimamura Y, Masuda S, Shirafuji K, Moli RT, Kumazawa S. Prenylflavonoid baharu yang diasingkan daripada Propolis yang dikumpulkan di Kepulauan Solomon. Biosci Biotechnol Biochem. 2012;76(5):1038-1040.
68. Seo EK, Silva GL, Chai HB, et al. Flavanon terprenilasi sitotoksik daripada pemancing Monotes. Fitokimia. 1997;45(3):509-515.
69. Huang YL, Yeh PY, Shen CC, Chen CC. Flavonoid antioksidan daripada rizom Helminthostachys zeylanica. Fitokimia. 2003; 64(7):1277-1283.
70. Meragelman KM, McKee TC, Boyd MR. Flavonoid Berprenilasi Anti-HIV daripada Monotes africanus. J Nat Prod. 2001;64(4):546-548.
71. Davies NW, Miller JM, Naidu R, Sotheeswaran S. Triterpenoids dalam eksudat tunas spesies FijianGardenia. Fitokimia. 1992;31(1):159- 162.
72. Zambrano EE, Casas AG, Di Venosa GM, Uriburu ML, Duran FJ, Palermo JA. Penilaian sintesis dan sitotoksisiti derivatif cincin A bagi sikloartanone. Phytochem Lett. 2017;21:200-205.
73. Prashant A, Krupadanam GLD. Dehydro-6-hydroxyrotenoid dan lupenone daripada Tephrosia villosa. Fitokimia. 1993;32(2):484-486.
74. Hisham A, Kumar GJ, Fujimoto Y, Hara N. Salacianone dan salacianol, dua triterpene daripada Salacia beddomei. Fitokimia. 1995;40(4): 1227-1231.
75. de Carvalho MG, Rincon Velandia J, de Oliveira LF, Bezerra FB. Triterpenos isolados de Eschweilera longipes miers (Lecythidaceae). Quím Nova. 1998;21(6):740-743.
76. Nes WD, Koike K, Jia Z, et al. 9 ,19-Analisis siklosterol oleh 1H dan 13C NMR, pemerhatian kristalografi dan pengiraan mekanik molekul. J Am Chem Soc. 1998;120(24):5970-5980.
77. Sholichin M, Yamasaki K, Kasai R, Tanaka O. ^<13>C resonans magnetik nuklear triterpena jenis Lupane, Lupeol, Betulin, dan asid Betulinik. Chem Pharm Bull. 1980;28(3):1006-1008.
78. Seo S, Tomita Y, Tori K. Karbon-13 spektrum nmr urs-12-enes dan penggunaan pada penugasan struktur komponen kultur tisu Isodon japonicus hara. Tetrahedron Lett. 1975;16(1):7-10.
79. Nguyen HX, Nguyen MTT, Nguyen NT, Awale S. Konstituen kimia Propolis dari Vietnam Trigona minor dan aktiviti Antiausterity mereka terhadap PANC-1 barisan sel kanser pankreas manusia. J Nat Prod. 2017;80(8):2345-2352.
80. de Correia S, David JM, David JP, Chai HB, Pezzuto JM, Cordell GA. Alkil fenol dan terbitan daripada Tapirira obtusa. Fitokimia. 2001;56(7):781-784.
81. Asakawa J, Kasai R, Yamasaki K, Tanaka O. 13C NMR kajian sapogenin ginseng dan triterpene jenis dammarane yang berkaitan. Tetrahedron. 1977;33(15):1935-1939.
82. Sanpa S, Popova M, Bankova V, Tunkasiri T, Eitssayeam S, Chantawannakul P. Sebatian antibakteria daripada Propolis Tetragonula laeviceps dan Tetrigona melanoleuca (hymenoptera: Apidae) dari Thailand. PLoS SATU. 2015;10(5):e0126886.
83. Anjaneyulu V, Satyanarayana P, Viswanadham KN, Jyothi VG, Rao KN, Radhika P. Triterpenoids daripada Mangifera indica (bahagian III). Fitokimia. 1999;50(7):1229-1236.
84. Herrera-Lopez MG, Rubio-Hernández EI, Leyte-Lugo MA, et al. Asal botani triterpenoid daripada propolis Yucatecan. Phytochem Lett. 2019;29:25-29.
85. da Silva MDSS, Cito AMDGL, Chaves MH, Lopes JAD. Triterpenoides tipo cicloartano de propolis de Teresina - PI. Quím Nova. 2005;28(5): 801-804.
86. Jalil J, Jantan I, Shaari K, Abdul Rafi IA. Pengasingan berpandukan bioassay bagi antagonis faktor pengaktif platelet yang kuat Alkenylresorcinol daripada Ardisia elliptica. Pharm Biol. 2004;42(6):457-461.
87. Wu LQ, Yang CG, Yang LM, Yang LJ. Tindak balas Wittig berbantukan ultrabunyi dan sintesis 5-alkil- dan 5-alkenil-resorsinol. J Chem Res. 2009;2009(3):183-185. d
88. Mizuno CS, Rimando AM, Duke SO. Aktiviti fitotoksik Quinones dan derivatif lipid Resorcinolic. J Agric Food Chem. 2010;58(7): 4353-4355.
89. Herrera-Lopez MG, Rubio-Hernández EI, Richomme P, Schinkovitz A, Calvo-Irabién LM, Rodríguez LMP. Lipid resorcinolic daripada Yucatecan Propolis. J Braz Chem Soc. 2020;31:186-192.
90. Nguyen HX, Do TNV, Le TH, et al. Juzuk kimia Mangifera indica dan aktiviti Antiausteritinya terhadap barisan sel kanser pankreas manusia PANC-1. J Nat Prod. 2016;79(8):2053-2059.
91. Bisoli E, Freire TV, Yoshida NC, et al. Phenanthrene sitotoksik, Dihydrophenanthrene, derivatif Dihydrostilbene, dan sebatian aromatik lain daripada Combretum laxum. Molekul. 2020;25(14):3154.
92. Apel C, Dumontet V, Lozach O, Meijer L, Guéritte F, Litaudon M. Phenanthrene derivatif daripada Appendicula reflexa sebagai perencat CDK1/cyclin B baharu. Phytochem Lett. 2012;5(4):814-818.
93. Karatoprak GŞ, Küpeli Akkol E, Genç Y, Bardakcı H, Yücel Ç, SobarzoSánchez E. Combretastatins: gambaran keseluruhan struktur, kemungkinan mekanisme tindakan dan aplikasi yang berpotensi. Molekul. 2020; 25(11):2560.
94. Mazumder K, Aktar A, Roy P, et al. Kajian semula tentang cerapan mekanistik Phytocompounds bioaktif antikanser terbitan tumbuhan dan hubungan struktur-aktiviti mereka. Molekul. 2022;27(9):3036.
MAKLUMAT SOKONGAN
Maklumat sokongan tambahan boleh didapati dalam talian dalam bahagian Maklumat Sokongan di penghujung artikel ini.
【Untuk maklumat lanjut: david.deng@wecistanche.com / WhatApp:86 13632399501】






