Bioassay Untuk Memantau Kesan Anti-penuaan Rawatan Darah Kord
Feb 27, 2022
Kenalan:jerry.he@wecistanche.com
Sang-Hun Bae1*, Ala Jo1,2*, Jae Hyun Park1, Chul-Woo Lim1, Yuri Choi1, Juhyun Oh2, Ji-Min Park1, TaeHo Kong1, Ralph Weissleder2,3, Hakho Lee2, Jisook Moon1
1. Jabatan Bioteknologi, Kolej Sains Hayat, Universiti CHA, Gyeonggi-do 13488, Republik Korea
2. Pusat Biologi Sistem, Hospital Besar Massachusetts, Sekolah Perubatan Harvard, Boston, MA 02114, Amerika Syarikat
3. Jabatan Biologi Sistem, Sekolah Perubatan Harvard, Boston, MA 02115, Amerika Syarikat *Pengarang ini memberi sumbangan yang sama.
Pengarang yang sepadan: Hakho Lee, PhD. Pusat Biologi Sistem, Hospital Besar Massachusetts, 185 Cambridge St, CPZN 5206, Boston, MA 02114, Amerika Syarikat. 617-726-8226 hlee@mgh.harvard.edu Jisook Moon, PhD. Jabatan Bioteknologi, Kolej Sains Hayat, Universiti CHA, Pangyo-ro 335, Bundang-gu, Seongnam-si, Gyeonggi-do 13488, Republik Korea. 82-31-881-7210 jmoon@cha.ac.kr
© Penerbit Antarabangsa Ivyspring. Ini ialah artikel akses terbuka yang diedarkan di bawah syarat lesen Creative Commons Attribution (CC BY-NC) (https://creativecommons.org/licenses/by-nc/4.0/). Lihat http://ivyspring.com/terms untuk terma dan syarat penuh.
Diterima: 2018.10.04; Diterima: 2018. 11. 18; Diterbitkan: 2019.01.01

Cistanche mempunyai kesan anti-penuaan
Abstrak
Latar belakang: Merawat haiwan tua dengan plasma peringkat perkembangan awal (cth, plasma tali pusat) menunjukkan potensi yang mengagumkan untuk memperlahankan degradasi fungsi neuron dan kognitif yang berkaitan dengan usia. Menerjemahkan penemuan tersebut kepada realiti klinikal, bagaimanapun, memerlukan cara yang berkesan untuk menilai keberkesanan rawatan; kaedah yang ideal hendaklah invasif minimum, boleh diterima untuk ujian bersiri, kos efektif dan kuantitatif.
Kaedah: Kami membangunkan pendekatan biosensor baharu untuk memantauanti penuaanterapi. Kami memajukan dua komponen penderia utama: i) metabolit bawaan darah dikenal pasti sebagai penanda penuaan pengganti; dan ii) sistem ujian padat dan kos efektif telah dibangunkan untuk aplikasi di tapak. Kami merawat tikus tua sama ada dengan plasma tali pusat manusia atau garam; profil metabolit tidak berat sebelah pada plasma tetikus mendedahkan asid arakidonik (AA) sebagai penunjuk kuat yang dikaitkan dengananti penuaankesan. Kami seterusnya melaksanakan sensor magneto-elektrokimia (cMES) yang kompetitif yang dioptimumkan untuk pengesanan AA terus daripada plasma. Platform yang dibangunkan boleh mengesan AA terus daripada jumlah kecil plasma (0.5 µL) dalam masa 1.5 jam.
Keputusan: ujian cMES mengesahkan korelasi yang kuat antara tahap AA dankesan anti-penuaan: Tahap AA, sementara menurun dengan penuaan, meningkat pada tikus berumur yang dirawat plasma yang juga menunjukkan peningkatan prestasi pembelajaran dan ingatan.
Kesimpulan: Platform cMES akan memperkasakan kedua-dua pra-dan klinikalanti penuaanpenyelidikan dengan membolehkan pengawasan rawatan membujur invasif minimum; kapasiti ini akan mempercepatkan pembangunananti penuaanterapi, meningkatkan kualiti kehidupan individu.
Kata kunci: Anti-penuaan, asid arakidonik, pemprofilan metabolit, sensor magneto-elektrokimia, Biosensor
pengenalan
Penuaan semakin diiktiraf sebagai faktor risiko klinikal untuk degenerasi kognitif (cth, neurodegeneration, demensia) dan penyakit kronik lain (cth, kanser, penyakit kardiovaskular, degenerasi otot) [1]. Dengan memperluaskan jangka hayat manusia dan populasi warga tua yang semakin meningkat, usaha penting sedang dijalankan untuk menjelaskan mekanisme penuaan [1-3] dan untuk mencari strategi terapeutik untuk melambatkan atau membalikkan proses penuaan [4]. Sesungguhnya, hasil yang menjanjikan daripada kajian haiwan telah dilaporkan; tikus dewasa yang menerima transfusi plasma daripada tikus muda memperoleh semula fungsi kognitif, keplastikan sinaptik, dan aktiviti neuron [5]. Perkembangan pesat dalamanti penuaanrawatan dan terjemahannya ke dalam ujian manusia dijangka [6]. Metrik semasa untuk memantau kesan rawatan, bagaimanapun, mempunyai kepraktisan yang terhad, kerana kaedah selalunya sukar digunakan dengan manusia (cth, pengimejan otak invasif, pemerhatian tingkah laku terkawal) dan subjektif (cth, soal selidik tentang pengalaman pesakit). Satu keperluan utama dalam memajukananti penuaanOleh itu, terapi terletak pada membangunkan ujian kuantitatif, invasif minimum untuk pemantauan rawatan.
Kami beralasan bahawa metabolit akan menjadi sumber yang kuat untukanti penuaanbiomarker. Metabolit adalah fenotip penting dalam organisma dan sedang dikaji sebagai biomarker diagnostik untuk penyakit lain [7]. Khususnya, penuaan biasanya dikaitkan dengan perubahan metabolik atau disfungsi, yang menjejaskan keseluruhan profil metabolit dalam organisma. Oleh itu, boleh difikirkan bahawa mengesan komposisi dan/atau tahap metabolit akan memberitahu keberkesanananti penuaanrawatan. Tambahan pula, ujian metabolit, terutamanya dalam bentuk ujian darah, boleh bersifat kuantitatif dan invasif minimum; merit ini akan memudahkan memaklumkan rejimen rawatan atau kumpulan pesakit yang berbeza, dan memantau dinamika (anti-) penuaan melalui pensampelan bersiri.
Kami di sini menerangkan strategi biosensor baharu untuk pemantauananti penuaanrawatan. Dua elemen utama telah dimajukan: i) metabolit bawaan darah dikenal pasti sebagai penanda penuaan pengganti; dan ii) sistem ujian yang cepat dan kos efektif telah dibangunkan untuk aplikasi dalam tetapan klinikal rutin. Khususnya, kami merawat kohort tikus tua (kira-kira 2 tahun) dengan plasma daripada darah tali pusat manusia. Analisis metabolomik yang komprehensif pada darah tikus mendedahkan bahawa asid arakidonik (AA), yang tahapnya menurun dengan ketara dengan penuaan, meningkat secara terbalik dalam kumpulan yang dirawat. Pemerhatian ini membawa kami untuk mencipta sensor magneto-elektrokimia untuk sasaran molekul kecil: kami mengoptimumkan tindak balas elektrokimia yang kompetitif di mana AA ditangkap pada manik magnet dan tertumpu untuk kepekaan yang lebih tinggi. Platform yang dibangunkan boleh mengesan AA terus daripada jumlah kecil plasma (0.5 µL) dalam masa 1.5 jam. Dengan menggunakan platform ini, kami boleh terus mewujudkan korelasi positif antara tahap AA darah dan prestasi haiwan yang lebih baik dalam tugas motor.
Keputusan
Merawat tikus dewasa dengan plasma darah kord Rajah 1a menunjukkan skema eksperimen keseluruhan.
Sebagai ejen, kami menggunakan plasma yang diperoleh daripada sampel darah tali pusat manusia. Kajian terdahulu menunjukkan bahawa tikus tua yang disuntik dengan plasma tetikus muda memulihkan fungsi ingatan spatial, dan pentadbiran sistemik plasma darah tali pusat manusia meningkatkan kognisi yang bergantung kepada hippocampal pada tikus tua [5, 8]. Menyuntik plasma, yang tidak mempunyai komponen selular, meminimumkan risiko penolakan imun yang datang daripada ketidakpadanan spesies. Tikus yang berumur (umur mula, 18 bulan) telah rawak dan menerima sama ada plasma (kumpulan rawatan) atau penimbal garam (kumpulan palsu) melalui suntikan sia-sia ekor (130 µL; lihat Rajah S1 untuk butiran). Sebagai kawalan positif, tikus muda (3 bulan) digunakan. Plasma yang diperoleh daripada darah tali pusat tidak dikumpulkan dan setiap tetikus telah berulang kali diselitkan dengan plasma daripada penderma yang sama (Rajah S1). Selepas 4-rawatan minggu, tikus tertakluk kepada ujian tingkah laku (iaitu, rotarod) dan darah diambil untuk analisis.

Rajah 1. Reka bentuk eksperimen. Plasma darah tali pusat manusia telah diberikan kepada kumpulan muda (3-bulan), tua (20- dan 23-bulan), dan kumpulan lama yang dirawat plasma (20- dan 23-bulan). Ketiga-tiga kumpulan telah menjalani 2-ujian percubaan Rotarod untuk mengukur koordinasi dan pembelajaran motor. Profil metabolit yang tidak disasarkan telah dilakukan pada darah dari tiga kumpulan, dan yang paling banyakanti penuaan-laluan yang berkaitan ditentukan melalui pendekatan bioinformatik. Biosensor telah dibangunkan untuk mengesan metabolit terpenting bagi laluan tersebut.

Rajah 2. Penentuan biomarker metabolit yang dikaitkan dengan rawatan plasma darah tali pusat manusia. (A) Profil global gangguan metabolit. Baris sepadan dengan ciri (gabungan unik nilai m/z dan masa pengekalan) daripada LC/MS dan lajur kepada sampel. Baris dikelompokkan secara hierarki. (B) Plot skor PCA untuk pengurangan dimensi. Sampel diplot terhadap komponen utama (PC) 1 dan 2. Nilai dalam kurungan legenda paksi ialah perkadaran varians yang dijelaskan oleh komponen tersebut. PC1 berkemungkinan besar menerangkan kesan anti-penuaan, memandangkan kumpulan yang dirawat plasma adalah lebih dekat dengan kumpulan muda daripada kumpulan palsu. (C) Analisis pengayaan laluan. Metabolit dikenal pasti dengan memadankan nilai m/z yang diukur dengan maklumat jisim molekul. Setiap bulatan mewakili laluan tertentu yang ditemui. Untuk laluan tertentu, lokasi x atau saiz bulatan sepadan dengan kepusatan relatif-antara (ukuran kesan laluan) metabolit, dan lokasi atau warna y (nilai p yang lebih rendah untuk merah dan lebih tinggi untuk biru) setakat metabolit manakah yang diwakili secara berlebihan. Laluan dominan mempunyai nilai x dan y yang lebih tinggi. Sehubungan itu, metabolisme asid arakidonik (AA) dikenal pasti sebagai laluan yang paling berkemungkinan untuk menjelaskankesan anti-penuaanplasma darah tali pusat.

Analisis metabolik pada sampel darah tikus
Kami mula-mula melakukan profil metabolit molekul kecil yang tidak berat sebelah dalam plasma tetikus. Sampel darah daripada ketiga-tiga kumpulan tetikus telah tertakluk kepada analisis kromatografi cecair dan spektrometri jisim (LC/MS). Kami memproses data m/z oleh MAIT (kit alat pengenalan automatik metabolit) dan mengenal pasti ciri-ciri penting secara statistik melalui ANOVA (8572 kombinasi unik m/z dan masa pengekalan) (Rajah 2a). Analisis pengelompokan hierarki (HCA) metabolit mendedahkan dua corak utama: i) profil metabolit adalah berbeza secara jelas antara tikus tua (tidak dirawat) dan muda; dan ii) profil tikus berumur yang dirawat plasma adalah lebih dekat dengan tikus muda.
Analisis komponen utama (PCA) mendedahkan struktur yang wujud bagi data metabolomik (Rajah 2b). Kira-kira 50 peratus daripada jumlah variasi boleh dijelaskan oleh komponen utama pertama (PC1) dan komponen utama kedua (PC2). Ketiga-tiga kohort (iaitu, kumpulan muda, dirawat plasma, dan kumpulan palsu) diselesaikan pada kedudukan diskret, menunjukkan bahawa ciri-ciri yang berkaitan secara biologi untuk membezakan kelas kumpulan telah dikenal pasti. Menariknya, kumpulan tua yang dirawat plasma berpindah dari penipuan ke arah kumpulan muda. Untuk mengukur pemisahan kumpulan, kami mengira pengelompokan hierarki pada dua komponen utama. Dalam dendrogram, kumpulan muda dan kumpulan yang dirawat plasma dikelompokkan pada tahap ketidaksamaan yang lebih rendah (atau tahap persamaan yang lebih tinggi, 1120.9) daripada kumpulan yang tidak dirawat (3162.5) (Rajah S2). Keputusan ini menunjukkan bahawa ciri terpilih (pembolehubah atau baris dalam Rajah 2a) boleh digunakan untuk membuat kesimpulan biomarker metabolit yang berkaitan dengan penuaan dananti penuaan. Kami menganotasi ciri dengan metabolit yang diketahui menggunakan pangkalan data dalam domain awam [9].
Kami selanjutnya menilai fungsi dan kesalinghubungan metabolit yang dikenal pasti, menggunakan pemetaan KEGG (Ensiklopedia Kyoto Gen dan Genom) [10]. Untuk laluan tertentu, kami mengukur i) perwakilan berlebihan metabolit calon dan ii) kepentingannya (iaitu, kepusatan antara) [11] sebagai nod perantaraan utama antara pasangan metabolit lain (lihat Kaedah untuk butiran). Kami mendapati bahawa metabolisme asid arakidonik (AA) adalah laluan yang paling banyak diwakili (nilai-y tertinggi dalam Rajah 2c), dan metabolit dalam laluan itu cenderung untuk mencari di laluan komunikasi (nilai-x yang lebih tinggi dalam Rajah 2c) dan mengawal aliran maklumat. Di antara banyak metabolit dalam metabolisme AA, kami memilih AA sendiri sebagai biomarker; sebagai permulaan masuk ke dalam laluan, AA sahaja boleh menjadi wakil metabolit lain yang terganggu.
Penderia magneto-elektrokimia (cMES) yang kompetitif untuk pengesanan AA dalam plasma
Kami seterusnya menetapkan untuk memajukan sistem ujian di tapak yang pantas untuk pengesanan AA. Kami memilih untuk menggunakan teknologi penderiaan magneto-elektrokimia [12–17]. Ia menggabungkan pengayaan dan pengesanan sasaran ke dalam satu platform: manik magnetik (MB) digunakan untuk menangkap dan melabel sasaran molekul, dan sasaran terikat manik dikesan melalui penderiaan elektrokimia. Pendekatan ini mempunyai banyak kelebihan praktikal: i) sampel asli (plasma atau darah) boleh digunakan terus tanpa memerlukan penulenan sampel; ii) ujian mencapai sensitiviti pengesanan tinggi melalui pengayaan magnet dan penguatan isyarat enzimatik; iii) berdasarkan skema pengesanan elektrik, penderia boleh dikecilkan dengan mudah sebagai peranti mudah alih (Rajah 3a).
Pengesanan AA melalui penderiaan magneto- elektrokimia, bagaimanapun, menimbulkan cabaran teknikal; memandangkan AA ialah molekul kecil (~304.5 Da), immunoassay menggunakan sepasang antibodi AA sukar digunakan. Oleh itu, kami meneroka format ujian kompetitif (cMES; penderia magneto-elektrokimia kompetitif) yang memerlukan hanya satu antibodi AA (Rajah 3b). Untuk tangkapan sasaran, kami menyalut MB dengan antibodi AA (MBAb). Kami juga menyediakan agen pesaing (AA-HRP) dengan menggabungkan AA dengan enzim pengoksida (horseradish peroxidase, HRP). Secara khusus, kami menggunakan bentuk hapten; AA berkonjugasi pada albumin serum lembu (BSA), dan seterusnya mengaitkan HRP kepada pembawa BSA (Rajah S3). Untuk ujian cMES, sampel darah dicampur dengan MBAb dan AA-HRP. Jumlah AA-HRP sudah cukup untuk memenuhi tapak pengikat AA dalam MBAb (Kaedah). Ini akan membawa kepada pembezaan pemuatan HRP pada MB, bergantung pada jumlah AA endogen dalam sampel. Menambah secara berurutan pengantara elektron kromogenik (3,3',5,5'-tetramethylbenzidine, TMB) menghasilkan arus elektrik yang dibacakan oleh elektrod satah. Masa tindak balas untuk tangkapan AA dan pengeraman TMB telah dioptimumkan untuk memaksimumkan tahap isyarat (Rajah S4).

Rajah 3. Penderia magneto-elektrokimia yang kompetitif (cMES) untuk ujian AA. (A) Skema peranti. Peranti cMES mempunyai jejak yang kecil dan mampu
operasi di tapak. (B) Kami mencipta ujian elektrokimia yang kompetitif untuk pengesanan AA. Manik magnetik (MBAb) telah digabungkan dengan antibodi terhadap AA.
Sampel kawalan mengandungi AA-HRP sahaja dan dicampur dengan manik magnet. Sampel ujian dicampur dengan manik magnet dan AA-HRP. (C) Arus elektrik
diukur oleh pembaca cMES mudah alih. Dalam ujian cMES, magnitud semasa berkurangan dengan peningkatan kepekatan AA [AA]. Isyarat daripada kawalan
sampel tetapkan garis dasar untuk [AA]=0 ng/mL. Perbezaan semasa (∆I) antara kawalan dan sampel plasma yang disasarkan digunakan sebagai metrik analitik. (D)
Jumlah AA yang diketahui telah meningkat dalam serum dan diukur oleh cMES. Had pengesanan ialah ~ 126 ng/mL. (E) cMES dan ELISA dibandingkan untuk
konkordans. Keputusan daripada kedua-dua modaliti menunjukkan persetujuan yang baik (R2=0.959). Data dipaparkan sebagai min ± SEM daripada ukuran tiga kali ganda.
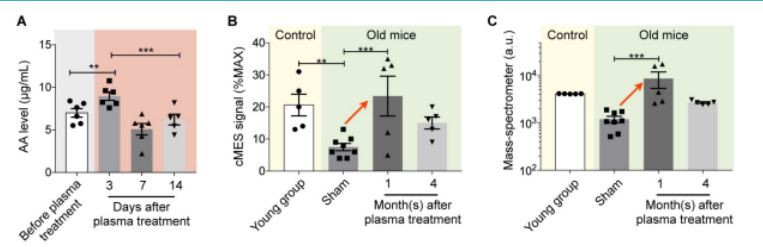
Rajah 4. Ukuran AA dalam sampel plasma. (A) Analisis kursus masa tahap AA tetikus selepas suntikan plasma. Kami menyuntik 13{{10}} μL plasma (kepekatan AA=7.2 µg/mL) ke dalam tikus (n=6) dan mengumpul darah tikus selepas 3, 7 dan 14 hari. Tahap AA darah tikus kemudian dipantau. Tahap AA meningkat dengan ketara pada hari ke-3 dan kembali ke paras normal selepas 7 hari. *p < 0.05;="" **p="">< 0.01;="" ***p="">< 0.001.="" (="" b="" )="" sampel="" plasma="" tikus="" telah="" diuji.="" dalam="" kumpulan="" kawalan="" (n="5)," tikus="" muda="" (umur,="" 5="" dan="" 8="" bulan)="" mempunyai="" tahap="" aa="" yang="" lebih="" tinggi="" daripada="" tikus="" tua="" yang="" dirawat="" secara="" palsu="" (umur,="" 20="" dan="" 23="" bulan;="" n="8)." bagi="" kumpulan="" yang="" dirawat="" plasma="" (n="5)," peningkatan="" yang="" berterusan="" dalam="" aa="" diperhatikan.="" *p="">< 0.05;="" **p="">< 0.01;="" ***p="">< 0.001.="" (c)="" sampel="" plasma="" daripada="" kohort="" yang="" sama="" seperti="" dalam="" (b)="" dianalisis="" dengan="" spektrometri="" jisim.="" tahap="" aa="" menunjukkan="" arah="" aliran="" yang="" sama="" seperti="" yang="" diukur="" oleh="" cmes.="" *p="">< 0.05;="" **p="">< 0.01;="" ***p="">< 0.001.="" data="" dipaparkan="" sebagai="" min="" ±="">
Hasil daripada ujian kompetitif, magnitud arus elektrik berkurangan dengan kepekatan AA plasma yang lebih tinggi ([AA]). Oleh itu, kami menyediakan sampel kawalan dengan mengeram MBAb dengan AA-HRP sahaja. Sampel kawalan digunakan untuk menetapkan garis dasar atas (iaitu, [AA]=0 ng/mL) untuk mengira perbezaan isyarat; arus elektrik daripada kawalan dan sampel plasma diukur, dan perbezaan bersih |∆I |=|Icontrol - Iplasma|telah diperolehi (Rajah 3c). begitu
ukuran pembezaan juga mengimbangi isyarat latar belakang biasa.
Percubaan pentitratan (Rajah 3d) menggunakan sampel yang dicucuk dengan jumlah AA yang berbeza-beza mendedahkan had pengesanan (LOD) sebagai ~125.9 ng/mL. LOD ujian adalah ~300-kali ganda lebih rendah daripada kepekatan AA biasa (38 µg/ml) dalam plasma tikus muda (5 bulan, n=2). Berdasarkan keputusan ini, kami mencairkan sampel plasma awal (100-kali ganda) dengan menambahkan larutan penimbal (lihat Kaedah). Isyarat daripada pengikatan tidak spesifik adalah hampir kepada tahap latar belakang intrinsik (~ 43 nA), yang berpotensi mendapat manfaat daripada faktor pencairan yang tinggi. Kami juga mengesahkan bahawa keputusan ujian sepadan dengan keputusan ELISA konvensional (R2=0.961, Rajah 3e). Ujian cMES, walau bagaimanapun, adalah lebih pantas (1 jam) daripada ELISA (4 jam), kebanyakannya disebabkan oleh kinetik pengikatan pantas; dalam cMES, MB menangkap AA dalam keseluruhan volum sampel (3-resapan dimensi), manakala tangkapan AA bergantung pada 1-resapan dimensi dalam ELISA berasaskan plat.
Pemantauan AA dalam tikus yang dirawat plasma
Kami menggunakan cMES untuk menganalisis tahap AA pada tikus selepas rawatan plasma tunggal. Oleh kerana AA secara semula jadi terdapat dalam darah tali pusat manusia, suntikan plasma secara tambahan akan meningkatkan tahap AA tetikus. Purata kepekatan AA daripada enam plasma darah tali pusat manusia yang berbeza ialah 7.2 ± 0.5 µg/mL (min ± SEM). Kami menyuntik 130 µL plasma darah tali manusia kepada tikus (n=6) dan memantau tahap AA mereka (Rajah 4a). Suntikan plasma segera meningkatkan paras AA darah (hari ke-3; p <0.01, berbanding="" semua="" titik="" masa="" lain),="" tetapi="" kesannya="" adalah="" sementara;="" tahap="" aa="" kembali="" normal="" 7="" hari="" selepas="" rawatan="" (p="0.34," berbanding="" titik="" masa="" sebelum="" suntikan="">
Kami seterusnya memantau tahap AA plasma selepas jadual rawatan penuh (Rajah S1). Tiga kohort tetikus berbeza telah digunakan: kumpulan umur yang dirawat plasma (n=8) dan palsu (n=8) (20-23 bulan) dan kumpulan kawalan muda (<8 months="" old,="" n="5)." we="" used="" 0.5="" µl="" of="" mouse="" plasma="" for="" each="" measurement.="" the="" sham="" group="" showed="" lower="" aa="" level="" compared="" to="" the="" young="" group="" (p="0.003," fig.="" 4b).="" the="" plasma="" treated="" group,="" however,="" showed="" increased="" aa="" levels="" even="" after="" 1="" month="" after="" the="" treatment.="" the="" effect="" was="" sustained="" up="" to="" 4="" months="" post="" treatment;="" the="" plasma-treated="" group="" had="" higher="" aa="" level="" than="" the="" sham="" group="" (p="0.0003)." we="" also="" analyzed="" aliquots="" of="" samples="" via="" lc/ms="" (fig.="" 4c).="" the="" results="" from="" both="" assays="" were="" concordant,="" corroborating="" aa's="" value="" as="" a="">
Rawatan plasma yang membawa kepada peningkatan kognitif dan tingkah laku pada tikus tua
Kami selanjutnya menilai fenotip tingkah laku kohort haiwan, terutamanya menilai pembelajaran motor dan fungsi ingatan mereka. Kami melakukan {{0}}ujian rotarod percubaan pada 1 dan 4 bulan selepas rawatan plasma atau palsu (Rajah 5a); kependaman (masa berjalan) tetikus sebelum terjatuh pada rod berputar digunakan untuk menilai prestasi motor haiwan. Pada 1 bulan selepas rawatan (20-bulan), kependaman kedua-dua kumpulan palsu dan yang dirawat plasma adalah jauh lebih rendah (p < 0.0001)="" berbanding="" kumpulan="" muda="" (5-bulan).="" )="" kumpulan="" (rajah="" 5b).="" kumpulan="" yang="" dirawat="" plasma,="" bagaimanapun,="" menunjukkan="" peningkatan="" secara="" beransur-ansur="" dalam="" pembelajaran="" motor="" dan="" ingatan,="" manakala="" fakulti="" yang="" sama="" merosot="" dalam="" kumpulan="" palsu.="" perubahan="" dalam="" tahap="" aa="" meneruskan="" perubahan="" tingkah="" laku,="" yang="" boleh="" berfungsi="" sebagai="" penunjuk="">anti penuaankesan rawatan (Rajah 5c).
Analisis tisu otak (Rajah 5d, 5e) menunjukkan bahawa tikus tua (kumpulan palsu) mempunyai kawasan sel positif DCX yang lebih kecil dalam zon sub-ventrikel berbanding tikus muda. Sebaliknya, kawasan sel positif DCX meningkat dalam haiwan yang dirawat plasma dan kekal tidak berubah (p=0.04) menunjukkan bahawa plasma darah tali pusat yang disuntik merangsang neurogenesis otak lama. Keputusan menunjukkan potensi manfaat rawatan plasma pada neurogenesis yang berterusan yang menghasilkan fungsi motor yang lebih baik dalam kumpulan yang dirawat.
Perbincangan
Kemajuan dalam terapi peremajaan secara serentak meningkatkan keperluan untuk ukuran objektif dan kuantitatif untuk membaca keberkesanan rawatan. Oleh itu, kami merancang kajian kami untuk mengenal pasti biomarker molekul yang boleh menerangkan ciri fenotip penuaan dananti penuaanrawatan. Eksperimen haiwan kami membawa kepada pemerhatian berikut: i) profil metabolit kohort tikus muda dan dewasa jelas berbeza; dan ii) menyuntik plasma kord manusia ke dalam tikus tua mengubah corak metabolit mereka lebih dekat dengan tikus muda. Menariknya, kami mendapati asid arakidonik (AA) sebagai biomarker pengganti yang paling berkesan untukanti penuaanrawatan; Metabolisme AA sangat tidak terkawal pada tikus muda dan tikus yang dirawat plasma, dan didapati memainkan peranan penting dalam berinteraksi dengan laluan metabolik lain seperti metabolisme asid linoleik [10, 18].
Kami terus membangunkan sistem penderia mudah alih (cMES) yang pantas untuk memudahkan pengesanan AA dalam penyelidikan rutin dan tetapan klinikal. Kami secara khusus menyepadukan skim ujian kompetitif dengan pengayaan imunomagnet dalam usaha untuk mengesan sasaran molekul kecil (iaitu, metabolit) terus daripada sampel plasma. Gabungan ini membawa kelebihan berikut. (i) Ujian ini mendapat manfaat daripada kinetik pengikatan pantas, kerana manik magnet menangkap AA dalam keseluruhan volum sampel (3-resapan dimensi). (ii) Proses ujian (cth, langkah mencuci) dipermudahkan dengan magnet luar yang digunakan untuk pengumpulan manik. (iii) Dengan menumpukan manik terikat AA secara magnetik berhampiran elektrod pengesanan, isyarat analisis keseluruhan boleh dipertingkatkan (~72 peratus ) [12]. Sesungguhnya, kami menunjukkan bahawa ujian cMES menggunakan<1 µl="" of="" plasma="" with="" the="" total="" assay="" time="" within="" 1.5="" hour.="" both="" cmes="" and="" mass="" spectrometry="" consistently="" showed="" that="" plasma="" aa="" levels="" decrease="" with="" aging,="" but="" that="" they="" reversely="" increase="" with="" cord-plasma="" treatment.="" importantly,="" increases="" in="" aa="" levels="" could="" be="" an="" early="" indicator="" of="" improved="" cognitive="" functions="" in="" treated="" animals.="" these="" results="" highlight="" the="" utility="" of="" aa-cmes;="" with="" minimally="" invasive="" blood="" draw,="" individual="" patients="" can="" be="" monitored="" in="" a="" serial="" fashion="" to="" better="" assess="" treatment="">

Rajah 5. Ujian tingkah laku dan molekul. (A) 2-ujian Rotarod percubaan telah dijalankan pada 1 dan 4 bulan selepas suntikan plasma. (B) Kumpulan yang dirawat plasma
menunjukkan peningkatan progresif dalam koordinasi motor; persembahan adalah hampir dengan kumpulan muda pada akhirnya (percubaan kedua pada 3 bulan). Masa berjalan kumpulan sham berkurangan dengan penuaan. *p < 0.05;="" **p="">< 0.01.="" (c)="" bagi="" kumpulan="" yang="" dirawat="" plasma,="" peningkatan="" tahap="" aa="" mendahului="" peningkatan="" fungsi="" motor.="" *p="">< 0.05;="" **p="">< 0.01;="" ***p="">< 0.001.="" (d)="" sel-sel="" otak="" dalam="" zon="" subventrikular="" telah="" diimunisasi="" untuk="" penanda="" neurogenesis,="" doublecortin="">
Bar skala ialah 50 µm. Ambil perhatian bahawa kumpulan palsu mempunyai kawasan sel positif DCX yang lebih kecil dalam zon sub-ventrikular daripada tikus muda, manakala kawasan itu meningkat dalam haiwan yang dirawat plasma dan kekal tidak berubah. (E) Kawasan sel positif DCX dalam imej (D) diukur. *p < 0.05;="" ***p=""><>
AA telah ditunjukkan untuk menggalakkan pertumbuhan otot dan perkembangan otak [19, 20]. Laporan lain juga menyerlahkan potensi manfaat AA dalamanti penuaan[21, 22]. Kajian semasa adalah selaras dengan penemuan ini, tetapi skopnya terhad untuk mewujudkan hubungan korelatif antara tahap AA dananti penuaanfenotip. Pemantauan AA bersiri, bagaimanapun, menunjukkan bahawa peningkatan AA dalam tikus yang dirawat plasma mungkin daripada sumber endogen, bukan daripada plasma yang ditransfusikan. Lebih-lebih lagi, berterusananti penuaankesan diperhatikan pada tikus penerima walaupun 4 bulan selepas tamat rawatan plasma. Pembelajaran motor dan fungsi ingatan bertambah baik; dan bilangan sel prekursor neuron meningkat dalam otak. Pemerhatian ini sangat mencadangkan perubahan fisiologi dalam tikus yang dirawat plasma; mekanisme yang tepat masih belum dijelaskan.
Beberapa batasan lain kajian ini harus ditangani dalam penyelidikan masa depan. Pertama, ujian cMES perlu diperhalusi untuk ketepatan yang lebih tinggi. Khususnya, dengan kekurangan sampel negatif sebenar (iaitu, sampel darah tanpa sebarang AA endogen), adalah sukar untuk mengambil kira isyarat daripada pengikatan tidak spesifik. Boleh dibayangkan, kesan matriks darah mungkin boleh diabaikan kerana kami mencairkan sampel sebanyak 100-kali ganda. Andaian sedemikian, walau bagaimanapun, perlu disahkan dengan menggunakan sampel plasma yang dipadamkan AA yang boleh disediakan daripada model tetikus kekurangan AA [23] atau melalui pengurangan imun AA. Kedua, kami memberi tumpuan kepada mengesan metabolit tunggal dalam metabolisme AA untuk kesederhanaan, tetapi pendekatan ini mungkin mengabaikan konteks biologi seperti interaksi antara metabolit dalam laluan tertentu. Termasuk panel metabolit akan lebih baik menangkap gangguan metabolik dan juga meningkatkan ketepatan diagnostik. cMES boleh diskalakan dengan mudah untuk mengesan pelbagai penanda sambil menggunakan jumlah sampel yang kecil. Ketiga, menginterpolasi penemuan semasa kepada manusia akan menjadi mencabar. Walaupun tikus dan manusia berkongsi laluan metabolik yang sama, tikus mempunyai 7-kali ganda kadar metabolisme lebih tinggi daripada manusia [24]. Percubaan manusia adalah perlu untuk menentukan dos plasma optimum untuk infusi dan untuk menetapkan garis dasar untuk biomarker; dimaklumkan oleh kajian haiwan, kami merancang kajian manusia sedemikian. Usaha ini akan mempercepatkan pembangunananti penuaanterapi, meningkatkan kualiti kehidupan individu serta mengurangkan beban masyarakat.

Kaedah
Reka bentuk eksperimen
Plasma telah diasingkan daripada darah tali pusat manusia yang dikumpulkan semasa bersalin. Plasma darah tali pusat diberikan melalui infusi intravena kepada tikus tua (18-bulan), dan kawalan palsu (18-bulan) dan tikus muda (3-bulan sebagai positif kawalan) telah disuntik dengan garam. Pada 1 dan 4 bulan selepas pemindahan, 2-ujian rotarod percubaan telah dijalankan untuk menilai koordinasi motor dan ingatan jangka panjang (Rajah S1). Profil metabolit yang tidak disasarkan telah dilakukan pada darah daripada tiga kumpulan dan analisis bioinformatik menentukananti penuaanlaluan yang berkaitan (metabolisme asid arakidonik). Biosensor dibangunkan untuk mengesan asid arakidonik peredaran darah dengan mudah dan cekap.
Penyediaan sampel darah tali pusat
Darah tali pusat manusia dikumpulkan di bawah Lembaga Semakan Institusi Hospital Besar CHA (Seoul, Korea, LHDN No. CHAMC-2015- 08-130-009). Darah tali pusat manusia telah didermakan daripada 4 penderma dan dirawat dengan sitrat-fasa-dekstrosa dengan antikoagulan adenine (CPDA-1). Plasma darah tali pusat manusia diasingkan dengan sentrifugasi pada 2,000 g selama 15 minit pada suhu bilik. Sampel plasma terpencil disimpan pada -80 darjah dan digunakan dengan satu kitaran pencairan beku pada suhu bilik.
Eksperimen haiwan
Protokol haiwan telah diluluskan oleh Jawatankuasa Penjagaan dan Penggunaan Haiwan Institusi Universiti CHA (IACUC). Kami menggunakan 18-tikus betina C57BL/6 sebulan untuk menilai gangguan metabolik dan fenotip tingkah laku yang berkait dengan penuaan dananti penuaan. Kawalan positif ialah 3-tikus betina C57BL/6 bulan. Semua tikus dibiakkan pada suhu bilik dalam kitaran standard 12 jam terang-gelap. Bagi tikus dewasa, plasma darah tali pusat atau garam (130 µL) disuntik secara intravena 12 kali selama 4 minggu. Plasma darah tali pusat manusia yang terpencil tidak dikumpulkan, dan haiwan tertentu menerima plasma darah tali pusat daripada penderma yang sama. Bilangan haiwan yang digunakan dalam setiap eksperimen diterangkan dalam bahagian kaedah yang sepadan. Plasma dikumpulkan melalui sentrifugasi (3,000} g, 15 minit pada suhu bilik).
Pemerolehan metabolit dan analisis data
Untuk profil metabolit bawaan darah, darah dikumpulkan daripada tikus melalui tusukan jantung pada titik masa yang ditetapkan: kumpulan muda (3-berumur sebulan, n=10), kumpulan palsu ({{ 4}}bulan, n=10; 23-bulan, n=12), kumpulan yang dirawat plasma (20-bulan, n {{13 }}; 23-berumur sebulan, n=5). Sampel darah dianalisis menggunakan sistem spektrometri jisim kromatografi cecair (LC-MS) (Agilent). Kami menukar fail LC/MS ke dalam format mzXML standard (ProteoWizard) [25] dan kemudian memprosesnya menggunakan MAIT (kit alat pengenalan automatik metabolit) [26] untuk pengesanan ciri, analisis statistik dan pengenalan metabolit. Ciri-ciri ketara secara statistik (iaitu, metabolit terion dan/atau berpecah) telah dikenal pasti melalui analisis varians (ANOVA). Ciri-ciri ini telah dipadankan dengan semua kemungkinan metabolit diduga dalam pangkalan data metabolom [9] berdasarkan nisbah jisim/cas bagi ion spektrum jisim (toleransi m/z 0.005). Kami mencirikan perubahan metabolit global melalui analisis pengelompokan hierarki dan struktur data metabolomik yang wujud melalui analisis komponen utama (PCA). Dua atau tiga replika teknikal (memastikan variasi teknikal jauh lebih kecil daripada variasi biologi) setiap tetikus dimasukkan dalam pembelajaran tanpa pengawasan seperti PCA dan pengelompokan hierarki. Pengelompokan hierarki pada komponen utama (HCPC) telah dilakukan oleh FactoMineR, pakej R [27]. Untuk analisis berfungsi, laluan metabolik yang paling mungkin terganggu oleh penuaan dan rawatan plasma ditentukan melalui analisis laluan KEGG (MetaboAnalyst 3.0) [28]. Taburan hipergeometrik digunakan untuk mengukur perwakilan berlebihan metabolit yang dipadankan dalam laluan KEGG tertentu.
Penyediaan manik immunomagnet
Manik magnetik (5 mg) disalut dengan kumpulan epoksi (Dynabeads M-270 Epoxy, Invitrogen) digantung dalam 100 µL larutan natrium fosfat 0.1 M. Seratus mikrogram antibodi terhadap asid arakidonik (Biomatik) telah ditambah dan dicampur dengan teliti. Seratus mikroliter larutan ammonium sulfat 3 M telah ditambah, dan campuran itu diinkubasi pada suhu bilik selama 2 jam dan kemudian diinkubasi lagi pada 4 darjah selama semalaman dengan putaran kecondongan perlahan. Tindak balas konjugasi telah dijalankan pada pH=7.4. Proses ini mendorong pembentukan ikatan kovalen antara kumpulan epoksi (manik) dan amina (antibodi), yang sebelum ini kami sahkan dengan menundukkan konjugat manik antibodi kepada cabaran pH [29]. Secara purata 2.4 × 104 antibodi tidak bergerak setiap manik. Manik magnet konjugasi antibodi dipisahkan dengan magnet kekal, dibasuh dua kali dengan larutan PBS, dan digantung semula dalam 200 µL PBS dengan 1 peratus BSA. Manik disimpan dalam 4 darjah sehingga satu bulan.
Konjugasi HRP kepada asid arakidonik
HRP kemudiannya dikonjugasikan kepada BSA melalui kimia aminasi reduktif. Khususnya, 100 µg AA terkonjugasi BSA (RPU51089, Biomatik) telah dilarutkan dalam 0.5 mL penimbal karbonat-biokarbonat 0.2 M (pH 9.4), ditambah kepada satu miligram pautan EZ terliofil. Plus Activated Peroxidase (Thermo Scientific), dan diinkubasi selama 1 jam pada suhu bilik. Seterusnya, 10 µL sodium cyanoborohydride (Thermo Scientific) telah ditambah dan adunan tersebut diinkubasi selama 15 minit pada suhu bilik. Akhir sekali, 20 µL penimbal Quenching (Thermo Scientific) telah ditambah, diikuti dengan pengeraman 15 minit pada suhu bilik. Elektroforesis gel dan analisis jalur protein mengesahkan konjugasi HPR kepada BSA-AA (Rajah S3a). AA konjugasi HRP dikumpulkan dan ditumpukan dengan penapis emparan Amicon Ultra 100K (Millipore). Baki peroksidase dan BSA-AA telah dibasuh dengan PBS selama empat kali.
Pengesanan elektrokimia AA dalam sampel plasma
Untuk pengesanan elektrokimia AA, darah dikumpul daripada kumpulan muda (n {{0}}), sham (n=8), dan kumpulan yang dirawat plasma (n=5 selama 1 bulan dan n=5 selama 3 bulan). Sampel plasma tetikus (0.5 µL) telah dicairkan dalam 50 µL 1 peratus BSA dalam PBS (x{11}}pencairan kali ganda) dan dicampur dengan larutan manik immunomagnet (50 µL) dan larutan AA terkonjugasi HRP (50 µL). Jumlah AA-HRP cukup besar untuk memenuhi tapak pengikatan dalam manik magnet. Kami menggunakan kira-kira 8.4×107 manik setiap ujian, yang menyediakan tapak pengikat AA 2.0×1012. Jumlah AA-HRP ialah ~1.7×1013; nisbah antara AA-HRP dan tapak pengikat ialah ~8:1. Campuran diinkubasi pada suhu bilik selama 1 jam dengan putaran kecondongan perlahan. Manik kawalan disediakan dengan mencampurkan 1 peratus BSA dalam PBS (50 µL) dengan larutan manik immunomagnet (50 µL) dan larutan AA terkonjugasi HRP (50 µL). Semua manik yang bertindak balas dipisahkan dengan magnet kekal dan dibasuh dua kali dengan 80 µL PBS (1 peratus BSA). Akhirnya, manik digantung semula dalam 7 µL PBS. Larutan manik yang disediakan dan 20 µL larutan TMB (Biomatik) telah dimuatkan di atas elektrod. Selepas 6 minit, pengukuran kronoamperometri dimulakan. Kami menggunakan sensor elektrokimia kecil (sistem prototaip yang dibangunkan oleh AcurreHealth Inc.). Tahap semasa dalam julat 40-45 s telah dipuratakan. Kami menggunakan faktor penukaran (×100) untuk melaporkan anggaran kepekatan AA asal dalam plasma.
Ujian imunosorben berkaitan enzim (ELISA)
Eksperimen ELISA dilakukan menggunakan kit ELISA (Biomatik) asid arakidonik tikus (AA) mengikut garis panduan pembuatan. AA yang dicairkan secara bersiri telah ditambah ke dalam setiap telaga, dan diinkubasi dengan AA konjugasi HRP pada 37 darjah selama 40 minit. Selepas mencuci dengan penimbal pencuci selama empat kali, larutan TMB ditambah dan diinkubasi selama 20 minit. Perkembangan warna telah dihentikan dengan menambahkan penyelesaian hentian. Penyerapan dibaca pada 450 nm menggunakan pembaca plat mikro (Tecan).
Ujian Rotarod
Kami mengubah suai ujian Rotarod Kong et al. [30] untuk menilai koordinasi lokomotor. Rotarod dengan rod diameter 3-cm bermula pada 4 rpm dan dipercepatkan sebanyak 4 rpm setiap 30 saat selama 5 min. Tikus diletakkan di atas joran, dan masa yang diambil untuk tikus jatuh dari joran diukur. Setiap tetikus diberi 3 percubaan sehari, dan masa berjalan setiap hari dikira sebagai purata masa latihan. Ujian rotarod pertama dijalankan pada 1-bulan selepas rawatan plasma: kumpulan muda (n=29), kumpulan palsu (n=17), kumpulan dirawat plasma (n {{ 11}}). Sesi latihan semula telah dimulakan pada 4-bulan selepas rawatan plasma. Untuk mengelakkan latihan berlebihan, latihan semula telah dijalankan selama 2 hari. Prosedur lain adalah sama seperti sesi pertama.
Pengimejan tisu otak
Pada 1 bulan (n=4) dan 4 bulan (n=3) selepas suntikan plasma darah tali pusat manusia atau suntikan salin, haiwan telah dieuthanasikan dan kemudian direndam dengan 4 peratus paraformaldehid (PFA) dan PBS melalui ventrikel kiri. Kumpulan muda (n=5) dan kumpulan palsu (n=4) digunakan sebagai kawalan. Otak mereka adalah
diekstrak dan dilindungi krio. Setiap otak dipecahkan pada cryotome pada ketebalan 30 μm. Kepada
melakukan imunohistokimia, pengikatan tidak spesifik telah disekat dengan 5 peratus serum kambing normal dalam 0.3 peratus Triton X-100 selama 40 minit. Antibodi utama terhadap Doublecortin (DCX; 1:400, Cell Signaling, #4604S) telah digunakan semalaman pada 4 darjah, dan kemudian PBS digunakan untuk mencuci [31]. Antibodi sekunder Alexa Fluor 488 (1:2000, Invitrogen, #A11008) telah digunakan untuk pengesanan DCX. Imej diambil menggunakan mikroskop pendarfluor (Nikon Eclipse 80i) dan dianalisis menggunakan Imej J [32].
Analisis statistik
Analisis statistik dilakukan menggunakan fungsi asas R dan lme4, pakej R untuk sama ada Linear
Model Kesan Campuran atau Model Linear Umum
(GLM) diikuti dengan ujian post-hoc LSD [33]. Data dibentangkan sebagai min ± ralat standard dan nilai ap < 0.05="" dianggap="">
Bahan Tambahan
Angka tambahan.
http://www.thno.org/v09p0001s1.pdf
Ucapan terima kasih
Kami berterima kasih kepada AccureHealth Inc. kerana menyediakan penderia elektrokimia kecil. Kajian ini sebahagiannya disokong oleh geran Institut Promosi Teknologi Maklumat dan Komunikasi (IITP) yang dibiayai oleh Kerajaan Korea (MSIT) (2017M3A9B4025699).
Minat Bersaing
Penulis telah mengisytiharkan bahawa tiada kepentingan bersaing wujud.
