Pandangan Komprehensif Mengenai Kitaran Kanser-Imuniti (CIC) dalam Kanser Serviks Pengantaraan HPV Dan Prospek Untuk Peluang Terapeutik Yang Muncul Bahagian 2
Jul 31, 2023
2.2. Tangkapan dan Pemprosesan Antigen (Langkah 2)
Sel penyampai antigen (APC) dicirikan dengan mempunyai reseptor pengecaman corak (PRR) pada permukaan luar membrannya, yang mempunyai kapasiti untuk mengenali pelbagai jenis eksogen (corak molekul berkaitan patogen—PAMP) dan antigen endogen (kerosakan). -corak molekul yang berkaitan—DAMPs) [68]. Pengikatan antigen dengan PRR mencetuskan laluan isyarat yang membolehkan internalisasi, pemprosesan, dan pembentangan seterusnya kepada sel imun adaptif (CIC-langkah 2) [68]. Perubahan dalam mekanisme ini juga telah diperhatikan semasa pembangunan CC. Kajian telah menunjukkan bahawa salah satu sebab utama jangkitan HPV berterusan adalah keupayaan virus untuk mengganggu reseptor dan deria imuniti semula jadi dan dengan itu mengelak sistem imun perumah.
Sehubungan dengan ini, didapati bahawa Reseptor seperti tol (TLR) 9 memainkan peranan penting dalam sistem tindak balas imun terhadap jangkitan HPV dan neoplasma serviks [69]. Penyiasatan in vitro dan in vivo menunjukkan bahawa ekspresi diubah TLR9 dikaitkan dengan persekitaran mikro tumor dalam kanser serviks berkaitan HPV [69-73]. Kajian ekspresi gen lain hanya mendapati penurunan ketara dalam TLR1 dan peningkatan dalam TLR3 daripada sel epitelium dalam karsinoma serviks [74]. Di samping itu, kehadiran reseptor TLR4 telah dikaitkan secara positif dengan keadaan hipoksia persekitaran mikro tumor dan untuk mencirikan perubahan ini dengan cara yang sepadan dengan peringkat dan subtipe CC yang berbeza dan dengan itu dapat membezakan dengan lebih jelas fungsinya. dalam tindak balas imun antitumor.
Hasil daripada interaksi antara APC dan persekitaran mikro tumor, APC mungkin mempunyai bilangannya dikurangkan dan fungsinya diubah [76,77]. Penurunan bilangan APC berlaku kedua-dua daripada pengurangan dalam APC pemastautin dan APC migrasi. Pada awalnya, perlu diingatkan bahawa kitaran jangkitan HPV dengan sendirinya merupakan mekanisme pengelakan untuk sistem imun hos kerana replikasi virus dan pembebasan zarah virus baru tidak menyebabkan lisis sel, kerana kematian keratinosit diprogramkan. Oleh itu, terdapat sama ada pengurangan atau kekurangan lengkap sitokin pro-radang yang mengaktifkan penghijrahan APC [78]. Malah, perubahan telah ditemui dalam ekspresi beberapa sitokin yang merangsang penghijrahan APC ke tumor. Sebagai contoh, dalam sel CC, pengurangan penghijrahan APC ke epitelium serviks untuk pengambilan antigen disebabkan oleh penurunan regulasi ligan motif CC chemokine (CCL) 2, CCL20, dan ligan chemokine (motif CXC) (CXCL) 14 [79– 81]. Di samping itu, kajian in vitro dan in vivo CC mendapati bukti penurunan regulasi penanda CD11b dan CD207 LC, yang menjejaskan penangkapan antigen dan mengurangkan pembezaan dan kematangan sel dendritik (DC) [79-81]. Terdapat bukti untuk menunjukkan bahawa sasaran HPV CCL20 adalah kemokin yang menarik sel sel Langerhans (LC), yang mengganggu laluan NF-κB [79]. Laluan ini mengawal ekspresi pelbagai gen yang terlibat dalam proses pro dan antiradang, seperti kemokin, sitokin, dan molekul lekatan [82]. Strategi pengelakan imun lain yang digunakan oleh HPV untuk menghalang laluan NF-κB termasuk interaksi onkoprotein virus dengan faktor berkaitan P300/CBP (PCAF) dan pengawalseliaan UCHL1 [83-85].
Tambahan pula, kajian telah menunjukkan bahawa onkoprotein HPV mengganggu interaksi antara keratinosit dan LC melalui molekul lekatan. Jumlah LC yang rendah timbul daripada penurunan ekspresi kadherin dan protein lekatan yang terdapat dalam CC [77,86]. Walau bagaimanapun, kajian terbaru yang melibatkan penggunaan model in vivo menunjukkan bahawa walaupun penurunan dalam E-cadherin mengubah morfologi LC, ia tidak penting untuk memastikan ia kekal dalam epitelium [87]. Selain itu, oncoprotein HPV E5 mengecilkan kelas I kompleks histokompatibiliti utama (MHC) permukaan sel dengan mengganggu persembahan antigen dan oleh itu pengiktirafan sel yang dijangkiti HPV oleh limfosit T sitotoksik [88,89]. Walau bagaimanapun, kajian lanjut masih diperlukan untuk meneroka perubahan yang dilaporkan dalam mekanisme dalaman pemprosesan antigen dalam APC, termasuk faktor seperti interaksi dengan strain HPV yang berbeza, ciri histologi, rangsangan persekitaran mikro, dan peringkat klinikal, dan untuk menentukan dalam apa cara ini boleh mempengaruhi tindak balas imun antitumor dengan ketara.
Variasi genetik, seperti polimorfisme, boleh menjejaskan pelbagai aspek sistem imun, termasuk penangkapan dan pemprosesan antigen. Implikasi fungsi variasi genetik ini bergantung pada bentuk dan kedudukan variasi dalam genom dan boleh berkisar daripada perubahan yang boleh diabaikan kepada perubahan yang ketara dalam fungsi gen. Analisis bioinformatik dalam bidang reseptor TLR telah mendedahkan bahawa polimorfisme berpotensi menjejaskan tapak pengikatan untuk faktor transkripsi dan mengganggu pengaktifan laluan isyarat TLR.
Walau bagaimanapun, keupayaan inferens fungsi alat ini adalah terhad dan penyelidikan tambahan diperlukan untuk memahami sepenuhnya mekanisme molekul di sebalik perubahan ini [90]. Sementara itu, meta-analisis telah dijalankan untuk menyiasat kesan variasi gen TLR9 dan TLR2 yang lazim (TLR9 1486 T/C, TLR9 G2848A, TLR2– 196 hingga −174 del/in) ke atas kejadian CC. Analisis mendedahkan bahawa polimorfisme TLR9–1486T/C (rs187084) dikaitkan dengan peningkatan risiko CC, manakala tiada pautan ditemui dengan varian TLR2–196 hingga -174 del/ins [72,73]. Begitu juga, kajian lain menunjukkan bahawa varian IL-12B rs3212227 dan TLR9 rs352140 tidak didapati meningkatkan kemungkinan CC dalam apa jua cara. Sebaliknya, variasi genetik XRCC3 RS861539, TNF- rs1800629 dan IL-6 rs1800795 telah dikaitkan [91]. Satu lagi analisis polimorfisme gen mendedahkan bahawa genotip GG bagi rs311678 SNP dalam gen GMP-AMP (cGAMP) kitaran laluan STING (stimulator gen interferon) dikaitkan dengan pengurangan risiko lesi prakanser serviks dengan ketara. Selain itu, kajian yang sama juga mendapati interaksi antagonis yang ketara antara jangkitan HPV dan polimorfisme rs311678 pada skala tambahan menggunakan model interaksi tiga lokus, yang melibatkan jangkitan HPV, julat umur untuk menarche, dan rs311678 SNP dalam cGAS [92]. Polimorfisme juga boleh mempengaruhi gen yang bertanggungjawab untuk subunit proteasom dalam MHC-I, yang berpotensi mempengaruhi persembahan antigen. Polimorfisme rs2071543 didapati dikaitkan dengan peningkatan risiko CC berkaitan HPV apabila hadir sebagai genotip T/T dan T/G daripada proteasome 8 subunit beta dan genotip A/A dan A/G subunit 9 [93 ].
Meta-analisis yang dijalankan baru-baru ini telah meneroka hubungan antara SNP bukan pengekodan dan lesi prakanser dan CC. Kajian itu meneliti 48 polimorfisme dan mendapati 16 SNP (berkaitan dengan protein imun, termasuk interleukin, interferon, TLR, TNF, CTLA, dan metalloproteinase), yang berkait rapat dengan peningkatan risiko CC [94]. Atas dasar ini, boleh dihipotesiskan bahawa polimorfisme diperhatikan secara meluas dalam gen yang berkaitan dengan sistem tindak balas imun terhadap CC berkaitan HPV dan mungkin mewakili penyesuaian yang berkembang kepada persekitaran yang dinamik. Walau bagaimanapun, hasil kajian polimorfisme mungkin berbeza antara populasi dan etnik yang berbeza. Terdapat juga beberapa batasan untuk kajian ini, termasuk: (a) perbezaan dalam kajian yang termasuk dalam meta-analisis, (b) bilangan kajian yang rendah yang meneliti polimorfisme tertentu, dan (c) kemungkinan bias penerbitan. Walau bagaimanapun, menjalankan pengesahan eksperimen tentang perbezaan fungsi antara polimorfisme genetik yang berkaitan dengan karsinogenesis yang disebabkan oleh HPV boleh membantu dalam pembangunan imunoterapi yang disasarkan untuk populasi tertentu.
2.3. Penyebuan dan Pengaktifan Sel Imun (Langkah 3)
Selepas penangkapan dan pemprosesan antigen, penyebuan dan pengaktifan sel T berlaku daripada sel T naif (langkah 3) (Rajah 1). Ini memerlukan APC untuk berhijrah ke nodus limfa. Walau bagaimanapun, pengurangan kapasiti migrasi yang dikaitkan dengan ekspresi rendah CCR7, reseptor yang diperlukan untuk keluar sel T dari tisu periferi dan kemasukan ke nodus limfa, diperhatikan dalam DC yang menyusup tumor [95]. Antara mekanisme yang terlibat, terdapat bukti bahawa protein E6 dan E7 daripada HPV menurunkan CCR7 dengan menaikkan IL-6 dalam saluran sel kanser serviks [96,97]. Sebaliknya, model in vitro menunjukkan bahawa LC daripada CC yang dirangsang oleh s-Poly-I:C mengekspresikan CCR7 dan meningkatkan penghijrahan ke ligan mereka (CCL21), yang menggariskan kepentingan ekspresi mereka untuk penghijrahan LC ke nodus limfa untuk menyebukan sel-T [98,99].
Sebaik sahaja APC menyusup ke nodus limfa, mereka bertemu dengan sel T naif, di mana mereka memulakan penyebuan dan pengaktifan mereka. Dalam fasa ini, telah diperhatikan semasa ujian in vivo CC bahawa terdapat sel-sel T CD8 utama LC dengan aktiviti proliferatif sederhana, pengeluaran IFN- yang rendah, dan tahap IL-10 yang tinggi [100] dan IL-17A [101]. Dalam kes khusus IL-10 (sitokin antiradang), perlu diperhatikan bahawa dalam CC, keratinosit, makrofaj dan LC juga mempunyai peningkatan pengeluaran IL-10 [102], dan satu kajian diperhatikan. bahawa sel Treg, secara in vitro, melalui kesan IL-10, mengurangkan kapasiti pengaktifan sel T naif, yang boleh ditafsirkan sebagai mekanisme maklum balas tindak balas imun [102,103]. Telah ditunjukkan bahawa penurunan tahap ekspresi miR{15}} mungkin dikaitkan dengan jangkitan HPV dan mewujudkan persekitaran mikro yang menggalakkan untuk karsinogenesis dengan mengurangkan ekspresi IFN dan meningkatkan ekspresi IL-10 [104,105]. Di samping itu, model in vivo menggunakan tikus K14E7 yang mengekspresikan protein E7 HPV-16, menunjukkan penurunan dalam penyebuan sel T CD8 tambah oleh LC [106], pengurangan bilangan sel Th1 yang disiapkan oleh DC, dominasi penyebuan sel-T dengan Foxp3 plus fenotip, dan ekspresi tinggi CD73 dan reseptor folat 4, daripada CD4 ditambah T-sel naif [107]. Walau bagaimanapun, secara tidak dijangka, kajian lain yang menggunakan model tikus in vivo yang menyatakan protein E7 HPV-16, walaupun memperoleh pengurangan bilangan dan penanda pengaktifan LC; lebih-lebih lagi, penurunan dalam penyebuan CD8 ditambah sel-T sitotoksik adalah bebas daripada LC [108].
Pemerhatian terakhir mungkin berkaitan dengan fakta bahawa terdapat beberapa subjenis APC dan ini seterusnya menunjukkan peringkat pematangan yang berubah-ubah. Untuk menyokong ini, kajian in vitro memberikan bukti bahawa sel-sel utama CD8 plus T-sel subjenis Langerin− DC mempunyai aktiviti proliferatif yang tinggi, pengeluaran IFN- yang tinggi, dan IL yang rendah-10 [109]. Walau bagaimanapun, kajian lanjut diperlukan di mana subtipe APC terlibat secara langsung dalam menyebu dan mengaktifkan setiap subjenis sel T, bergantung pada subjenis CC. Oleh itu, sebagai contoh, apabila subtipe sel T dibandingkan dalam nodus limfa yang mengeringkan tumor daripada adenokarsinoma serviks (ADC), terdapat kehadiran sel-T yang lebih besar, dengan dominasi sel Tregs, CD8 ditambah sel T dengan lebih tinggi. profil 'ekzos', tahap CD8 tambah sel T memori pusat yang lebih tinggi (TMC CD27 tambah CD45RA−), dan sel T memori efektor CD8 (TEM CD27−CD45RA−) berbanding karsinoma sel skuamosa serviks (SCC) [110]. Oleh itu, terdapat perbezaan (dari sudut penyebuan dan pengaktifan sel-T) antara subtipe histologi CC yang perlu diterokai.
2.4. Penghijrahan Sel Imun ke Tumor (Langkah 4)
Berikutan ini, sel-T yang disiapkan dan diaktifkan oleh APC mesti berhijrah ke tumor (Langkah 4). Seperti yang diperhatikan dalam langkah sebelumnya, beberapa keabnormalan telah ditemui. Oleh itu, kehadiran kemokin tertentu telah terbukti sangat penting. Sebagai contoh, sel CC telah meningkatkan pengeluaran IL-6, yang merangsang fibroblas stroma untuk menghasilkan sitokin CCL20 melalui laluan isyarat CCAAT/enhancer-binding protein (C/EBP), yang seterusnya berkaitan dengan peningkatan tumor. pengambilan CD4/IL17/CCR6 serta sel pro-tumorigenik Th17 [41,101]. Selain itu, model in vivo dan in vitro menunjukkan bahawa oncoprotein HPV E7 merendahkan ekspresi CXCL14 dengan hipermetilasi promoter CXCL14. Dengan cara ini, ekspresi paksa chemokine ini dalam CC mempercepatkan penghijrahan sel NK, CD4 ditambah T-sel, dan CD8 ditambah T-sel ke persekitaran setempat [111,112]. Begitu juga, ekspresi rendah XCR1 dalam DC telah terbukti penting kerana ia mengurangkan penghijrahan langsung CD8 ditambah sel T dengan interaksi chemokine Ligand CXCL1, serta pengaktifannya sendiri dan sel NK [113,114]. Tambahan pula, secara in vitro, pembelahan ligan reseptor chemokine CXCL9, CXCL10 dan CXCL11 oleh protein metallopeptidase matriks 9 (MMP-9) membawa kepada pengurangan penghijrahan sel T; dalam persetujuan dengan penemuan sebelumnya, perencatan MMP9 menunjukkan peningkatan ekspresi CXCL10, IL-12p70 dan IL18 [115].
Sesetengah kajian telah menunjukkan bahawa perubahan mungkin berbeza mengikut subtipe histologi CC. Oleh itu, penghijrahan sel-T dalam ADC adalah lebih rendah daripada di SCC; ciri tunggal ini telah dikaitkan dengan ekspresi rendah CXCL9, CXCL10, dan CXCL11 dalam ADC berbanding dengan SCC dan dipercayai bahawa ini mungkin dikaitkan dengan kehadiran lebih besar jenis 1 DC konvensional (cDC1) dalam SCC berbanding dalam ADC, yang dikaitkan dengan pengeluaran sitokin yang lebih tinggi yang merangsang penghijrahan CD8 ditambah T-sel sitotoksik ke tumor [110]. Di samping itu, ekspresi rendah CCL4 dan -Catenin didapati, serta korelasi positif antara tahapnya dan cDC1 yang menyusup tumor [110]. Oleh itu, kebolehubahan profil chemoattraction sitokin sel T sebahagiannya dapat menjelaskan heterogeniti yang diperhatikan dalam kecacatan penghijrahan sel imun dalam CC.
2.5. Penyusupan Sel Imun ke dalam Tumor (Langkah 5)
Selepas disiapkan dan diaktifkan, sel-T menyusup ke tisu tumor (Langkah 5). Dalam langkah ini, sel T CD4 ditambah Th17 dan sel T Foxp3 ditambah mempunyai kadar penyusupan yang lebih tinggi daripada yang terdapat dalam tisu biasa. Adalah dipercayai bahawa kedua-dua subtipe sel ini menyumbang kepada perkembangan tumor, melalui peningkatan dalam IL-6, IL-10, dan transforming growth factor (TGF- ) [101,116]. Selain itu, satu kajian imunohistokimia telah menyiasat hubungan antara tahap STING, CD103 ditambah penyusupan sel T, dan prognosis kanser serviks. Kajian ini mendapati gabungan tahap STING yang tinggi dan penyusupan sel T CD103 yang tinggi adalah cara untuk mencapai prognosis yang lebih baik dalam kanser serviks. Walau bagaimanapun, perlu diingatkan bahawa penyelidikan tambahan diperlukan untuk memahami sepenuhnya mekanisme yang mendasari persatuan ini dan menentukan potensi tepat STING dan CD103 ditambah penyusupan sel T, sebagai sasaran terapeutik dalam kanser serviks [117]. Tambahan pula, bukti menyokong pandangan bahawa perubahan dalam matriks ekstraselular yang dihasilkan oleh perkembangan dan perkembangan sel tumor memainkan peranan penting dalam mengawal penyusupan sel imun. Oleh itu, sebagai contoh, sel tumor merangsang sintesis komponen matriks oleh fibroblas, dengan mewujudkan struktur yang lebih padat yang menghalang penyusupan sel imun seperti CD8 plus Tcells [118]. Antara bukti mekanisme yang memudahkan peningkatan dalam pertumbuhan tumor dan metastasis dengan pengurangan penyusupan sel T ialah pembentukan semula matriks ekstraselular dan rangsangan melalui faktor pertumbuhan dan sitokin [115,119].
Oleh itu, terdapat peningkatan pengeluaran protein matriks ekstraselular seperti fibronektin 1 (FN1), MMP1, dan MMP9 dalam keadaan keradangan dan tumor kronik serviks [51,119-122]. Selain itu, penulis mengesan korelasi positif antara tahap ekspresi mereka dan peningkatan dalam proses keradangan kronik, perkembangan klinikal, pencerobohan, dan metastasis tumor [119,120,122]. Atas sebab ini, penggunaan gabungan MMP9 dengan penanda tumor lain seperti CA-125 telah disyorkan untuk diagnosis CC [121]. Kajian in vitro dengan SiHa, HeLa dan C{13}}sel A telah dijalankan untuk menganalisis penghijrahan sel-sel ini dan didapati bahawa asid fenil-laktik (PLA) sering dihasilkan oleh mikrobiota lactobacilli meningkatkan penghijrahan sel dan ekspresi MMP9 [123,124]. Adalah dicadangkan bahawa perlu ada peningkatan dalam translokasi nuklear faktor IκB dan p65 oleh rangsangan PLA dengan mengaktifkan laluan isyarat NF-kB [124]. Antara mekanisme yang dicadangkan dalam pengawalan ekspresi MMP9 ialah peningkatan dalam pengeluaran IL-6 oleh sel tumor kanser serviks [95]
Proses neovaskularisasi yang tidak normal dalam kanser serviks menunjukkan bahawa ia bukan sahaja berkaitan dengan bekalan darah sel tumor; ia juga menyumbang kepada mewujudkan persekitaran imunosupresif tumor. Ini kerana angiogenesis berlaku dengan cara yang tidak normal dan membawa kepada pembezaan sel imunosupresif dan pengurangan kapasiti penyusupan dan fungsi sel imun sitotoksik [125]. Apabila teknik imunohistokimia digunakan dalam karsinoma sel skuamosa serviks, faktor boleh aruh hipoksia-1 (HIF-1 ) adalah (a) didapati dikawal, (b) membawa kepada prognosis yang lebih teruk [126], dan (c) dikenal pasti sebagai protein yang mungkin terlibat dalam proses ini. Adalah dipercayai bahawa hipoksia yang dihasilkan oleh persekitaran mikro tumor merangsang ekspresi HIF-1 dan faktor pertumbuhan endothelial vaskular (VEGF) sambil menyebabkan angiogenesis yang tidak normal dan mengubah ekspresi beberapa molekul lekatan antara sel (ICAM) dan lekatan sel vaskular. molekul (VCAM) [127].
Apabila garis keturunan sel kanser serviks yang berbeza yang dijangkiti dengan jenis HPV yang berbeza dibandingkan, adalah diperhatikan bahawa bergantung kepada keturunan, terdapat perbezaan dalam penyusupan sel imun. Sebagai contoh, dalam vivo dan menggunakan tikus bogel dan model RAG1−/−, sel SiHa (HPV16 plus ) dan Hela (HPV18 plus ) menunjukkan penyusupan sel radang yang lebih besar daripada sel C33A (HPV−) [128]. Selain itu, tahap tinggi faktor perencatan migrasi makrofaj (MIF) dan CCL5 diperhatikan dalam semua sel; walau bagaimanapun, hanya sel SiHa dan HeLa mengecilkan ekspresi ICAM, dan perencat pengaktif plasminogen-1 (PAI-1) telah dikawal oleh sel C33A dan dikurangkan oleh sel SiHa dan HeLa [128]. Oleh itu, adalah disyorkan bahawa pelbagai jenis HPV yang menjangkiti serviks secara kronik juga perlu diambil kira, dengan objektif untuk menjelaskan perbezaan yang diperhatikan dalam penyusupan sel imun dalam tumor kanser serviks.
2.6. Pengiktirafan Sel Tumor oleh Sel Imun (Langkah 6)
Selepas itu, sel-T menyusup ke tisu tumor, dan ini sepatutnya membolehkan mereka mengenali sel-sel kanser. Walau bagaimanapun, terdapat bukti sel tumor kanser serviks dengan penurunan regulasi beberapa gen MHC, yang mengakibatkan pengurangan pengiktirafan sel tumor oleh sel T sitotoksik dan sel NK [129,130]. Antara gen MHC-I yang dikurangkan yang telah ditemui dalam kanser serviks ialah antigen leukosit manusia (HLA) A, HLAB, HLA-C, HLA-E, dan HLA g [131]. Bukti kanser kepala dan leher telah disediakan untuk mengenal pasti mekanisme downregulation yang terlibat, serta downregulation ekspresi CXCL14 yang disebabkan oleh jangkitan kronik HPV dan oleh itu downregulation gen MHC-I [112]. Adalah dipercayai bahawa ini mungkin berlaku dengan cara yang sama dalam kanser serviks [112]. Oleh itu, ujian in vivo dan in vitro telah dijalankan untuk memberikan bukti bahawa circEYA1 RNA bulat dikurangkan dalam adenokarsinoma serviks dan mempunyai kapasiti untuk menangkap miR-582-3p upregulating CXCL14 [132]. Di samping itu, kajian metilom, menggunakan keratinosit yang diabadikan, mendapati bahawa unsur promoter distal (CGI) gen HLA-E menunjukkan hipermetilasi oleh onkoprotein E7 HPV dan dikaitkan dengan downregulation [131]. Walau bagaimanapun, adalah perlu untuk menjalankan lebih banyak kajian epigenetik dengan tujuan untuk memahami mekanisme khusus pengiktirafan imunologi sel tumor oleh sel T.
Gen kompleks MHC-II juga telah menjadi sasaran perubahan dalam ekspresi mereka. Oleh itu, model in vivo, menggunakan tikus K14.E7, menunjukkan penurunan regulasi MHC-II dalam LC epidermis yang menyusup, dan peningkatan regulasi gen yang dikaitkan dengan tindak balas imun yang berkurangan, seperti Indoelamina-2-3-dioxygenase (IDO) 1, Arginase 1, IL-12/23p40 dan IL-6 [106]. Tambahan pula, didapati dalam kanser serviks bahawa sel-sel Foxp3 plus Treg, in vitro upregulasi E3 ubiquitin ligase yang berkaitan dengan membran RING-CH (MAC) 1, dan E3 ubiquitin ligase. Protein ini merendahkan CD86 dan MHC-II DC, yang dimediasi oleh IL-10 yang dihasilkan oleh sel Foxp3 plus Treg [103]. Protein yang terdapat dalam matriks ekstraselular juga kelihatan memainkan peranan penting dalam mekanisme pengecaman sel tumor. Berdasarkan ini, bukti didapati bahawa protein galectin (Gal) 3 menghalang interaksi antara reseptor TCR dan CD8, menyebabkan ketidakaktifan dan mendorong aktiviti imunosupresif [133]. Oleh itu, pengiktirafan sel tumor oleh sel imun boleh diubah secara global dan bukan sahaja oleh laluan kompleks MHC-I.
2.7. Pemusnahan Sel Tumor (Langkah 7)
Akhirnya, selepas sel-sel tumor telah diiktiraf oleh sel-T, mekanisme yang membawa kepada pemusnahan sel tumor harus dicetuskan (Langkah 7). Tanda-tanda kecacatan yang didedahkan pada peringkat ini termasuk regulasi molekul perencatan bersama seperti ligan stimulator bersama sel T (ICOSLG), CD276, perencat pengaktifan sel T (VTCN) yang mengandungi domain set-V, dan ligan protein kematian sel yang diprogramkan (PD-L), yang telah ditunjukkan sebagai salah satu mekanisme perencatan utama tindak balas imun antitumor [134,135]. Dalam kanser serviks yang berkaitan dengan HPV, ekspresi PD-L1 dan interferon-inducible 16 reseptor (IFI16) yang tinggi telah diperhatikan, dan ungkapan ini telah dikaitkan dengan perkembangan tumor. Tambahan pula, telah ditunjukkan bahawa IFI16 boleh merangsang ekspresi PD-L1 melalui laluan STING-TBK1-NF-kB [136].
Kajian yang dijalankan baru-baru ini mendedahkan bahawa sel-T daripada pesakit kanser serviks memaparkan ekspresi PD yang tinggi-1, yang membawa kepada pengeluaran TGF- dan IL-10 yang lebih besar, penurunan tahap IFN- dan terjejas. Proliferasi sel T, dengan itu mewujudkan toleransi imunologi dan memudahkan pertumbuhan tumor [135,137]. Dalam menyokong ini, ujian in vitro menunjukkan bahawa perencatan ekspresi PD-L1 dalam sel CaSki dikaitkan dengan peningkatan percambahan dan aktiviti sitotoksik CD8 ditambah T-sel [138,139]. Selain itu, serta tahap ekspresi PD-1 yang tinggi, CD8 serta sel-T yang menyusup dalam karsinoma sel skuamosa mempunyai profil 'keletihan' yang lebih tinggi dan regulasi imunoglobulin sel T dan yang mengandungi domain mucin (TIM) 3 dan gen pengaktifan limfosit (LAG) 3 [110]. Telah didapati dalam ujian in vitro bahawa protein E2 HPV berisiko tinggi menurunkan STING, sensor sistem tindak balas imun semula jadi tumor yang membantu dalam pengeluaran IFN jenis I [139].
Perubahan tepat dalam fungsi STING dalam CC berkaitan HPV masih belum dijelaskan sepenuhnya. Walau bagaimanapun, kajian in vitro telah menunjukkan bahawa protein HPV16 E7 boleh berinteraksi dengan NLRX1 dan meningkatkan pusing ganti sensor STING, yang membawa kepada pengurangan dalam tindak balas interferon dan perkembangan dan perkembangan karsinoma sel skuamosa kepala dan leher (HNSCC). Interaksi antara protein HPV16 E7, NLRX1, dan STING yang terdapat dalam HNSCC mungkin mencadangkan bahawa terdapat mekanisme pengawalseliaan yang sama untuk sistem tindak balas imun hos dalam CC [140]. Di samping itu, dilaporkan bahawa protein HPV E7 mungkin menindas ekspresi STING melalui mekanisme epigenetik [141]. Akibatnya, telah dicadangkan bahawa laluan isyarat STING boleh bertindak sebagai pengawal penting CIC, bukan sahaja dengan memainkan peranan dalam memusnahkan sel tumor tetapi juga mengaktifkan DC, meningkatkan persembahan antigen, mengaktifkan, dan membezakan pertumbuhan T. -sel, merangsang penyusupan limfosit T sitotoksik (CTL) dan menghalang penyusupan sel T pengawalseliaan yang menindas imun [20].
Berkenaan dengan sitotoksisiti sel T CD8 ditambah, penurunan ekspresi E-cadherin didapati dan ini berkaitan dengan prognosis yang lebih teruk dalam kanser serviks [142,143]. E-cadherin telah terbukti penting untuk polarisasi dan pembebasan granul sitotoksik yang digunakan oleh CD8 ditambah sel T sitotoksik untuk membunuh sel tumor, yang dirangsang oleh interaksi antara integrin E (CD103) sel T yang menyusup tumor dan E-cadherin sel tumor [144-148].
Pengaruh beberapa metabolit dalam tindak balas imun selular juga telah dikaji. Oleh itu, korelasi positif telah ditemui antara kepekatan metabolit tryptophan yang dihasilkan oleh sel-sel kanser dan perkembangan tumor dan metastasis nodus limfa dalam karsinoma sel skuamosa serviks [149]. Antara metabolit yang dikaji ialah quinurenine, manakala nisbah quinunerin/tryptophan telah meningkat dalam kanser serviks [150]. Kajian in vitro menggunakan garis keturunan kanser serviks yang berbeza menunjukkan peningkatan regulasi enzim yang merendahkan tryptophan IDO1; walau bagaimanapun, downregulation in vitro tidak menunjukkan perbezaan dalam pertumbuhan sel tumor [151]. Walau bagaimanapun, kajian menggunakan model tikus BALB/c bogel dan K14.E7 (mengekspresikan gen E7 HPV) dalam vivo menunjukkan bahawa downregulation IDO1 secara signifikan dikaitkan dengan peningkatan bilangan sel NK yang menyusup dan penurunan pertumbuhan tumor [151,152]. Mekanisme yang terlibat dalam model tikus K14.E7 telah dikenal pasti dengan menyatakan bahawa pengawalseliaan IDO1 dikaitkan dengan rembesan tempatan IFN dan penindasan CD8 ditambah T-sel [152].
Pada peringkat ini, pengawalan tindak balas imun oleh CD4 ditambah sel T juga nampaknya sangat penting. Bukti menunjukkan terdapat insiden kanser serviks yang lebih tinggi pada pesakit dengan imunosupresi oleh jangkitan virus immunodeficiency manusia (HIV) [153,154]. Telah diperhatikan bahawa peningkatan bilangan beredar CD4 ditambah NKG2D ditambah T-sel dan ekspresi rendah reseptor kostimulasi CD28 dalam pesakit kanser serviks dikaitkan dengan kekerapan penanda sitotoksik yang berkurangan dan pengurangan pengeluaran sitokin proinflamasi [155]. Selain itu, terdapat bukti bahawa protein galectin-1 (Gal-1) mendorong pelepasan CD4 ditambah sel Th17 dan Th1 serta mendorong pembiakan sel Tregs [133].
Interaksi antara subtipe sel imun yang berbeza juga boleh mempengaruhi pemusnahan sel tumor. Sehubungan itu, model kajian in vitro menunjukkan bahawa LC kanser serviks yang dirangsang dengan s-Poly-I:C mempunyai peningkatan ekspresi penanda kematangan sel (CD40, CD80, CD83, CD86, CCR7, MHC1 dan MHCII), penghijrahan yang lebih baik dan peningkatan pengeluaran sitokin pro-radang yang berkaitan dengan rangsangan [tindak balas sitotoksik pengantara sel CD8 tambah sel (IL-1beta, IL-6, IL-12p70, IP-10, TNF-alpha, IFNalfa, MCP-1, MIP-1alfa, MIP-1beta dan RANTES) [99]. Walau bagaimanapun, eksperimen in vivo menggunakan tikus telah mendapati bahawa pengurangan LC meningkatkan aktiviti sitotoksik sel T [109]. Dalam tahun-tahun kebelakangan ini, telah diperhatikan bahawa CD4 ditambah T-sel boleh dibezakan menjadi subtipe dengan fungsi yang tidak jelas atau kontroversi, seperti sel Th17 [156,157]. Kajian yang menganalisis kanser serviks secara keseluruhan mendapati bahawa kehadiran sel Th17 dikaitkan dengan prognosis yang baik [158]. Walau bagaimanapun, analisis yang melibatkan hanya ADC menunjukkan bahawa dominasi sel Th17 mendorong perkembangan tumor [159]. Baru-baru ini, bilangan PU.1 tambah T-sel yang lebih tinggi telah ditemui dalam kanser serviks jika dibandingkan dengan tisu serviks biasa, tetapi fungsinya masih tidak diketahui [160]. Sehingga kini, apabila model in vivo telah digunakan dengan tikus CH3, sel-sel ini telah terbukti mempunyai fungsi perencatan yang berkesan ke atas pertumbuhan karsinoma sel skuamosa mulut, dan apoptosis teraruh dengan merangsang pengeluaran IL-9 dalam sel tumor [ 161]. Walau bagaimanapun, ia masih perlu untuk menjelaskan fungsi mereka dalam kanser serviks.
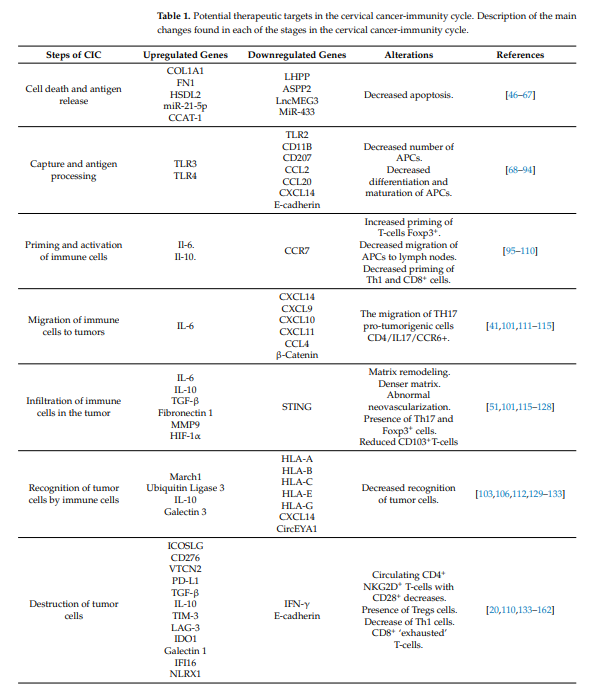
Antara mekanisme lain yang dikaji berkaitan dengan membunuh sel tumor ialah metabolisme spesies oksigen reaktif. Oleh itu, dalam SCC, terdapat bukti peningkatan regulasi gen dwi oxygenase 1 (DUOX1), dwi oxygenase 2 (DUOX2), dan NADPH oxidase 2 (NOX2). Perkaitan telah ditemui dengan peningkatan kelangsungan hidup bebas penyakit, mungkin melalui mekanisme yang melibatkan interferon gamma (IFN-), pengeluaran interferon alpha (IFN-), dan pengaktifan laluan isyarat sel NK [162]. Jadual 1 menunjukkan setiap langkah CIC dan perubahannya untuk sasaran yang tidak dikawal dalam kanser serviks.
3. Imunoterapi Bersasaran CIC dalam Kanser Serviks
3.1. Vaksin DNA
Berdasarkan perubahan yang ditemui dalam pembebasan antigen (Fasa 1), terdapat kajian alternatif untuk memperkenalkan molekul berbeza yang boleh mengaktifkan tindak balas imun. Antaranya, terdapat vaksin berasaskan epitope terapeutik; bagaimanapun, kemustahilan peptida kecil menghasilkan tindak balas imun yang kuat mewakili cabaran untuk pembangunan jenis vaksin ini [163]. Oleh itu, beberapa kajian telah menggunakan epitop HPV E6 dan E7 yang dikaitkan dengan adjuvant, tetapi hasilnya masih dalam peringkat awal [164]. Imunisasi genetik telah didokumenkan sebagai strategi yang berkesan untuk induksi imuniti humoral dan selular dalam sejumlah besar model haiwan [165,166]. Walau bagaimanapun, beberapa kajian menunjukkan imunogenik yang rendah, yang boleh dijelaskan dengan pengenalan bahan genetik dalam sel tidak spesifik, dan oleh ketidakupayaannya untuk mereplikasi atau merebak melalui sel jiran dalam vivo [167,168]. Oleh itu, terdapat banyak kajian penyelidikan yang direka untuk mempotensikan vaksin terapeutik DNA, seperti pengoptimuman sistem penghantaran DNA ke sel, melalui cara fizikal (elektroporasi, balistik bio, tatu, dll.) dan kaedah kimia (liposom, nanopartikel, kationik). peptida, dsb.) [169–175]. Percubaan telah dibuat untuk memperbaiki jujukan gen itu sendiri: penyesuaian kodon untuk ekspresi dalam mamalia [176]; gabungan dengan protein lain yang memihak kepada antigen vaksin yang ada [177-179]; dan penggabungan molekul stimulasi bersama seperti sitokin dan kemokin [180–182]. Walau bagaimanapun, keputusan vaksin ini masih tidak mencukupi untuk membolehkan ia digunakan sebagai rawatan dan ia kekal dalam fasa kajian pra-klinikal [171].
3.2. Vaksin Berasaskan DC
Hasil daripada perubahan yang dikenal pasti dalam pembentangan antigen (Langkah 2 dan 3), vaksin terapeutik menggunakan DC telah muncul sebagai pilihan rawatan yang menjanjikan dalam beberapa tahun kebelakangan ini [183]. Penggunaan DC untuk pembangunan vaksin terapeutik terhadap kanser adalah berdasarkan kapasiti mereka untuk membentangkan antigen dan mendorong tindak balas imun yang berkesan, melalui penyebuan dan rangsangan percambahan dan pengaktifan sel T [184]. Pada masa ini, eksperimen dengan vaksin terapeutik terhadap kanser berdasarkan DC melibatkan pendedahan mereka kepada antigen HPV, jenis protein antigen lain, peptida atau lisat tumor ex vivo, jangkitan atau pemindahan DC dengan pengekodan DNA atau RNA antigen HPV, dan penghantaran DC seterusnya. kepada pesakit [183,185-187]. Beberapa kajian telah terbukti berkesan dalam merawat kanser serviks pada peringkat praklinikal.
Sebagai contoh, DC berdenyut dengan protein gabungan, yang dibentuk oleh peptida berfungsi Mycobacterium tuberculosis protein kejutan haba (MTBHsp70) yang bersatu dengan domain ekstraselular reseptor peptida formyl 1 (FPR1), menunjukkan peningkatan kematangan DC, serta keupayaan untuk meningkatkan IL-12p70, IL-1 , pengeluaran TNF, dan meningkatkan kesan sitotoksik sel T sitotoksik (CTL) dalam tikus [187]. Malah, dalam kajian baru-baru ini, eksosom terbitan DC yang dimuatkan dengan peptida E7 dan poli (I: C) telah digunakan, dalam model in vitro dan in vivo, yang mendorong penjanaan dan percambahan sel-sel T CD8 plus sitotoksik, bersama-sama dengan peningkatan dalam rembesan IL-2 dan IFN- dan pengurangan dalam pelepasan IL-10 [186]. Selain itu, kajian in vitro, menggunakan gabungan biologi RIX-2 (dibentuk oleh: IL-1 , IL-2, IL-6, IL-8, TNF , GM-CSF, dan IFN ) dalam sel LC, telah menunjukkan penyelarasan penanda pematangan, peningkatan pengeluaran IL-12p70, CXCL10 dan CCL2, peningkatan ekspresi CCR7 dan penghijrahan sel, serta percambahan dan pengaktifan yang dipertingkatkan. daripada sitotoksik CD8 ditambah T-sel [188]. Walau bagaimanapun, beberapa isu serius perlu dijelaskan untuk meningkatkan keberkesanan vaksin ini dan menambah baik penyusupan dan pengekalan sel T effector, termasuk pengenalpastian reseptor membran dan pengaktif DC, dan penentuan subjenis tertentu DC yang mungkin terlibat dalam proses ini untuk rangsangan dan pengaktifan sel T yang berkesan [189].
3.3. Vaksin Berasaskan Sel T
Perubahan yang diperhatikan dalam Langkah 4 hingga 7 CIC telah menimbulkan strategi terapeutik yang tertumpu pada peningkatan fungsi sel T. Oleh itu, terdapat bukti bahawa E6 dan E7 HPV epitope spesifik CD4 plus dan CD8 plus T-sel boleh dihasilkan secara in vitro, menggunakan limfosit yang diekstrak daripada nodus limfa pesakit kanser serviks [190]. Selain itu, ujian klinikal fasa II pada pesakit dengan kanser serviks metastatik, menggunakan infusi sel T yang dirawat ex vivo dan dipilih sebagai reaktif terhadap E6 dan E7; ia diperhatikan dalam beberapa kes bahawa terdapat regresi lengkap atau separa kanser [191]. Walau bagaimanapun, pada masa ini, kadar keberkesanan kira-kira 30 peratus telah direkodkan, bersama-sama dengan perkembangan rintangan terapeutik [191-193]. Di samping itu, tindak balas berubah terhadap bentuk rawatan ini boleh dijelaskan oleh kebolehubahan genetik individu dan kepelbagaian sel kanser. Dalam menyokong ini, mutasi diperhatikan dalam interferon gamma 1 dan reseptor HLAA [194]. Selain itu, terdapat bukti bahawa kereaktifan sel T terhadap tumor kanser serviks yang dijangkiti HPV16- adalah berbeza daripada kereaktifan yang diperhatikan dalam18-tumor yang dijangkiti HPV [195]. Oleh itu, sebelum ia boleh digunakan untuk meningkatkan keberkesanan rawatan ini, reka bentuk terapi jenis ini memerlukan kajian yang lebih mendalam tentang genetik setiap individu dan ciri-ciri tumor sebelum memberikan rawatan ex vivo kepada sel-T.
3.4. Terapi Berasaskan RNA Bukan Pengekodan
Kajian tentang rintangan terhadap imunoterapi telah mendapati bahawa RNA bukan pengekodan boleh memodulasi proses ini [196]. Antara mikroRNA yang dikaji dalam kanser serviks, didapati bahawa ekspresi PD-L1 boleh dikurangkan dengan rangsangan dengan miR140/142/340/383 dan penindasan miR-18a [197]. Strategi ini sangat bernilai kerana penggunaan antibodi anti-PD-1/PD-L1 dalam ujian klinikal fasa I dan fasa II dalam kanser serviks menunjukkan keberkesanan dan ketahanan yang rendah terhadap rawatan [198,199]. Satu lagi kajian menunjukkan bahawa pentadbiran miR-34a dan sPD-1, menggunakan gelembung mikro lipid kationik subkutan pada tikus, membawa kepada peningkatan pengeluaran IFN yang dikaitkan dengan peningkatan tindak balas imun antitumor [200]. Baru-baru ini, kajian praklinikal lain tentang kanser serviks telah mengesyorkan mendorong ekspresi E-cadherin dengan merangsang ekspresi miR-185-5p [201], menggunakan miR-126 untuk induksi sitotoksisiti yang dimediasi oleh TNF- dan FasL [ 202] dan menggunakan lncRNA HOX (HOTAIR—antisense transkrip RNA HOX bukan pengekodan panjang), yang bertindak secara kompetitif terhadap miR-148a dan telah menunjukkan keupayaan untuk mengambil bahagian dalam pengawalan ekspresi HLA-G [203]. Walau bagaimanapun, bukti menunjukkan bahawa strategi ini masih perlu diperbaiki.
3.5. Penyuntingan Gen CRISPR/Cas9
Alat baharu untuk mengetepikan ekspresi onkoprotein HPV, E6 dan E7, ialah alat penyunting gen CRISPR/Cas9. Inturi dan Jemth [204] menunjukkan bahawa kalah mati oncoprotein ini oleh CRISPR/Cas9 membolehkan kedua-dua laluan isyarat p53/p21 dan pRb/p21 dipulihkan, yang menyebabkan penuaan dalam sel-sel ini. Berkenaan dengan keupayaan sistem CRISPR/Cas untuk menghalang pertumbuhan sel tumor serviks dalam tikus bogel, diperhatikan bahawa jumlah tumor adalah jauh lebih kecil pada tetikus yang mengalami pembelahan mRNA E6/E7 oleh sistem CRISPR/Cas berbanding dengan kumpulan kawalan [205,206]. Satu lagi kajian menunjukkan bahawa gangguan onkogen HPV oleh CRISPR/Cas9 dalam karsinoma sel skuamosa oropharyngeal positif HPV (OPSCC) menghasilkan pemulihan laluan cGAS-STING. Keputusan ini memberikan pandangan baharu tentang rawatan yang diperlukan untuk menyasarkan jangkitan HPV, serta kanser serviks, memandangkan STING telah dianggap sebagai sasaran imunoterapi baharu yang berpotensi untuk kanser serviks [207,208].
Dalam kajian baru-baru ini yang menggunakan tikus SCID bermanusia yang dicantumkan sel SiHa, penyekatan laluan PD-1 melalui CRISPR/Cas9 telah dianalisis bersama-sama dengan kalah mati onkogen HPV. Keputusan menunjukkan bahawa fungsi limfosit telah dipulihkan dengan peningkatan bilangan CD8 plus dan CD4 plus T-sel, serta sel dendritik [209]. Selain itu, kajian oleh Zhen dan rakan sekerja [210] menunjukkan bahawa penghantaran liposom CRISPR/cas9, secara in vivo, boleh menghapuskan HPV, yang mengakibatkan peningkatan bilangan sel T CD8 dan ekspresi sitokin pro-radang. Pengurangan dalam bilangan sel T reg dan sel penindas myeloid juga diperhatikan.
Bentuk penyampaian inovatif sistem CRISPR/Cas mewakili kemajuan yang besar kerana ia membolehkan pendekatan klinikal baharu diguna pakai untuk rawatan HPV dan karsinoma serviks, dan keberkesanannya telah terbukti luar biasa dalam vivo dan in vitro. Penghantaran komponen CRISPR/Cas, yang disuntik secara intratumoral, menunjukkan pengurangan ketara dalam kadar pertumbuhan tumor dan tumor, serta memelihara struktur bersebelahan dan memastikan bahawa teknologi mempunyai keadaan keselamatan yang baik untuk sel normal. Penghantaran sistemik CRISPR/Cas juga telah direkodkan dalam literatur dan telah membuka aplikasi terapeutik baharu dan berpotensi yang tidak terhad kepada tapak aplikasi [211].
4. Kesimpulan
Berdasarkan hasil kajian yang dinyatakan di atas, jelas, tahap kerumitan yang tinggi terlibat semasa mengkaji tindak balas imun antitumor kerana terdapat beberapa penyelewengan dalam semua fasa tindak balas imun adaptif selular terhadap kanser serviks [212]. Begitu juga, sel CD8 plus T sitotoksik memainkan peranan penting dalam memusnahkan sel tumor. Walau bagaimanapun, bukti menunjukkan bahawa ini sahaja tidak mencukupi untuk mencapai tindak balas imun antitumor yang cekap. Oleh itu, adalah perlu untuk mengkaji kajian bersama-sama dengan jenis sel lain yang terlibat dalam CIC. Sebagai contoh, fungsi subjenis APC yang berbeza boleh mempengaruhi kedua-dua penyebuan dan pengaktifan sel-T, serta kapasiti penghijrahan dan efektornya. Fungsi imunosupresif sel Treg juga perlu diambil kira kerana terdapat interaksi yang berterusan dan dinamik antara pelbagai jenis sel imun dan sel tumor. Selain itu, kerana banyak kajian menjalankan analisis kanser serviks secara holistik, terdapat beberapa keputusan yang bercanggah antara subtipe kanser serviks seperti ADC dan SCC. Oleh itu, pemisahan kajian mengikut subtipe histologi mereka boleh membantu untuk menjelaskan mekanisme yang terlibat dalam tindak balas imun dengan cara yang lebih berkesan.
Pada masa ini, strategi yang digunakan untuk memerangi perubahan ini tidak cukup berkesan dan hanya sekumpulan kecil pesakit yang mendapat manfaat [196,213]. Ini mungkin disebabkan oleh fakta bahawa kebanyakan sasaran terapeutik yang dikenal pasti adalah hasil analisis reduksionis yang telah menyumbang secara signifikan kepada pemahaman yang lebih baik tentang mekanisme tindak balas imun. Namun begitu, tindak balas imun sangat bersepadu dan memerlukan terapi yang mencapai pelbagai sasaran, sambil menghalang mekanisme pampasan daripada menjana ketahanan terhadap rawatan. Begitu juga, pendekatan terapeutik masa depan harus mempunyai pandangan yang lebih peribadi. Sebagai contoh, perbezaan dalam tindak balas imun terhadap kanser serviks yang disebabkan oleh pembolehubah seperti subtipe histologi, strain HPV, umur dan peringkat klinikal perlu diterokai dengan lebih lanjut.
Sumbangan Pengarang:
Pengkonsepan, JPA dan ECC; carian literatur, JPA dan ECC; penulisan—penyediaan draf asal, JPA; menulis—menyemak dan menyunting, BMC dan ECC; penyeliaan, ECC dan BMC Semua pengarang telah membaca dan bersetuju dengan versi manuskrip yang diterbitkan.
Pembiayaan:
Kajian ini dibiayai sebahagiannya oleh Coordenação de Aperfeiçoamento de Pessoal de Nível Superior—Brasil (CAPES)—Kod Kewangan 001.
Konflik Kepentingan:
Penulis mengisytiharkan bahawa mereka tidak mempunyai kepentingan bersaing.
Rujukan
Sung, H.; Ferlay, J.; Siegel, RL; Laversanne, M.; Soerjomataram, I.; Jemal, A.; Bray, F. Statistik Kanser Global 2020: Anggaran GLOBOCAN Insiden dan Kematian Seluruh Dunia untuk 36 Kanser di 185 Negara. CA Kanser J. Clin. 2021, 71, 209–249. [CrossRef]
2. Stelzle, D.; Tanaka, LF; Lee, KK; Ibrahim Khalil, A.; Baussano, I.; Shah, ASV; McAllister, DA; Gottlieb, SL; Klug, SJ; Winkler, AS; et al. Anggaran beban global kanser serviks yang dikaitkan dengan HIV. Lancet Glob. Kesihatan 2021, 9, e161–e169. [CrossRef]
3. Bhatla, N.; Aoki, D.; Sharma, DN; Sankaranarayanan, R. Kanser serviks uteri: kemas kini 2021. Int. J. Gynecol. Obstet. 2021, 155 (Bekalan S1), 28–44. [CrossRef]
4. Wiemann, B.; Starnes, toksin CO Coley, faktor nekrosis tumor dan penyelidikan kanser: Perspektif sejarah. Pharmacol. Di sana. 1994, 64, 529–564. [CrossRef] [PubMed]
5. McCarthy, EF Toksin William B. Coley dan rawatan sarkoma tulang dan tisu lembut. Iowa Orthop. J. 2006, 26, 154–158.
6. Guo, ZS Hadiah Nobel dalam bidang perubatan 2018 diberikan kepada imunoterapi kanser. Kanser BMC 2018, 18, 1086. [CrossRef]
7. Perintis Imunoterapi Kanser Menangkan Nobel Perubatan. Tersedia dalam talian: https://www.science.org/content/article/cancerimmunotherapy-pioneers-win-medicine-nobel (diakses pada 16 Disember 2022).
8. Farhood, B.; Najafi, M.; Mortezaee, K. CD8 ditambah limfosit T sitotoksik dalam imunoterapi kanser: Kajian semula. J. Sel. Fisiol. 2019, 234, 8509–8521. [CrossRef] [PubMed]
9. Maskey, N.; Maskey, N.; Thapa, N.; Thapa, N.; Maharjan, M.; Maharjan, M.; Shrestha, G.; Shrestha, G.; Maharjan, N.; Maharjan, N.; et al. Menyusup limfosit CD4 dan CD8 dalam lingkungan serviks rahim yang dijangkiti HPV. Cancer Manag. Res. 2019, 11, 7647–7655. [CrossRef] [PubMed]
10. Borst, J.; Ahrends, T.; B ˛abała, N.; Melief, CJM; Kastenmüller, W. CD4 ditambah sel T membantu dalam imunologi kanser dan imunoterapi. Nat. Rev. Immunol. 2018, 18, 635–647. [CrossRef]
11. Najafi, M.; Farhood, B.; Mortezaee, K. Sumbangan sel T pengawalseliaan kepada kanser: Kajian semula. J. Sel. Fisiol. 2018, 234, 7983–7993. [CrossRef]
12. Moynihan, KD; Irvine, DJ Berperanan untuk Imuniti Semula Jadi dalam Imunoterapi Gabungan. Kanser Re. 2017, 77, 5215–5221. [CrossRef] [PubMed]
13. DeMaria, O.; Cornen, S.; Daëron, M.; Morel, Y.; Medzhitov, R.; Vivier, E. Memanfaatkan imuniti semula jadi dalam terapi kanser. Alam Semula Jadi 2019, 574, 45–56. [CrossRef] [PubMed]
14. Kametani, Y.; Miyamoto, A.; Seki, T.; Ito, R.; Habu, S.; Tokuda, Y. Kepentingan model tetikus manusia untuk penilaian tindak balas imun humoral terhadap vaksin kanser. Pers. Med. Univ. 2018, 7, 13–18. [CrossRef]
15. Varn, FS; Mullins, DW; Arias-Pulido, H.; Fiering, S.; Cheng, C. Program imuniti adaptif dalam kanser payudara. Imunologi 2016, 150, 25–34. [CrossRef]
For more information:1950477648nn@gmail.com
