Potensi Vaksin Berasaskan Sel Dendritik Untuk Memodulasi Populasi Sel Limfoid Semula Jenis 3
Nov 24, 2023
Abstrak:
Vaksin sel dendritik (DC) ialah sejenis imunoterapi yang bergantung pada komunikasi DC dengan aspek lain sistem imun. DC ialah sel pembentangan antigen yang kuat yang terlibat dalam pengaktifan tindak balas imun semula jadi dan pendidikan imuniti adaptif, menjadikannya sasaran ideal untuk imunoterapi. Sel limfoid semula jadi (ILC) secara relatifnya baru dikenal pasti dalam bidang imunologi dan mempunyai peranan penting dalam kesihatan dan penyakit. Kajian yang diterangkan di sini meneroka komunikasi antara jenis 3 ILC (ILC3s) dan DC menggunakan model murine vaksin berasaskan DC. Perubahan tempatan dan sistemik dalam populasi ILC3 berikutan pemberian vaksin DC diperhatikan, dan apabila dicabar dengan sel melanoma B16F10, perubahan dalam populasi ILC3 dalam paru-paru diperhatikan. Interaksi antara DC dan ILC3 perlu diterokai lebih lanjut untuk menentukan potensi komunikasi mereka dalam kesihatan, penyakit dan pembangunan imunoterapi.

cistanche tubulosa-meningkatkan sistem imun
Kata kunci:
sel dendritik (DC); jenis 3 sel limfoid semula jadi (ILC3); bawaan; komunikasi
1. Pengenalan
Sel limfoid semula jadi (ILC) ialah kumpulan leukosit heterogen yang diperoleh daripada sel progenitor limfoid biasa yang mempunyai fungsi penting dalam pembangunan tisu, pembaikan, dan homeostasis. ILC telah dikaitkan dengan penyakit radang yang berbeza termasuk penyakit radang usus, psoriasis, asma, dan pelbagai penyakit autoimun [1]. Mereka biasanya dipisahkan kepada tiga kumpulan utama, jenis 1 (ILC1), jenis 2 (ILC2), dan jenis 3 (ILC3), berdasarkan ekspresi faktor transkripsi, profil sitokin, dan penanda fenotip tertentu [2]. Sel pembunuh semulajadi (NK) kadangkala dikelompokkan sebagai subset ILC1 kerana persamaannya; walau bagaimanapun, sel NK telah terbukti mempunyai ciri yang berbeza daripada ILC1 seperti ekspresi faktor transkripsi dan aktiviti sitolitik yang telah membezakannya sebagai subjenis ILC mereka sendiri [3]. Walau bagaimanapun, ramai yang masih menganggap sel NK sebagai subset ILC1s [4]. Disebabkan oleh profil sitokin, faktor transkripsi dan fungsi imunologi yang serupa, ILC (sel NK, ILC1s, ILC2s, dan ILC3s) dianggap sebagai rakan semula jadi kepada komponen sistem imun adaptif yang mencerminkan limfosit T sitotoksik, Th1, Th2, dan Th17. jawapan, masing-masing [4]. Walau bagaimanapun, tidak seperti sel T, mereka kekurangan reseptor khusus antigen [5].
DC adalah leukosit semula jadi yang penting dalam induksi tindak balas imun dan toleransi. Mereka mempunyai reseptor pengecaman corak yang mengenali corak molekul berkaitan patogen dan/atau kerosakan dan merupakan sel pembentangan antigen yang paling cekap [6]. Melalui pembentangan antigen dan rembesan sitokin, DC boleh menentukan nasib sel T naif dan mendorong tindak balas pro-radang atau imunosupresi. Sel T boleh dididik untuk mengenali antigen sebagai berbahaya dan menyerangnya atau sebagai tidak berbahaya dan mengambil fenotip tolerogenik [6]. DC juga terlibat dalam pengaktifan imuniti semula jadi serta pendidikan imuniti adaptif. Melalui sentuhan langsung atau penghasilan sitokin yang berbeza dan faktor larut, DC boleh mengaktifkan leukosit semula jadi lain dan menggalakkan tindak balas imun semula jadi [7].
Kuasa DC telah digunakan dalam imunoterapi seperti vaksin DC. Vaksin DC disediakan dengan mengasingkan DC daripada pesakit atau mengasingkan prekursor DC dan memperoleh DC. DC ini dimanipulasi ex vivo, yang melibatkan pematangan DC dengan cara imunogenik. DC juga dimuatkan dengan antigen tertentu, yang akan menjadi sasaran vaksin untuk membangunkan tindak balas imunogenik yang diarahkan kepada [8]. Vaksin DC ialah platform imunoterapeutik yang mengambil kesempatan daripada keupayaan DC untuk mendidik sistem imun adaptif untuk mendorong tindak balas khusus antigen, terutamanya sel T sitotoksik khusus antigen. Oleh itu, majoriti penyelidikan vaksin DC telah memberi tumpuan kepada kapasiti DC untuk mendidik sistem imun adaptif. Walau bagaimanapun, dalam beberapa tahun kebelakangan ini, hubungan antara DC dan sel NK telah ditunjukkan mempunyai pengaruh yang kuat terhadap imuniti anti-tumor yang penting untuk keberkesanan vaksinasi DC [9-11]. Ini menunjukkan keperluan penting untuk meneroka hubungan lain antara DC dan leukosit semula jadi yang berbeza dan pengaruh komunikasi ini terhadap keberkesanan vaksin DC. Oleh kerana sel NK adalah sebahagian daripada keluarga ILC dan kerana persamaan rapat ILC dengan sel T [5], objektif kajian yang dibentangkan di sini adalah untuk menyiasat potensi hubungan antara DC dan ahli keluarga ILC lain, ILC3s. Kami menggunakan platform vaksin DC (moDC) terbitan monosit di mana DC dihasilkan ex vivo daripada sel prekursor sumsum tulang murine. Vaksin MoDC adalah bentuk vaksin DC yang paling biasa kerana, mengikut sejarah, ia adalah yang paling mudah untuk dihasilkan [12].

manfaat cistanche untuk lelaki-menguatkan sistem imun
Klik di sini untuk melihat produk Cistanche Enhance Immunity
【Minta lebih lanjut】 E-mel:cindy.xue@wecistanche.com / Whats App: 0086 18599088692 / Wechat: 18599088692
ILC3 mempunyai fungsi penting dalam homeostasis usus, imuniti terhadap bakteria ekstraselular, dan perkembangan tisu limfoid [5]. ILC3 boleh dibahagikan kepada kumpulan yang berbeza dalam ekspresi penanda permukaan dan pengeluaran sitokin. Walau bagaimanapun, semua ILC3 menyatakan ROR t [13]. Satu subkumpulan ILC3 ialah ILC3-sel induser tisu limfoid yang penting dalam organogenesis [14]. ILC3 juga boleh dibahagikan berdasarkan ekspresi reseptor sitotoksisiti semulajadi (NCR), yang pada tikus adalah ekspresi NKp46 [15,16], dan pada manusia, ia adalah NKp44 [17,18]. Oleh itu, terdapat NCR+ dan NCR-ILC3 yang mempunyai perbezaan dalam kapasiti fungsian dan ciri fenotipnya. Sebagai contoh, telah dicadangkan bahawa NCR+ ILC3 menghasilkan IL-22 tetapi bukan IL-17, manakala NCR− ILC3 boleh menghasilkan kedua-dua sitokin [19]. Walau bagaimanapun, dalam kajian baru-baru ini oleh Fiancette et al., NCR+ ILC3s ditunjukkan mampu menghasilkan jumlah IL yang rendah-17 [20]. Rankin et al. ditunjukkan pada tikus bahawa NCR+ ILC3s memerlukan faktor transkripsi T-bet. Oleh itu, NCR+/− ILC3 boleh dibezakan berdasarkan ekspresi NKp46 dan T-bet. Dalam kajian yang diterangkan di sini, ILC3 murine ditakrifkan oleh keturunan−CD45+DX5−ROR t +, dengan NCR+ ILC3s juga ialah T-bet+NKp46+ dan NCR−ILC3s ialah T-bet−NKp46 − (Jadual 1 dan Lampiran A Rajah A1–A3).
Jadual 1. Subset ILC3 ditakrifkan oleh analisis sitometri aliran.

Objektif penyelidikan ini adalah untuk membantu menjelaskan jika terdapat komunikasi antara vaksin DC dan ILC3 dan potensi interaksi mereka dalam imunoterapi DC. ILC3 telah ditunjukkan mempunyai peranan dalam pelbagai penyakit dan kanser dan oleh itu mempunyai potensi dalam konteks imunoterapi yang berbeza. ILC3 adalah agak baru dalam bidang imunologi dan akibatnya, pengaruhnya terhadap penyakit dan rawatan telah diterokai secara terhad. ILC3 bertindak balas terhadap rangsangan luar, yang akan menentukan aktiviti mereka dan sama ada mereka menggalakkan perkembangan atau penindasan tumor [21,22]. Sama seperti sel Th17, ILC3 mempunyai faktor transkripsi ROR t dan menghasilkan sitokin tindak balas Th17 seperti IL-17 dan IL-22. IL-22 penting untuk mengawal jangkitan bakteria dalam usus [16]. Walau bagaimanapun, dalam model kanser kolon yang disebabkan oleh bakteria, telah ditunjukkan bahawa IL-17 dan IL-22 daripada ILC dalam kolon menyumbang kepada perkembangan kanser kolon [23]. Tambahan pula, ILC3 telah dikaitkan dengan hasil negatif dalam kanser payudara [24]. Sebaliknya, persatuan antara NCR+ ILC3s dan struktur limfoid tertier (TLS) dan hasil klinikal yang lebih baik dalam kanser paru-paru bukan sel kecil telah diperhatikan [18]. Di samping itu, kajian baru-baru ini menyiasat ILC3 dalam kanser kolorektal. Kajian itu memerhatikan peningkatan dalam ILC1 dan penurunan dalam ILC3 dalam sampel pesakit tumor kolorektal yang direseksi berbanding dengan tisu bersebelahan bukan malignan yang dipadankan. Penjujukan RNA dan pemprofilan transkrip mendedahkan ILC3 telah meningkatkan keplastikan dan kapasiti fungsi yang berbeza dalam tumor kolorektal berbanding dengan tisu bukan malignan. Menariknya, penjujukan RNA juga mencadangkan bahawa ILC3 yang menyusup tumor telah mengimbangi keplastikan untuk beralih kepada fenotip ILC1. Kajian mendapati bahawa interaksi ILC3 dengan sel T menyokong imuniti jenis I, dan dalam kanser kolorektal, interaksi ini terhad, yang menghalang tindak balas anti-tumor. Ini menyokong fungsi penting untuk ILC3 dalam imuniti anti-tumor. Secara keseluruhannya, kertas itu menunjukkan peranan penting yang dimiliki oleh ILC3 dalam pengawalan homeostasis imunologi dan kanser kolorektal [25]. Oleh itu, ILC3 dianggap mempunyai dua peranan dalam kesihatan dan penyakit. Mereka boleh menggalakkan perkembangan kanser [23,24,26] tetapi juga boleh menyumbang kepada tindak balas anti-tumor [18,25,27,28]. Fenotip dan sumbangan mereka kepada kanser nampaknya kontekstual, yang menunjukkan potensi untuk memanipulasi ILC3 melalui imunoterapi untuk mendapatkan fenotip yang membantu dengan tindak balas anti-kanser dan bukannya menyokong perkembangan tumor. Oleh itu, vaksin berasaskan DC mewakili kaedah yang mungkin untuk mempengaruhi persekitaran mikro tumor melalui manipulasi fenotip ILC dan pengeluaran sitokin mereka, yang akan membolehkan untuk menyesuaikan tindak balas imun bergantung pada keadaan dan boleh memberi manfaat dalam penyelidikan kanser.
Memandangkan terdapat penyelidikan terhad ke dalam komunikasi antara DC dan ILC3, terutamanya dalam konteks vaksinasi DC, kajian yang diterangkan di sini menyiasat perubahan dalam populasi ILC3 berikutan pemberian vaksin berasaskan DC kepada tikus. Dalam makalah ini, komunikasi antara vaksin berasaskan DC dan ILC3 telah diperhatikan, yang ditunjukkan melalui pengaruh vaksin yang berterusan terhadap tindak balas ILC3 selama sekurang-kurangnya 10 hari selepas imunisasi.

cistanche tubulosa-meningkatkan sistem imun
2. Keputusan
2.1. Bilangan Kedua-dua NCR+ dan NCR− ILC3s Meningkat dalam Nodus Limfa Pengeringan Tempatan selepas Pentadbiran Vaksin DC
Vaksin DC telah disediakan dengan membezakan DC daripada sel yang berasal dari murine-bone-sumsum ex vivo. DC ini telah dirangsang untuk menggalakkan kematangan mereka supaya mereka akan memperoleh fenotip imunogenik. DC kemudiannya dimuatkan dengan peptida. Oleh kerana kajian ini memberi tumpuan kepada sifat komunikasi antara dua leukosit semula jadi, DC, dan ILC3s, peptida yang dipilih untuk pengeluaran vaksin secara sengaja tidak relevan dengan model biologi kami untuk mengelakkan sel T spesifik antigen menjadi pembolehubah yang mengelirukan. Oleh itu, vaksin DC telah dimuatkan dengan peptida yang berasal dari ayam-ovalbumin.
Untuk mula menyiasat sama ada vaksinasi DC mempengaruhi populasi ILC3, kami terlebih dahulu menilai sama ada terdapat perbezaan dalam selular proksimal ke tapak vaksinasi. Terdapat perubahan dalam nodus limfa penyaliran tempatan berikutan vaksinasi DC, yang termasuk peningkatan bilangan ILC3s (Rajah 1). Kinetik peningkatan dalam ILC3s menunjukkan bahawa ILC3s secara beransur-ansur meningkat berikutan vaksinasi DC (Rajah 1b, c). Bilangan NCR+ dan NCR− ILC3 dalam nodus limfa penyaliran tempatan telah dinilai dan kedua-dua subpopulasi meningkat berikutan pemberian vaksin DC. Walaupun kedua-dua populasi NCR+ dan NCR− ILC3 memuncak pada tiga hari selepas vaksinasi DC, NCR− ILC3 kembali ke nombor homeostatik tujuh hari selepas imunisasi manakala bilangan NCR+ ILC3 kekal lebih tinggi berbanding tikus kawalan yang dirawat secara palsu.
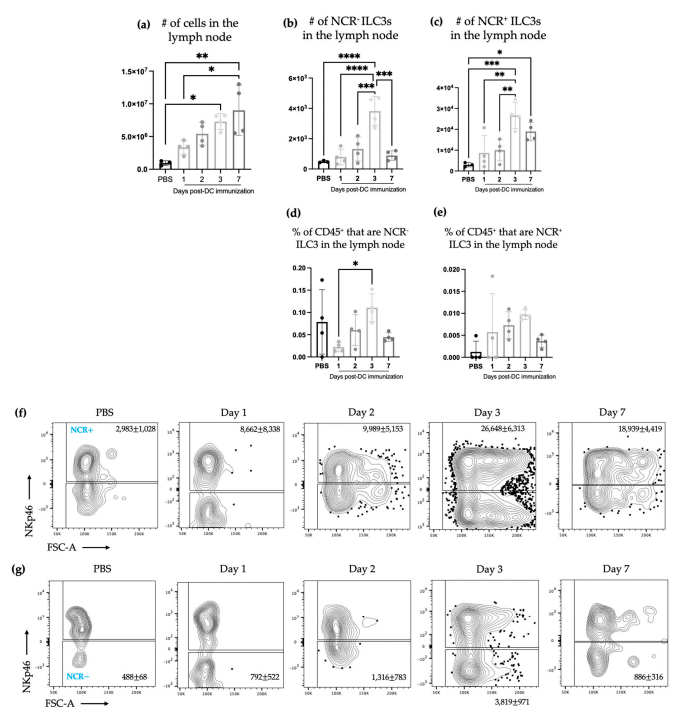
Rajah 1. Bilangan reseptor sitotoksisiti semula jadi (NCR)+ dan NCR− jenis 3 sel limfoid semula jadi (ILC3s) meningkat dalam nodus limfa penyaliran tempatan selepas imunisasi DC. Tikus C57BL/6 betina telah disuntik dengan vaksin DC melalui suntikan tapak kaki belakang. Nodus limfa popliteal diperiksa untuk populasi ILC3. (a) Jumlah bilangan sel dalam nodus limfa ditentukan. Pengumpulan (b) NCR− ILC3s dan (c) NCR+ ILC3s dalam nodus limfa dan peratusan sel CD{{10}} dalam nodus limfa yang (d) NCR− ILC3s dan (e) NCR+ ILC3s. Setiap bar mewakili data daripada empat nodus limfa popliteal. Ujian-t Pelajar digunakan pada setiap titik masa untuk menentukan perbezaan ketara antara tikus kawalan yang disuntik dengan garam penimbal fosfat (PBS) dan tikus yang disuntik dengan vaksin DC (nilai-p * < 0.{{ 21}}5, ** < 0.005, *** < 0.0005 dan **** < 0.0001). Plot titik perwakilan menunjukkan bilangan purata (f) NCR− ILC3s dan (g) NCR+ ILC3s dalam nodus limfa popliteal yang mengalir. Graf memaparkan min dengan sisihan piawai.
2.2. Vaksin DC Meningkatkan Pengeluaran Sitokin ILC3 dalam Limpa tanpa Mengubah Jumlah Bilangan ILC3 Splenik
Seterusnya, perubahan sistemik dalam populasi ILC3 telah diperiksa dengan menilai limpa, yang merupakan organ limfoid sekunder terbesar [29], seminggu selepas vaksinasi DC, yang merupakan titik masa standard makmal kami untuk menilai perubahan dalam leukosit secara sistemik. Tiada perbezaan ketara yang diperhatikan dalam jumlah bilangan NCR+ atau NCR− ILC3 dalam limpa (Rajah 2).
![Figure 2. There were no changes in the number of splenic ILC3s after DC immunization. Female C57BL/6 mice (n = 8 [PBS] or 10 [DC]) were inoculated with DC vaccines via hind footpad injections. Spleens were harvested one-week following inoculation and examined for ILC3 populations. Splenic total number of (a) NCR− ILC3s and (b) NCR+ ILC3s (and the geometric mean fluorescent intensity of T-bet for NCR+ ILC3s) and the percentage of splenic CD45+ cells that were (c) NCR− ILC3s and (d) NCR+ ILC3s were monitored and quantified by flow cytometry analysis. A Student's t-test was used to determine the significance between the populations in the control mice inoculated with phosphate-buffered saline (PBS) and the DC-inoculated mice. The means were not significantly different. Representative dot plots showing the average number of splenic (e) NCR− ILC3s and NCR+ ILC3s. The standard deviation and mean are represented by the graph bars and error bars. Figure 2. There were no changes in the number of splenic ILC3s after DC immunization. Female C57BL/6 mice (n = 8 [PBS] or 10 [DC]) were inoculated with DC vaccines via hind footpad injections. Spleens were harvested one-week following inoculation and examined for ILC3 populations. Splenic total number of (a) NCR− ILC3s and (b) NCR+ ILC3s (and the geometric mean fluorescent intensity of T-bet for NCR+ ILC3s) and the percentage of splenic CD45+ cells that were (c) NCR− ILC3s and (d) NCR+ ILC3s were monitored and quantified by flow cytometry analysis. A Student's t-test was used to determine the significance between the populations in the control mice inoculated with phosphate-buffered saline (PBS) and the DC-inoculated mice. The means were not significantly different. Representative dot plots showing the average number of splenic (e) NCR− ILC3s and NCR+ ILC3s. The standard deviation and mean are represented by the graph bars and error bars.](/Content/uploads/2023842169/20231121112027297db863b910419cb14e5be0ef848770.png)
Rajah 2. Tiada perubahan dalam bilangan ILC3 splenik selepas imunisasi DC. Tikus C57BL/6 betina (n=8 [PBS] atau 10 [DC]) telah disuntik dengan vaksin DC melalui suntikan tapak kaki belakang. Limpa dituai seminggu selepas inokulasi dan diperiksa untuk populasi ILC3. Jumlah bilangan limpa (a) NCR− ILC3s dan (b) NCR+ ILC3s (dan purata keamatan pendarfluor geometri T-bet untuk NCR+ ILC3s) dan peratusan sel CD limpa45+ yang (c) NCR− ILC3s dan (d) NCR+ ILC3s dipantau dan dikira dengan analisis sitometri aliran. Ujian-t Pelajar digunakan untuk menentukan kepentingan antara populasi dalam tikus kawalan yang disuntik dengan garam penampan fosfat (PBS) dan tikus yang diinokulasi DC. Caranya tidak jauh berbeza. Plot titik perwakilan menunjukkan purata bilangan splenik (e) NCR− ILC3s dan NCR+ ILC3s. Sisihan piawai dan min diwakili oleh bar graf dan bar ralat.
Memandangkan profil sitokin ILC3 boleh dipengaruhi oleh faktor persekitaran, pengeluaran ILC3 IL-22 dan IL-17 dalam limpa diukur seminggu selepas vaksinasi DC. Terdapat peningkatan dalam ILC3 yang menghasilkan IL-17 atau IL-22 atau kedua-dua sitokin dalam tikus yang dirawat dengan vaksin DC berbanding tikus kawalan (Rajah 3).
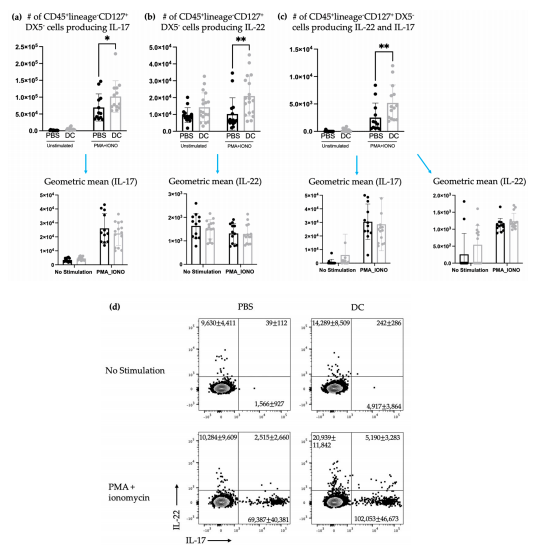
Rajah 3. Terdapat peningkatan dalam ILC3 splenik yang menghasilkan IL-17 dan IL-22 berikutan imunisasi DC. Tikus C57BL/6 betina (n=12–18) telah disuntik dengan vaksin DC melalui suntikan tapak kaki belakang. Tikus kawalan telah dirawat dengan garam penampan fosfat (PBS). Seminggu selepas imunisasi, limpa dituai dan diperiksa untuk IL-17- dan IL{{10}}menghasilkan ILC. Bilangan sel keturunan−CD127+DX5− yang menghasilkan (a) IL-17, (b) IL-22 dan (c) kedua-dua IL-17 dan IL{{ 16}} dan keamatan pendarfluor min geometri yang sepadan ditentukan menggunakan pewarnaan sitokin intraselular dan sitometri aliran. Data dianalisis menggunakan ujian ANOVA dua hala (nilai-p * < 0.05, ** < 0.005). (d) Plot titik perwakilan menunjukkan purata bilangan CD45+ keturunan-CD127+DX5− sel splenik yang menghasilkan IL-17 dan/atau IL-22. Graf memaparkan min dengan sisihan piawai.
2.3. Subpopulasi ILC3 Mengikuti Imunisasi dan Cabaran DC dengan Sel Melanoma B16F10
ILC3 boleh memainkan dua peranan dalam perkembangan kanser dengan menyumbang kepada kedua-dua tindak balas pro dan antitumorigenik [22]. Oleh itu, pengaruh vaksinasi DC pada tindak balas ILC3 dalam konteks kanser telah disiasat. Tikus telah dirawat dengan vaksin DC dan seminggu kemudian, mereka dicabar secara intravena dengan sel melanoma B16F10, yang mengakibatkan pembenihan paru-paru. Seperti yang dinyatakan, kerana hanya komponen imuniti semula jadi yang dinilai, pendidikan khusus antigen oleh vaksin tidak akan dinilai dalam eksperimen kami dan, oleh itu, model melanoma yang digunakan tidak menyatakan ovalbumin, menjadikan peptida dimuatkan ke DC. tidak relevan. Eksperimen kinetik (Rajah 1) menunjukkan bahawa tindak balas tempatan ILC3 boleh diperhatikan dalam masa tiga hari. Oleh itu, tiga hari selepas cabaran, bilangan subpopulasi ILC3 dan keupayaan mereka untuk menghasilkan sitokin telah diperiksa dalam limpa dan paru-paru. Sama seperti apa yang diperhatikan dalam limpa tikus naif, tidak terdapat perbezaan yang signifikan dalam jumlah bilangan NCR+ dan NCR− ILC3 splenik antara kumpulan kawalan dan kumpulan imunisasi DC (Rajah 4). Walau bagaimanapun, tidak seperti dalam model naif, dalam limpa, tiada lagi perubahan dalam pengeluaran IL-17 dan/atau IL-22 (Rajah 5).

Rajah 4. Tiada perubahan dalam jumlah bilangan ILC3 splenik selepas vaksinasi DC dan cabaran dengan sel melanoma B16F10. Tikus C57BL/6 betina (n=10) telah disuntik dengan vaksin DC melalui suntikan tapak kaki belakang dan seminggu kemudian, tikus diberikan dengan 3 × 105 sel B16F10 melalui suntikan urat ekor. Limpa dituai dan diperiksa untuk pengumpulan populasi ILC3 tiga hari selepas pentadbiran B16F10. Bilangan splenik (a) NCR− ILC3s dan (b) NCR+ ILC3s (dan purata geometrik intensiti pendarfluor T-bet untuk NCR+ ILC3s) dan peratusan sel CD splenik45+ yang (c) NCR− ILC3s dan (d) NCR + ILC3s dipantau dan dikira oleh sitometri aliran. Ujian-t Pelajar digunakan untuk menentukan kepentingan antara populasi dalam tikus kawalan yang dirawat dengan garam penampan fosfat (PBS) dan tikus yang diinokulasi DC. Caranya tidak jauh berbeza. Plot titik perwakilan menunjukkan purata bilangan splenik (e) NCR− ILC3s dan NCR+ ILC3s. Min dan sisihan piawai diwakili dengan graf bar dan bar ralat.

Rajah 5. Tiada perubahan dalam bilangan IL-17 dan/atau IL-22-splenik yang menghasilkan ILC selepas vaksinasi DC dan cabaran dengan sel melanoma B16F10. Tikus C57BL/6 betina (n=10) telah disuntik dengan vaksin DC melalui suntikan tapak kaki belakang dan seminggu kemudian, 3 × 105 sel B16F10 diberikan secara intravena. Tiga hari kemudian, limpa dituai dan diperiksa untuk pengeluaran sitokin ILC3. Bilangan sel CD keturunan127+DX5- yang menghasilkan (a) IL-17, (b) IL-22 dan (c) kedua-dua IL-17 dan IL-22 dan purata keamatan pendarfluor geometri yang sepadan ditentukan menggunakan pewarnaan sitokin intraselular dan sitometri aliran. Data dianalisis menggunakan ujian ANOVA dua hala dan tiada perbezaan yang signifikan antara tikus yang divaksinasi DC dan kawalan yang dirawat dengan salin buffer fosfat (PBS) dikesan. (d) Plot titik perwakilan menunjukkan purata bilangan sel CD45+sel keturunan127+DX5- splenik yang menghasilkan IL-17 dan/atau IL-22.
Suntikan intravena sel B16F10 melalui urat ekor adalah model tikus biasa metastasis melanoma sintetik ke paru-paru [30]. Oleh itu, paru-paru juga diperiksa untuk menentukan bilangan subpopulasi ILC3 dan menilai pengeluaran sitokin mereka.
Terdapat penurunan dalam bilangan NCR− ILC3s dengan peningkatan serentak dalam bilangan NCR+ ILC3s (Rajah 6). Walau bagaimanapun, tiada kesan yang diperhatikan daripada vaksinasi DC terhadap pengeluaran sitokin pengantara ILC3-dalam paru-paru (Rajah 7).
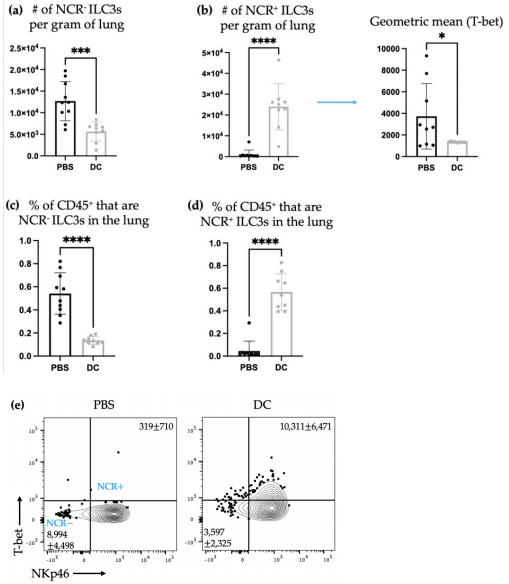
Rajah 6. Berikutan imunisasi DC dan cabaran dengan sel B16F10, terdapat perubahan berangka dalam subpopulasi ILC3 dalam paru-paru. Tikus C57BL/6 betina (n=10) menerima vaksin DC melalui suntikan tapak kaki belakang dan seminggu kemudian, 3 × 105 sel B16F10 diberikan secara intravena. Tiga hari selepas cabaran, paru-paru diperiksa menggunakan sitometri aliran untuk bilangan (a) NCR− ILC3s dan (b) NCR+ ILC3s (dan purata keamatan pendarfluor geometri T-bet untuk NCR+ ILC3s) dan peratusan CD{ {18}} sel yang (c) NCR− ILC3s dan (d) NCR+ ILC3s. Ujian-t Pelajar digunakan untuk menentukan kepentingan antara subpopulasi dalam tikus kawalan yang dirawat dengan garam penampan fosfat (PBS) dan tikus yang diinokulasi DC (nilai-p *<0.05, *** <0.0005, and **** < 0.0001). Representative dot plots showing the average number of pulmonary (e) NCR− ILC3s and NCR+ ILC3s. The graphs display the mean with the standard deviation.
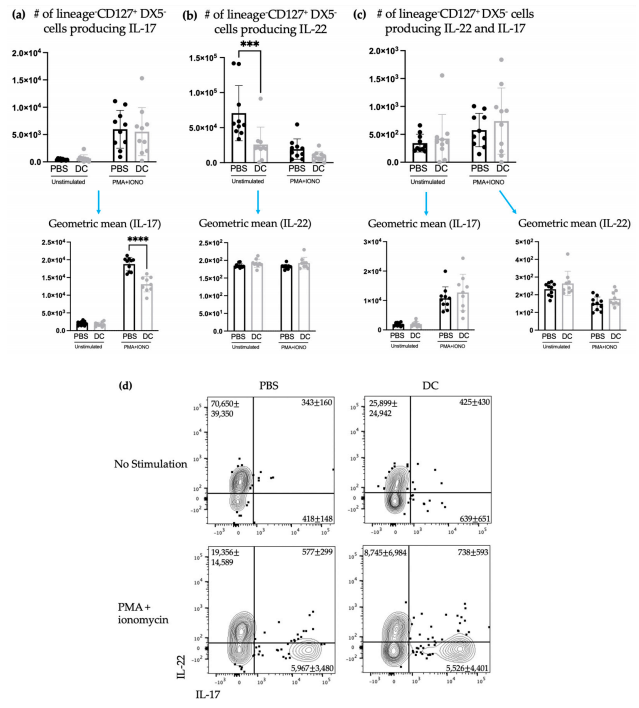
Rajah 7.Tiada perubahan dalam bilangan ILC3 yang menghasilkan IL-17 dan/atau IL-22 dalam paru-paru selepas vaksinasi DC dan cabaran dengan sel melanoma B16F10. Tikus C57BL/6 betina (n=10) telah disuntik dengan vaksin DC melalui suntikan tapak kaki belakang dan seminggu kemudian, mereka diberikan secara intravena dengan 3 × 105 sel B16F10. Tiga hari kemudian, paru-paru telah dituai dan diperiksa untuk{12}}penghasilan sitokin pengantara ILC. Bilangan sel keturunan−CD127+DX5− yang menghasilkan (a) IL-17, (b) IL-22, dan (c) kedua-dua IL{{0}} dan IL-22 serta keamatan pendarfluor purata geometriknya yang sepadan ditentukan menggunakan pewarnaan sitokin intraselular dan sitometri aliran. Data dianalisis menggunakan ujian ANOVA dua hala (nilai-p *** <0.0005). Tiada perbezaan yang ketara dalam jumlah bilangan penghasil IL-22-, penghasil IL-17-dan IL-22 dan IL-17 penghasil multi-sitokin−CD{{ 12}}sel DX5−. (d) Plot titik perwakilan menunjukkan purata bilangan sel CD45+ keturunan−CD127+DX5− pulmonari yang menghasilkan IL-17 dan/atau IL-22. Sisihan piawai dan min diwakili oleh bar graf dan bar ralat.
3. Perbincangan
Kajian yang diterangkan di sini berusaha untuk menyiasat potensi komunikasi antara ILC3 dan DC dalam konteks vaksin DC. Terdapat peningkatan dalam bilangan kedua-dua subpopulasi NCR+ dan NCR− ILC3 dalam menyalirkan nodus limfa (Rajah 1) berikutan vaksinasi DC, yang menunjukkan komunikasi tempatan yang berlaku antara vaksin DC dan subpopulasi ILC3. Walau bagaimanapun, komunikasi antara DC dan NCR+ ILC3 mempunyai pengaruh yang lebih tahan lama pada jumlah bilangan NCR+ ILC3 daripada yang diperhatikan antara DC dan NCR− ILC3s. Ini menunjukkan bahawa DC mungkin mempunyai interaksi unik dengan ILC3 bergantung pada ekspresi NCR mereka. Tiada perubahan yang diperhatikan dalam bilangan subpopulasi ILC3 dalam limpa tujuh hari selepas vaksinasi DC (Rajah 2) atau sepuluh hari selepas vaksinasi DC dan tiga hari cabaran sel melanoma selepas B16F10 (Rajah 4). Kaedah kami untuk menguji ILC3 untuk pengeluaran IL-17 dan IL-22 mereka mempunyai had kerana ia menunjukkan kedua-dua tindak balas translasi dan transkrip akibat rangsangan semula sel secara in vitro. Walau bagaimanapun, kami menambah kawalan percubaan dalam semua eksperimen, yang akan menjadi rawatan tanpa rangsangan in vitro untuk mengesan apa yang dihasilkan oleh ILC3 sebagai tindak balas kepada isyarat yang diterima dalam vivo. Seperti yang digambarkan dalam Rajah 3d, 5d dan 7d, sel yang tidak menerima rangsangan in vitro menghasilkan IL-17 dan IL-22. Di samping itu, walaupun nombor sel ILC3 splenik tidak berubah (Rajah 2), pengeluaran sitokin oleh subpopulasi ILC3 adalah berbeza tujuh hari selepas vaksinasi DC (Rajah 3). Ini mencadangkan vaksinasi DC boleh mempengaruhi kefungsian tindak balas ILC3 tanpa menjejaskannya secara berangka. Sebagai komponen sistem imun semula jadi, pemerdagangan ILC3 masuk dan keluar dari tisu mungkin berlaku dalam tempoh beberapa hari, oleh itu menghalang pengesanan perbezaan berangka termodulat rawatan tujuh hingga sepuluh hari selepas vaksinasi DC. Bukti untuk ini diperhatikan dalam nodus limfa yang mengeringkan vaksin DC di mana bilangan ILC3 meningkat dalam tempoh tiga hari dan kemudian mula berkurangan (Rajah 1). Oleh itu, mungkin terdapat perubahan berangka dalam subpopulasi ILC3 dalam limpa yang terlepas kerana mereka telah kembali ke nombor homeostatik oleh imunisasi pasca-DC hari ketujuh. Walau bagaimanapun, kajian tertumpu pada tindak balas yang lebih tahan lama berbanding tindak balas sementara jangka pendek dan, oleh itu, tidak menyiasat jalan ini dengan lebih lanjut. Menariknya, walaupun bilangan subpopulasi ILC3 splenik tidak berbeza daripada kumpulan kawalan, profil sitokin mereka telah diubah (Rajah 3). Pengeluaran IL-22 dan IL-17 telah meningkat dalam ILC3 splenik, sekali gus menunjukkan bahawa vaksinasi DC mempunyai kesan sistemik pada ILC3. Ringkasnya, vaksinasi DC tidak memberi kesan kepada kuantiti ILC3 splenik tetapi mempengaruhi fungsinya.
Walaupun terdapat kesan yang berterusan pada ILC3-pengeluaran sitokin yang diperoleh tujuh hari selepas imunisasi DC dalam limpa tikus bebas tumor, pengaruh ini pada ILC3 dalam limpa tidak dapat dikesan tiga hari selepas cabaran intravena dengan sel melanoma B16F10 ( Rajah 5). Vaksin DC muncul kepada populasi ILC3 utama dalam model bebas tumor yang ditindas apabila cabaran tumor. Oleh kerana ILC sangat dipengaruhi oleh persekitaran mereka, ini boleh mencadangkan bahawa komunikasi antara DC dalam vaksin dan ILC3 adalah terhad kepada model bebas tumor. Sebaliknya, ini juga mungkin disebabkan oleh pengerahan ILC3 yang telah disiapkan ke lokasi lain dalam badan di mana B16F10s mungkin telah berkumpul dan mewujudkan persekitaran mikro yang mendorong pengambilan leukosit.
Terdapat pergeseran dalam subpopulasi ILC3 yang diperhatikan dalam paru-paru sepuluh hari selepas vaksinasi DC dan tiga hari cabaran sel selepas B16F10 berbanding tikus kawalan bukan DC yang divaksinasi yang hanya menerima pentadbiran sel B16F10. Khususnya, terdapat peningkatan dalam bilangan NCR+ ILC3s dan penurunan dalam NCR− ILC3s dalam paru-paru (Rajah 6). T-bet ialah faktor transkripsi yang dikaitkan dengan tindak balas Th1 [31]. Oleh itu, peningkatan dalam NCR+ ILC3s, yang menyatakan T-bet, menunjukkan potensi promosi imuniti jenis 1. Ini boleh menjadi tindak balas ILC3 yang bermanfaat dalam konteks kanser di mana tindak balas imun jenis 1 biasanya dikehendaki.

manfaat cistanche untuk lelaki-menguatkan sistem imun
Telah ditunjukkan bahawa NCR+ ILC3s boleh diperolehi daripada subset NCR− ILC3s [16]. Oleh itu, peningkatan dalam NCR+ ILC3s dan penurunan dalam NCR− ILC3s boleh dikaitkan dengan rangsangan yang mendorong suis dalam NCR− ILC3s untuk menjadi NCR+ ILC3s. Jika ILC3 sedang menjalani penukaran fenotip daripada NCR− kepada NCR+, mereka mungkin tidak dapat menghasilkan sitokin semasa atau sejurus selepas bertukar dan semasa menyesuaikan diri dengan persekitaran dan fenotip baharu mereka. Oleh itu, pengeluaran sitokin mereka mungkin telah dihentikan atau ditangguhkan semasa penukaran fenotip sedang berlaku, yang boleh menjelaskan sebab tiada perubahan dalam ILC3-pengantara IL-17 dan/atau IL-22 pengeluaran dalam paru-paru (Rajah 7). Walau bagaimanapun, mungkin juga vaksinasi DC tidak mempengaruhi pengeluaran sitokin oleh ILC3 dalam paru-paru pada masa ini.
4. Bahan dan Kaedah
Kelulusan Etika
Semua kajian murine dilakukan mengikut protokol penggunaan haiwan #3807 di bawah pengawasan kakitangan penjagaan haiwan di Universiti Guelph.
tikus
Tikus C57BL6 betina telah diterima daripada Charles River Laboratories berumur lima hingga lapan minggu. Tikus-tikus itu ditempatkan dalam persekitaran terkawal di unit pengasingan haiwan Universiti Guelph dan diberi masa seminggu untuk menyesuaikan diri sebelum memulakan eksperimen. Tikus diberi makan dan diberi air secara ad libitum.
Kultur Sel Dendritik
Femur dan tibia tikus C57BL6 betina telah dituai dan hujung tulang dipotong. Menggunakan picagari, sumsum tulang tibias dan femur dikeluarkan bersama PBS ke dalam cawan Petri. Sumsum tulang digantung semula menjadi penggantungan sel tunggal dan dikira menggunakan hemocytometer. Sel-sel itu kemudiannya digantung semula dalam media (RPMI [HyClone Cat# SH30027.01] dengan 2-mercaptoethanol [Gibco Ref# 21985-023], 1% penicillin/streptomycin [HyClone Cat# SV30010] dan 10% serum lembu janin [VWR Cat#97068-085]) kepada kepekatan 1.25 × 106 sel per mL, ditambah dengan 20 ng/mL granulocyte–macrophage colony-stimulating factor (GM-CSF) (Biolegend Cat#576308) dan dialiquoted ke dalam kelalang kultur 25 cm2, 5 mL setiap kelalang. Kultur dimasukkan ke dalam inkubator yang dilembapkan pada suhu 37 ◦C dengan 5% CO2 dan dibiarkan tumbuh selama 7 hari. Pada hari kedua kultur, 5 mL media segar dengan 20 ng/mL GM-CSF telah ditambah. Pada hari kelima, 5 mL setiap kultur disentrifugasi, dan supernatan dikeluarkan. Sel-sel telah digantung semula dalam 5 mL media segar dengan 20 ng/mL GM-CSF dan ditambah semula ke dalam kelalang kultur. Budaya dituai pada hari ke-7 dan disediakan untuk vaksinasi.
Penyediaan Vaksinasi Sel Dendritik
Kultur sel dendritik (DC) dipindahkan ke tiub kon 50 mL dan dikira menggunakan hemocytometer. Sel-sel telah dirangsang dengan 100 ng/mL lipopolysaccharide (LPS) daripada Escherichia coli O55:B5 (Sigma Cat#L2880) dan 1 µg/mL chicken ovalbumin (OVA)257–264(SIIN) (PepScan Systems, Lelystad, Belanda) selama 1 jam dalam inkubator pada suhu 37 ◦C dengan 5% CO2. Sel-sel kemudiannya dibasuh dengan PBS tiga kali dan digantung semula kepada kepekatan 5 × 105 sel setiap 30 μL. Vaksin telah diberikan pada dos 5 × 105 sel setiap 30 µL PBS.
Pemprosesan Tisu
Nodus limfa dan limpa dituai dan dimasukkan ke dalam piring Petri dengan 2 mL larutan garam penimbal Hanks (HBSS). Mereka ditekan ke dalam penggantungan sel tunggal menggunakan bahagian belakang penyumbat picagari 3 mL. Penggantungan sel tunggal telah ditapis ke dalam tiub kon 50 mL menggunakan penapis sel bersaiz 70 µm-liang. Nodus limfa dikira menggunakan hemocytometer. Limpa telah disentrifugasi, supernatan dikeluarkan, dan sel-sel digantung semula dalam penimbal lisis ACK (8.29 g NH4Cl [0.15 M], 1 g KHCO3 [10.0 mM], 37.2 mg Na2EDTA [0.1 mM] dalam 1 mL air Milli Q) dan dibiarkan selama lima minit untuk melisiskan eritrosit. Sel-sel telah dibasuh dengan HBSS dua kali sebelum digantung semula dalam media dan dikira menggunakan hemocytometer.
Paru-paru dituai dan ditimbang sebelum dimasukkan ke dalam tiub MACSTM lembut yang mengandungi 1 mg/mL kolagenase IV (Gibco Ref#17104-019) dan 5 µg/mL DNase I (Roche Ref#11284932001) dalam HBSS. Menggunakan pemisah gentleMACSTM, sampel dijalankan melalui protokol paru-paru A dan kemudian diinkubasi selama 20 minit dalam inkubator pada suhu 37 ◦C dengan 5% CO2. Sampel kemudiannya dijalankan melalui protokol paru-paru B pada pemisah gentleMACSTM. Dua kali jumlah sampel HBSS telah ditambah kepada sampel untuk meneutralkan tindak balas enzim. Sampel ditapis ke dalam tiub kon 50 mL melalui penapis sel bersaiz 70 µm-pori. Sel-sel itu kemudiannya dibasuh dua kali dengan HBSS dan digantung semula dalam penimbal lisis ACK. Selepas lima minit dalam penimbal lisis ACK, sel-sel telah dibasuh dua kali dengan HBSS dan digantung semula dalam media.
Ujian Tindak Balas Sitokin
Suspensi sel tunggal daripada sampel tisu telah disemai ke dalam 96-plat perigi dalam pendua, di mana satu telaga dianggap sebagai kawalan tanpa rangsangan dan satu lagi menerima rawatan perangsang. Telaga yang tidak dirangsang hanya diberi media dan telaga yang dirawat perangsang menerima 10 ng/mL phorbol myristate acetate (PMA) dan 1,500 ng/mL ionomycin dalam media. Sel-sel tersebut diletakkan di dalam inkubator pada suhu 37 ◦C dengan 5% CO2 selama satu jam. Kemudian, Brefeldin A (GolgiPlug, Biolegend Cat#420601) (x100 pencairan) telah ditambah kepada semua telaga sampel, dan plat diletakkan semula ke dalam inkubator selama empat jam tambahan. Sel-sel itu kemudian dibasuh dua kali dengan PBS dan diwarnai untuk analisis oleh sitometri aliran.
B16F10 sel melanoma
Sel B16F10 telah dicairkan daripada nitrogen cecair dan dikira menggunakan hemocytometer. Sel-sel tersebut kemudiannya digantung semula dalam media (medium Eagles diubah suai glukosa tinggi Dulbecco [HyClone Cat#SH3002201] dengan 1% penisilin/streptomycin [HyClone Cat# SV30010] dan 10% serum anak lembu lembu [VWR Cat#10158-358]) untuk kepekatan 1 × 105 sel per mL. Sel B16F10 kemudiannya diasingkan ke dalam kelalang kultur dan dimasukkan ke dalam inkubator pada suhu 37 ◦C dengan 5% CO2. Untuk menyediakan sel B16F10 untuk pentadbiran, sel telah dipindahkan dari kelalang kultur ke tiub kon 50 mL, dibasuh dengan PBS, dan kemudian digantung semula dalam PBS. Sel-sel dikira menggunakan hemocytometer dan digantung semula dalam PBS untuk memberikan dos 3 × 105 sel setiap 200 μL.
Pewarnaan Antibodi Sitokin Intraselular
Sel-sel telah disemai ke dalam {{0}}plat perigi dan digantung semula dalam blok Fc (anti-CD16/CD32, BioLegend Cat#101320) dan diinkubasi pada 4 ◦C selama 15 minit. Sel-sel telah dibasuh dengan garam penampan fosfat yang mengandungi 0.5% albumin serum lembu (penampan FACS) dua kali, kemudian digantung semula dalam campuran induk antibodi pewarna permukaan sel (CD45, BioLegend Cat#103132; NKp46, BioLegend Cat#137617; DX5, BioLegend Cat#108919; CD127, BioLegend Cat#135007; Lineage Cocktail, BioLegend Cat#133311) dan diinkubasi pada 4 darjah selama 20 minit. Sel-sel telah dibasuh dengan salin penampan fosfat dua kali dan digantung semula dalam pewarna daya maju Zombie Aqua Fixable (FVD) (BioLegend Cat#423101) dan diinkubasi pada suhu 4◦C selama 30 minit. Salin penampan fosfat digunakan untuk mencuci sel dua kali sebelum penggantungan semula dalam penimbal penetapan (BioLegend Cat#420801). Sel-sel telah diinkubasi pada 4 ◦C selama 20 minit. Selepas penetapan, sel telah dibasuh dua kali dengan penimbal permeabilisasi (BioLegend Cat#421002). Sel-sel telah digantung semula dalam campuran induk antibodi pewarna intraselular (IL-22, BioLegend Cat#516404; IL-17A, eBioscience Cat# 17-7177-81) dan diinkubasi pada suhu 4 ◦C untuk 20 min. Sel-sel telah dibasuh dua kali dengan penimbal permeabilisasi, kemudian digantung semula dalam penimbal FAC, dan kemudian diproses dengan sitometer aliran BD FACSCantoTM II dan dianalisis menggunakan perisian BD FACSDivaTM.

manfaat cistanche untuk lelaki-menguatkan sistem imun
Pewarnaan Antibodi Faktor Transkripsi
Sel-sel telah disemai ke dalam {{0}}plat perigi dan digantung semula dalam blok FC (anti-CD16/CD32 BioLegend Cat# 101320) dan diinkubasi pada 4 ◦C selama 15 minit. Sel-sel telah dibasuh dua kali dengan penimbal FAC (0.5% dalam albumin serum lembu [HyClone Cat# SH30574.02] dalam PBS), kemudian digantung semula dalam campuran induk antibodi pewarna permukaan sel (CD45, BioLegend Cat#103132; NKp46 , BioLegend Cat#137617; DX5, BioLegend Cat# 108919; CD127, BioLegend Cat#135007; Lineage Cocktail, BioLegend Cat#133311), dan diinkubasi pada suhu 4 ◦C selama 20 minit. Sel-sel itu kemudiannya dibasuh dengan garam penampan fosfat dua kali digantung semula dalam FVD (BioLegend Cat#423101) dan diinkubasi pada 4 ◦C selama 20 minit. Sel-sel telah dibasuh dengan garam penimbal fosfat dua kali dan digantung semula dalam penimbal penetapan FoxP3 tetikus (BD Pharmingen BD Sciences Cat#51-9006124) dan diinkubasi pada 4 ◦C selama 30 minit. Selepas penetapan, sel telah dibasuh dengan penimbal permeabilisasi FoxP3 tetikus (BD Pharmingen BD Sciences Cat# 51-9006125) yang digantung semula dalam penimbal permeabilisasi FoxP3, dan diinkubasi pada 37 ◦C selama 30 minit. Sel-sel telah digantung semula dalam antibodi faktor transkripsi (ROR gamma(t), eBioscience Cat#17-6988-82; T-bet, eBioscience Cat# 12-5825-82) dan diinkubasi pada 4 ◦C selama 20 minit. Sel-sel telah dibasuh dengan penimbal permeabilisasi dua kali, kemudian digantung semula dalam penimbal FAC, dan dianalisis menggunakan sitometer aliran BD FACSCantoTM II dan perisian BD FACSDivaTM.
Analisis statistik
Populasi splenik dan pulmonari NCR+ dan NCR− ILC3 dianalisis menggunakan ujian-t tidak berpasangan. Analisis populasi eksperimen kinetik dibandingkan menggunakan analisis varians sehala biasa (ANOVA) dan ujian perbandingan berganda Tukey. Analisis sitokin dalam limpa dan paru-paru diperiksa menggunakan ANOVA dua hala dan ujian perbandingan berganda Šídák. Min bagi kumpulan rawatan ditakrifkan sebagai berbeza secara ketara dengan nilai p < 0.05.
Strategi gerbang
Pertama, menggunakan kawasan serakan ke hadapan (FSC-A) dan kawasan serakan sisi (SSC-A), limfosit telah berpagar. Kemudian, sel doublet dikecualikan menggunakan FSC-A dan FSC-height (FSC-H). Sel hidup telah berpagar dengan mengambil sel negatif untuk FVD. Kemudian, CD127+ dan sel koktel keturunan telah diambil untuk mengecilkan ILC. Sel CD45+ kemudiannya dihidupkan. Untuk memastikan bahawa semua sel NK dikecualikan, DX5− kemudiannya berpagar. Untuk pengecaman faktor transkripsi ILC3s, sel-sel ROR t + kemudiannya dipagarkan, dan daripada sel-sel ini, NCR+ ILC3s ialah T-bet+ dan NKp46+ dan NCR− ILC3s ialah T-bet− dan NKp46. Untuk pengecaman sitokin, selepas gating pada limfosit, sel tunggal, sel hidup dan CD{18}} keturunan−CD45+, IL-17 dan IL-22 kemudiannya berpagar sebagai dihasilkan oleh ILC3 kerana ILC3 akan menjadi satu-satunya sel dalam gerbang akhir ini yang boleh menghasilkan IL-22 dan IL-17.

manfaat cistanche untuk lelaki-menguatkan sistem imun
5. Kesimpulan
Walaupun peningkatan ILC3-yang menghasilkan IL-17 dan IL-22 pengeluaran dalam limpa yang diperhatikan dalam model bebas tumor telah hilang dalam model cabaran tumor, terdapat peralihan yang bertentangan dalam NCR+ dan Populasi NCR− ILC3 dalam paru-paru. Ini menunjukkan bahawa vaksinasi DC boleh mempengaruhi ILC3 dalam model cabaran tumor serta dalam tikus bebas tumor. Walau bagaimanapun, kesan hubungan ini antara DC dalam vaksin dan ILC3 terhadap tindak balas anti-tumor masih tidak diketahui dan merupakan hala tuju penyelidikan masa depan. Oleh itu, kajian yang diterangkan di sini menunjukkan bahawa terdapat komunikasi yang berlaku antara vaksin berasaskan DC dan subpopulasi ILC3, kedua-duanya dalam tikus bebas tumor dan tumor. Komunikasi ini dan kesan seterusnya terhadap tindak balas imun kelihatan rumit. Pemerhatian ini menyumbang kepada badan literatur yang ingin menguraikan hubungan antara vaksin DC dan ILC3 dalam usaha untuk membangunkan strategi vaksinasi DC yang dipertingkatkan. Kami mengesyorkan kajian lanjut menyiasat potensi untuk mereka bentuk strategi vaksinasi yang boleh memodulasi komunikasi ini untuk mengoptimumkan tindak balas ILC3 untuk membantu dalam tindak balas anti-tumor dan mengehadkan sokongan terhadap tindak balas pro-tumor.
Rujukan
1. Crinier, A.; Vivier, E.; Bléry, M. Sel limfoid semula jadi seperti pembantu dan imunoterapi kanser. Semin. Immunol. 2019, 41, 101274. [CrossRef] [PubMed]
2. Salimi, M.; Wang, R.; Yao, X.; Li, X.; Wang, X.; Hu, Y.; Chang, X.; Fan, P.; Dong, T.; Ogg, G. Populasi sel limfoid semula jadi yang diaktifkan terkumpul dalam tisu tumor manusia. BMC Cancer 2018, 18, 341. [CrossRef] [PubMed]
3. Ludah, H.; Bernink, JH; Lanier, sel L. NK dan sel limfoid semula jadi jenis 1: Rakan kongsi dalam pertahanan perumah. Nat. Immunol. 2016, 17, 758–764. [CrossRef] [PubMed]
4. Bruchard, M.; Ghiringhelli, F. Mentafsir Peranan Sel Limfoid Semula Jadi dalam Kanser. Depan. Immunol. 2019, 10, 656. [CrossRef]
5. Mazzurana, L.; Rao, A.; Van Acker, A.; Mjösberg, J. Peranan sel limfoid semula jadi dalam sistem imun manusia. Semin. Imunopathol. 2018, 40, 407–419. [CrossRef]
6. Solano-Gálvez, SG; Tovar-Torres, SM; Tron-Gómez, MS; Weiser-Smeke, AE; Álvarez-Hernández, DA; Franyuti-Kelly, GA; Tapia-Moreno, M.; Ibarra, A.; Gutiérrez-Kobeh, L.; Vázquez-López, R. Sel Dendritik Manusia: Ontogeni dan Subsetnya dalam Kesihatan dan Penyakit. Med. Sci. 2018, 6, 88. [CrossRef]
7. Steinman, RM; Hemmi, H. Sel dendritik: Menterjemah imuniti semula jadi kepada adaptif. Curr. Atas. mikrobiol. Immunol. 2006, 311, 17–58. [CrossRef]
8. Fu, C.; Ma, T.; Zhou, L.; Mi, QS; Jiang, A. Vaksin Berasaskan Sel Dendritik Melawan Kanser: Cabaran, Kemajuan dan Peluang Masa Depan. Immunol. Menyiasat. 2022, 51, 2133–2158. [CrossRef]
9. Karimi, K.; Boudreau, JE; Fraser, K.; Liu, H.; Delanghe, J.; Gauldie, J.; Xing, Z.; Bramson, JL; Wan, Y. Kekebalan Antitumor Yang Dipertingkatkan yang Ditimbulkan oleh Vaksin Sel Dendritik Adalah Hasil Keupayaan Mereka untuk Melibatkan Kedua-dua Sel NK penghasil CTL dan IFN. Mol. Di sana. 2008, 16, 411–418. [CrossRef]
10. Bouwer, AL; Saunderson, SC; Caldwell, FJ; Damani, TT; Pelham, SJ; Dunn, AC; Jack, RW; Stoitzner, P.; McLellan, sel NK AD diperlukan untuk imunoterapi berasaskan sel dendritik pada masa cabaran tumor. J. Immunol. 2014, 192, 2514–2521. [CrossRef]
11. Pampena, MB; Levy, EM Sel pembunuh semulajadi sebagai sel pembantu dalam vaksin kanser sel dendritik. Depan. Immunol. 2015, 6, 13. [CrossRef] [PubMed]
12. Gardner, A.; de Mingo Pulido, Á.; Ruffell, B. Sel Dendritik dan Peranannya dalam Imunoterapi. Depan. Immunol. 2020, 11, 924. [CrossRef] [PubMed]
13. Cortez, VS; Robinette, ML; Colonna, M. Sel limfoid semula jadi: Pandangan baharu tentang fungsi dan perkembangan. Curr. Pendapat. Immunol. 2015, 32, 71–77. [CrossRef] [PubMed]
14. Montaldo, E.; Juelke, K.; Romagnani, C. Kumpulan 3 sel limfoid semula jadi (ILC3s): Asal, pembezaan, dan keplastikan pada manusia dan tikus. Eur. J. Immunol. 2015, 45, 2171–2182. [CrossRef]
15. Vacca, P.; Chiossone, L.; Mingari, MC; Moretta, L. Keheterogenan Sel NK dan Sel Limfoid Semula Jadi Lain dalam Manusia dan Murine Decidua. Depan. Immunol. 2019, 10, 170. [CrossRef] [PubMed]
16. Rankin, LC; Girard-Madoux, MJ; Seillet, C.; Mielke, LA; Kerdiles, Y.; Fenis, A.; Wieduwild, E.; Putoczki, T.; Mondot, S.; Lantz, O.; et al. Pelengkap dan redundansi IL-22-menghasilkan sel limfoid semula jadi. Nat. Immunol. 2016, 17, 179–186. [CrossRef] [PubMed]
17. Hoorweg, K.; Peters, CP; Cornelissen, F.; Aparicio-Domingo, P.; Papazian, N.; Kazemier, G.; Mjösberg, JM; Spits, H.; Cupedo, T. Perbezaan Fungsian antara NKp44(-) Manusia dan NKp44(+) RORC(+) Sel Limfoid Semulajadi. Depan. Immunol. 2012, 3, 72. [CrossRef]
18. Carrega, P.; Loiacono, F.; Di Carlo, E.; Scaramuccia, A.; Mora, M.; Conte, R.; Benelli, R.; Spaggiari, GM; Cantoni, C.; Campana, S.; et al. NCR(+) ILC3 menumpukan pada kanser paru-paru manusia dan dikaitkan dengan struktur limfoid intratumoral. Nat. Commun. 2015, 6, 8280. [CrossRef]
19. Ludah, H.; Artis, D.; Colonna, M.; Diefenbach, A.; Di Santo, JP; Eberl, G.; Koyasu, S.; Locksley, RM; McKenzie, AN; Mebius, RE; et al. Sel limfoid semula jadi–cadangan untuk tatanama seragam. Nat. Rev. Immunol. 2013, 13, 145–149. [CrossRef]
20. Tunang, R.; Finlay, CM; Willis, C.; Bevington, SL; Soley, J.; Ng, STH; Baker, SM; Andrews, S.; Hepworth, MR; Withers, rangkaian faktor transkripsi DR Reciprocal mentadbir fungsi subset ILC3 pemastautin tisu dan identiti. Nat. Immunol. 2021, 22, 1245–1255. [CrossRef]
21. van Beek, JJP; Martens, AWJ; Bakdash, G.; de Vries, Sel Limfoid Semulajadi IJM dalam Kekebalan Tumor. Bioperubatan 2016, 4, 7. [CrossRef] [PubMed]
22. Mattner, J.; Wirtz, S. Kawan atau Lawan? Peranan Samar-samar Sel Limfoid Semula Jadi dalam Perkembangan Kanser. Trend Immunol. 2017, 38, 29–38. [CrossRef]
23. Kirchberger, S.; Royston, DJ; Boulard, O.; Thornton, E.; Franchini, F.; Szabady, RL; Harrison, O.; Powrie, F. Sel limfoid semula jadi mengekalkan kanser kolon melalui penghasilan interleukin-22 dalam model tetikus. J. Exp. Med. 2013, 210, 917–931. [CrossRef] [PubMed]
24. Irshad, S.; Flores-Borja, F.; Lawler, K.; Monypenny, J.; Evans, R.; Lelaki, V.; Gordon, P.; Cheung, A.; Gazinska, P.; Noor, F.; et al. RORgammat(+) sel limfoid semula jadi menggalakkan metastasis nodus limfa kanser payudara. Kanser Re. 2017, 77, 1083–1096. [CrossRef] [PubMed]
25. Goc, J.; Lv, M.; Bessman, NJ; Flamar, AL; Sahota, S.; Suzuki, H.; Teng, F.; Putzel, GG; Eberl, G.; Withers, DR; et al. Disregulasi ILC3s melancarkan perkembangan dan rintangan imunoterapi dalam kanser kolon. Sel 2021, 184, 5015–5030.e16. [CrossRef]
26. Liu, Y.; Lagu, Y.; Lin, D.; Lei, L.; Mei, Y.; Jin, Z.; Gong, H.; Zhu, Y.; Hu, B.; Zhang, Y.; et al. NCR(-) Kumpulan 3 Sel Limfoid Semula Jadi Mengatur Paksi IL-23/IL-17 untuk Menggalakkan Perkembangan Karsinoma Hepatoselular. EBioPerubatan 2019, 41, 333–344. [CrossRef] [PubMed]
27. Bruchard, M.; Geindreau, M.; Perrichet, A.; Truntzer, C.; Undi, E.; Boidot, R.; Racoeur, C.; Barsac, E.; Chalmin, F.; Hibos, C.; et al. Pengambilan dan pengaktifan sel limfoid semula jadi jenis 3 menggalakkan tindak balas imun antitumor. Nat. Immunol. 2022, 23, 262–274. [CrossRef]
28. Rethacker, L.; Budak lelaki, M.; Bisio, V.; Roussin, F.; Denizeau, J.; Vincent-Salomon, A.; Borcoman, E.; Sedlik, C.; Piaggio, E.; Toubert, A.; et al. Sel limfoid semula jadi: NK dan subset ILC3 sitotoksik menyusup ke nodus limfa kanser payudara metastatik. Onkoimunologi 2022, 11, 2057396. [CrossRef]
29. Cesta, MF Struktur normal, fungsi, dan histologi limpa. Toksik. Pathol. 2006, 34, 455–465. [CrossRef]
30. Ishiguro, T.; Nakajima, M.; Naito, M.; Muto, T.; Tsuruo, T. Pengenalpastian gen yang dinyatakan secara berbeza dalam subline melanoma murine B16 dengan potensi metastatik yang berbeza. Kanser Re. 1996, 56, 875–879.
31. Szabo, SJ; Kim, ST; Costa, GL; Zhang, X.; Fathman, CG; Glimcher, LH Faktor transkripsi novel, T-bet, mengarahkan komitmen keturunan Th1. Sel 2000, 100, 655–669. [CrossRef] [PubMed]
