Interaksi Antara Antioksidan Polifenolik Quercetin Dan Naringenin Menentukan Kelakuan Kimia Dan Biologi Berkaitan Redoks Tersendiri Bagi Campuran Mereka Bahagian 3
Mar 14, 2022
Sila hubungioscar.xiao@wecistanche.comuntuk maklumat lanjut
Aktiviti antioksidan melalui ujian DPPH.
Penentuan aktiviti antioksidan bagi antioksidan yang disiasat dan campurannya telah dijalankan olehspektrofotometriujian menggunakan radikal DPPH seperti yang diterangkan sebelum inil3,55. Pertama, larutan stok radikal DPPH dicairkan dengan metanol sehingga penyerapan berjumlah 0.9±0.05 pada 515 nm. Kedua, antioksidan dan campurannya telah dicairkan dengan sewajarnya dengan 70 peratus etanol untuk mencapai kepekatan yang berada dalam julat linear assayi355. Kemudian, larutan DPPH(1 mL) dicampur dengan sampel yang dicairkan(30 μL) dan penyerapan diukur pada 515 nm selepas 10 minit pada 37 darjah C. Semua tindak balas telah dijalankan dalam 48-plat perigi. Pengukuran penyerapan dilakukan dengan bantuan spektrofotometer TECAN Infinite M200 (Tecan Group Ltd., Switzerland). Aktiviti antioksidan sampel dikira semula kepada pekali stoikiometri ng seperti yang diterangkan sebelum ini, dengan pengubahsuaian5. Secara ringkas, bilangan radikal yang dibuang oleh sampel yang diuji telah dikira berdasarkan undang-undang Beer-Lambert dan pekali kepupusan molar DPPH berikutan pengukuran yang dilakukan selepas 10 minit tindak balas antara larutan antioksidan dan radikal55. Nilai n dikira sebagai tangen bagi hubungan linear antara bilangan mol DPPH yang dibuang oleh 1 mLantioksidanlarutan dalam julat kepekatan, di mana larutan "stok" mempunyai kepekatan"100 peratus " dan kepekatan lain adalah pecahan 100 peratus seperti yang ditakrifkan oleh faktor pencairan.

Sila klik di sini untuk mengetahui lebih lanjut
Aktiviti antioksidan melalui titrasi potensiometri dan voltammetri nadi pembezaan.
Potensi pengurangan standard(E) untuk Q dan R diukur dengan pentitratan potensiometri (PT) seperti yang diterangkan di tempat lain5. Ringkasnya, sebatian yang dikaji dan titran (K, [Fe (CN)]) telah dibubarkan dalam PBS. Kepekatan sebatian tulen ialah 0.3 mg/mL, Campuran mengandungi 0.3 mg/mL setiap sebatian. Pengukuran telah dijalankan menggunakan peralatan JENCO 6230 N ORP-146C Micro Oxidation-Reduction (USA) dengan bantuan elektrod rujukan (RE) AglAgCl dan elektrod penyukat platinum. PT telah dilakukan pada 37±0.01 darjah yang dikekalkan terutamanya oleh Ultra Thermostat (PolvScience, USA). Isipadu yang sama titran telah ditambah kepada analit dan potensi mantap dibaca. Akibatnya, lengkung pentitratan, E=f(V..), telah dianalisis dengan bantuan perisian SigmaPlot Version 13.0(Systat Software Inc., UK) dengan memasang parameter sigmoid,5-matematik model kepada data eksperimen35. Potensi pada titik kesetaraan (EP lwn. RE) telah dibaca terus daripada model ini berdasarkan parameter a. Ia sama dengan isipadu titran yang ditambahkan pada titik infleksi. Akhir sekali, nilai EP berbanding SHE (potensi pengurangan standard, EO) telah dikira. Istilah pembetulan potensi RE(c) telah diwujudkan melalui pentitratan pasangan redoks, FeCl.6H, O, dan Na,S, O3.5H,O, dicirikan oleh potensi pengurangan piawai yang diketahui.
Sebaliknya, kuasa antioksidan (AOP) sebatian yang dikaji dan campurannya diukur dengan voltammetri nadi pembezaan (DPV) seperti yang ditunjukkan sebelum ini dengan pengubahsuaian. Secara ringkas, pengukuran telah dilakukan menggunakan potensiostat Gamry Reference 60{{10}} (Gamry Instruments, USA) yang mengandungi sistem tiga elektrod. Elektrod karbon berkaca(GC,1.6 mm diameter), wayar platinum dan elektrod AgAgCl (Hydromet SC, Poland) telah digunakan sebagai kerja (WE), tambahan (AE) dan elektrod rujukan(RE), masing-masing13. Sebelum percubaan, permukaan WE telah digilap menggunakan ampaian alumina (0.0zarah 5 μm, Buehler, Amerika Syarikat)pada pad kain mikro(MF-1040, BASi, USA)dan kemudian dibersihkan dengan air suling dan metanol. Sebatian yang dikaji telah dicairkan dalam DMSO dan penimbal natrium fosfat(pH=7.4±0.1), jadi kepekatan akhir penimbal fosfat ialah {{30}}.1 M dalam sampel. Penampan berfungsi sebagai elektrolit penyokong. Kepekatan sebatian tulen ialah 3 mM. Campuran mengandungi 3 mM setiap sebatian. Untuk menghapuskan oksigen reaktif secara elektrokimia, larutan yang dikaji telah dinyahoksida oleh perkolasi argon sebelum pengukuran. Voltammogram DPV untuk N-.N tambah dan campuran: ON-dan RN tambah telah direkodkan dalam julat-0.2 hingga tambah 1.3 V, manakala untuk Q dan R dalam julat-0.2 hingga ditambah 0.6 V vs.RE.Kadar imbasan berpotensi 0.1 V.s', ketinggian nadi 0.05 V, dan masa nadi 0.1 s pada 25±0.01 darjah telah ditetapkan.
Voltammogram DPV telah dianalisis oleh perisian SigmaPlot Versi 13.0 (Systat Software Inc., UK). Nilai AOP dikira dalam dua langkah. Pengiraan mempertimbangkan bukan sahaja potensi dan arus puncak anodik (E,; I,), tetapi juga potensi set dan arus yang diukur pada setiap titik lengkung voltammetrik. Ia membenarkan nilai yang lebih tepat diperoleh daripada yang dilaporkan dalam kerja kami sebelum ini3. Pertama, parameter tenaga antioksidan (AOE) dikira mengikut Pers. 1:
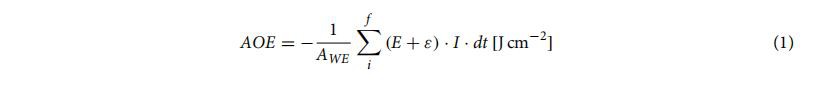
dengan AwE ialah luas permukaan WE(sama dengan {{0}}.162±0.004 cm'dalam kajian kami), E ialah potensi set berbanding RE [V], ialah a faktor pembetulan dengan mengambil kira kehadiran simpang cecair antara WE dan RE (di sini 0.103 V), I ialah arus yang diukur berbanding arus latar belakang [A], ia—ialah potensi masa pensampelan [dt=0 .5 s].
Kedua, AOP yang dinyatakan dalam unit W cm² dikira berdasarkan Persamaan.2∶

dengan tt;—ialah perbezaan antara masa permulaan puncak pengoksidaan(t) dan penghujungnya (t).
Untuk menentukan Awp, voltammetri kitaran untuk larutan 1.10-3MK,[Fe(CN).] dalam 0.1 M KCl telah dilakukan. Nilai ini dikira berdasarkan persamaan Randles-Sevcik82 daripada cerun arus puncak anodik sebagai fungsi punca kuasa dua kadar imbasan, I, =f(pi/2). Thee diukur dengan cara yang sama seperti dalam pentitratan potensiometri. Selain itu, dalam kerja ini, parameter termodinamik proses pengoksidaan ialah potensi puncak anodik yang diperbetulkan oleh persimpangan cecair antara WE dan RE (E.,=E.. tambah e), manakala parameter kinetik merangkumi cas yang dipindahkan ( Q) dan arus anodik (I,).

Cistanche boleh meningkatkan imuniti
Kultur sel. Dalam kajian yang dibentangkan, garis sel HT29 (kolon manusiaadenokarsinoma) daripada ATCC digunakan sebagai model usus manusia, Sel-sel telah dikekalkan dalam medium McCoy ditambah denganantibiotik(100 U/mL streptomycin dan 100 g/L penisilin) dan serum lembu janin(100 mL/L)13. Talian sel HT29 dikekalkan pada 37Cunder 5 peratus CO, atmosfera dalam inkubator sel(Heal Force)3. Talian sel telah digunakan antara petikan 6 dan l1. Sel yang dikultur telah diuji untuk pencemaran mycoplasma menggunakan Kit Pengesanan Mycoplasma Universal dari ATCC (USA).
Penilaian sitotoksisiti. Untuk menentukan kesan disucikanantioksidan(Q, N tambah, R, N-) dan campurannya (QN-, RN tambah ) pada pertumbuhan sel HT29, MTTtest digunakan seperti yang diterangkan sebelum ini3,5. Secara ringkasnya, sel yang berkembang pesat telah disemai dalam 96-plat kultur tisu telaga (5×10 sel setiap telaga dalam 0.18 mL medium) dan dibiarkan mengendap selama 24 jam pada 37 darjah di bawah 5 peratus CO, Kemudian, sel telah dirawat selama 6,24 atau 72 jam dengan 0.02 ml kepekatan berbeza antioksidan tulen atau campurannya3,5. Antioksidan dan campurannya telah dilarutkan dalam etanol (naringenin, naringin dan campuran—30 peratus (v/v), kuersetin-40 peratus (v/v), rutin—20 peratus (v/v )). Kepekatan akhir sebatian tulen adalah antara 10 nM hingga 100 uM. Campuran mengandungi kepekatan setara bagi setiap sebatian(10 nM-100 μM). Kepekatan terakhir etanol dalam media kultur ialah 2 peratus (v/v) dalam kes rutin, 3 peratus (v/v)naringenin, naringin, dan campuran serta 4 peratus (v/v)quercetin. Selepas pendedahan 6 dan 24 jam, medium disedut dari telaga dan digantikan dengan 0.2 mL medium segar. Sel-sel telah diinkubasi pada 37 darjah hingga 72 jam daripada jumlah masa pengeraman13,55. Selepas 72 jam pengeraman, ke semua telaga 0.05 mL larutan MTT (4 g/L) telah ditambah dan sel-sel dikekalkan selama 4 jam lagi pada 37 darjah C13,5. Kemudian, medium disedut dari telaga dan kristal formazan dilarutkan dalam 0.05 mL DMSO. Penyerapan penyelesaian yang diperolehi diukur pada 540 nm dengan bantuan pembaca plat TECAN Infinite M200 (Tecan Group Ltd, Switzerland)15. Rawatan telah dilakukan sebagai empat replika teknikal. Tiga ulangan bebas bagi setiap rawatan telah dilakukan. Kesan sampel yang disiasat ke atas pertumbuhan sel HT29 dinyatakan sebagai peratus perencatan pertumbuhan sel yang terdedah kepada antioksidan individu dan campurannya berbanding sel kawalan yang dirawat dengan pelarut sahaja, yang pertumbuhannya dianggap sebagai 100 peratus 13,55
Ujian CAA (aktiviti antioksidan selular). Ujian CAA (The OxiSelect Cell Biolabs, Inc. USA) digunakan untuk menilai aktiviti antioksidan selular bagi sebatian sahaja (O, N plus, R, N-) dan campuran (ON-, RN plus ) dalam sel HT29 seperti yang diterangkan sebelum ini35. Sel-sel yang berkembang pesat telah disemai dalam 96-plat hitam kultur tisu telaga dengan bahagian bawah lutsinar untuk pengukuran pendarfluor (3×104 sel setiap telaga dalam 0.2 ml medium) dan telah dibiarkan mengendap selama 24 jam pada 37 darjah di bawah 5 peratus CO,i3.55. Semua antioksidan telah dibubarkan dalam 10 peratus etanol. Sel-sel kemudiannya dirawat dengan 50{{50}} kali larutan dicairkan 2',7'-dichlorofluorescein diacetate (0.05 mL)disediakan dengan kit, dan volum yang sama bagi kepekatan berbeza sampel antioksidan selama 1, 3, atau 6 jam. Kepekatan akhir sebatian tulen adalah antara 1 hingga 100 uM. Campuran mengandungi kepekatan setara bagi setiap sebatian (1-100uM). Sel kawalan telah dirawat dengan 1{99}} peratus etanol sahaja (v/v). Kepekatan terakhir etanol dalam media kultur ialah 5 peratus (v/v). Semua rawatan telah dijalankan dalam tiga replika teknikal dan tiga eksperimen bebas telah dilakukan. Langkah seterusnya telah dijalankan mengikut cadangan pengeluar(https://www.cellbiolabs.com). Pengiraan telah dilakukan seperti yang diterangkan sebelum ini, Kesan genotoksik. Untuk menentukan kesan genotoksik yang ditunjukkan oleh antioksidan individu (O, N plus, RN-) dan campurannya (ON-, RN plus ) dalam sel HT29, prosedur ujian komet telah digunakan seperti yang diterangkan sebelum ini. Sel HT29 yang berkembang pesat telah disemai dalam 24-plat kultur tisu telaga(10 sel darjah setiap telaga dalam 1.8 mL medium) dan dibenarkan untuk mengendap selama 24 jam pada 37 darjah di bawah 5 peratus CO, 55, Kemudian, sel-sel telah dirawat selama 24 jam dengan 0.2 mL kepekatan antioksidan yang berbeza sahaja atau dalam campuran. Kepekatan akhir sebatian tulen adalah antara 1 hingga 100 uM. Campuran mengandungi kepekatan setara bagi setiap sebatian (1-100 uM). Kepekatan etanol akhir dalam medium kultur ialah 3 peratus (v/v). Sel-sel yang digunakan sebagai kawalan negatif dirawat dengan pelarut sahaja. Selepas masa rawatan, medium disedut dari telaga dan sel dibasuh dengan 0.5 mL PBS. Sel-sel tersebut kemudiannya ditanggalkan menggunakan 0.2 mL larutan tripsin (0.5 g/L)55 Aktiviti tripsin telah dihentikan dengan menambahkan 1.8 mL medium pertumbuhan lengkap pada setiap telaga. Sel-sel itu digantung semula, dikira dan diasingkan ke dalam tiub 1.5 mL(30×103³sel setiap tiub). Suspensi sel telah disentrifugasi(100×g,5 min,4 darjah). Pelet sel telah dibasuh dengan l mL PBS dan disentrifugasi semula (100×g,5 min, 4 darjah )5. Kemudian, PBS dibuang dan sel-sel itu digantung semula dalam 150 μL 0.5 peratus LMP agarose dalam air pra- dipanaskan hingga 42 darjah C dan 40 μL campuran ini diletakkan sebagai dua tompok pada slaid mikroskop yang telah disalut dengan 1 peratus takat lebur normal agarose (NMP agarose). Slaid ditutup dengan penutup. Agarosa dibenarkan untuk ditetapkan oleh meletakkan slaid mikroskop di atas dulang ais sejuk selama sekurang-kurangnya 5 min5. Tiga slaid dengan dua ulangan pada setiap satu disediakan untuk setiap kepekatan bahan yang diuji. Selepas lisis semalaman dalam penimbal beralkali garam tinggi (2.5 M NaCl, 0.1 M EDTA ,0.01 M Tris,1 peratus Triton X100,pH10), slaid telah dimasukkan ke dalam platform elektroforesis GT Sub-Sel Bio-Rad (UK), ditutup dengan penimbal elektroforesis sejuk (0.3 M NaOH, 1 mM EDTA, pH 13) dan kromatin dibenarkan berehat selama 25 minit sebelum elektroforesis. Elektroforesis dijalankan pada 26 V dan 300 mA(0.75 V/cm) selama 30 minit dalam kegelapan pada 4-8 darjah . Selepas langkah ini, slaid dicuci terlebih dahulu menggunakan PBS dan kemudian air. Selepas itu, DNA telah diwarnai dengan SybrGreen dalam penimbal TE (0.1 M Trizma-Base, 1 mM EDTA, pH 7.5) selama 20 min~. Selepas pewarnaan, slaid dibasuh dengan air suling selama 5 minit. "Komet" DNA dianalisis di bawah mikroskop pendarfluor (Zeiss ImagerZ2, USA) ditambah dengan sistem pengimbasan slaid berkomputer (Metafer4, Jerman). Analisis komet melibatkan mengira 200 nukleus berturut-turut setiap sampel5. Ketoksikan genotoksik sampel yang dianalisis dinyatakan sebagai peratus DNA dalam ekor komet. Tiga replika bebas bagi setiap rawatan telah dilakukan.

Cistanche boleh meningkatkan imuniti
Metilasi DNA global.
For the determination of global methylation of DNA, a modified comet assay procedure was developed. Methylation sensitive comet assay was performed according to Wentzel's procedure with significant modifications. The cells were seeded in 6-well tissue culture plates(4×105 cells per well in 3.6 mL of medium) and were allowed to settle for 24 h at 37°C under 5%CO,Then, the cells were treated with 0.4 mL, of different concentrations of the tested antioxidants or their mixtures for 24 h at 37C. The final concentrations of individual compounds and solvents were the same as used for genotoxic effect assessment. After incubation time, the medium was aspirated from the wells and the cells were washed with 2 mL of PBS. The cells were detached using 0.4 mL of trypsin solution (0.5 g/L). Then,3.6 mL of medium was added to each well. The cells were re-suspended, counted, and aliquoted into 1.5 mL tubes(30×10 cells per tube). The cell suspension was centrifuged (100×g,5 min, 4°C). The cell pellets were washed with 1 mL of PBS and centrifuged again(100×g 5 min,4℃C).PBS was discarded and the cell pellet was re-suspended in 100μL of 1%LMP agarose in water pre-warmed to 45 °C. Then,40 μL of this mixture was placed as two spots on a microscope slide pre-coated with 1%normal melting point agarose(NMP agarose)5. The slides were then covered with coverslips and left to set on an ice-cold tray for at least 5 min to solidify agarose5. Each treatment embraced a set of 3 microscope slides. After overnight lysis in a high salt alkaline buffer(2.5 M NaCl, 0.1 M EDTA, 0.01 M Tris,1% Triton X100, pH 10), the slides were washed twice with water>5. Kromatin yang padat padat telah dibuka dengan merawat nukleus dengan larutan 1.5 mM proteinase K (0.2 mL setiap slaid)3. Slaid ditutup dengan parafilem, diletakkan ke dalam bekas plastik yang dialas dengan tisu lembap, dibiarkan selama 10 min pada 37 darjah , kemudian dibasuh dengan air3. Dengan cara ini, nukleoid telah disediakan untuk pencernaan dengan endonuklease sekatan (Dewan dan MspI). Kedua-dua enzim mengiktiraf urutan sekatan yang sama(5'-CCGG-3') tetapi menunjukkan kepekaan yang berbeza terhadap sitosin termetilasi. HpalI dianggap hanya mencerna jujukan bukan metilasi. MspI boleh membelah jujukan tidak bermetilasi serta jujukan bermetilasi sepenuhnya. Oleh itu, tahap relatif metilasi DNA bagi urutan CpG dicerminkan sebagai perbezaan antara jumlah global DNA dalam ekor komet yang diperhatikan dengan pencernaan MspI dan nukleoid tercerna HpalI. Untuk mewujudkan keadaan yang sesuai untuk pencernaan enzim.{{20}}.2 mL penimbal Tango yang dicairkan dengan air gred molekul dalam nisbah 1:9(v/v) telah digunakan pada setiap slaid dalam set. Slaid ditutup dengan parafilem, dimasukkan ke dalam bekas plastik yang dialas dengan tisu lembap dan dibiarkan selama 10 min pada 37 darjah Ce. Kemudian, lebihan penimbal dikeluarkan. Setiap satu daripada tiga slaid dalam set telah dilayan secara berbeza. Pada slaid (kawalan) pertama, hanya 0.15 mL penimbal Tango yang dicairkan telah digunakan. Nukleus tertanam agarose pada slaid kedua dirawat dengan 0.15 mL enzim Hall (0.37 μunit), manakala pada slaid ketiga isipadu MspI yang sama telah ditambah (0.26 μunit). Larutan enzim disediakan menggunakan penimbal Tango yang dicairkan. Slaid ditutup dengan parafilem dan dimasukkan ke dalam bekas plastik lembap. Pencernaan enzimatik dijalankan selama 45 minit pada 37 darjah. Selepas penghadaman, slaid dicuci dua kali dengan air. Langkah selanjutnya ujian komet, seperti elektroforesis dan pewarnaan DNA, telah dilakukan seperti yang diterangkan dalam bahagian "Metilasi DNA Global". "Komet" DNA dianalisis di bawah mikroskop pendarfluor (Zeiss ImagerZ2, Amerika Syarikat) ditambah dengan sistem pengimbasan slaid berkomputer (Metafer4, Jerman). Analisis komet dilakukan dengan bantuan perisian skor Komet (AS) dan melibatkan pengiraan 100 nukleus setiap sampel. Purata peratus DNA dalam ekor komet adalah ukuran pemecahan DNA. Untuk mengira DNA globalmetilasi( peratus metilasi CpG), persamaan berikut telah digunakan: peratus metilasi CpG=100—Hpal/MspI×100, dengan Hpal/MspI ialah nisbah peratusan DNA dalam ekor komet nukleoid yang dicerna dengan HpalII dan DNA peratusan dalam ekor komet nukleoid yang dicerna dengan Mspl85. Artifak kerosakan DNA diambil kira dengan menolak peratusan DNA dalam ekor sampel kawalan daripada nilai yang diperoleh untuk sampel yang dicerna dengan enzim sekatan. Tiga ulangan bebas bagi setiap eksperimen telah dilakukan.

Analisis mikroarray.
Analisis genom telah dilakukan seperti yang ditunjukkan sebelumi355, sel HT29 telah disemai dalam 24-plat kultur tisu telaga (105 sel setiap telaga dalam 1.8 mL medium) dan dibenarkan untuk mengendap selama 24 jam pada 37 darjah di bawah 5 peratus CO, Kemudian, sel telah dirawat selama 24 jam dengan 0.2 mL kepekatan antioksidan yang berbeza sahaja (Q, N-) atau dalam campuran (QN-). Kepekatan akhir sebatian yang disiasat adalah antara 1 hingga 10 uM. Campuran mengandungi kepekatan yang setara bagi setiap sebatian. Sel-sel yang digunakan sebagai kawalan negatif dirawat dengan pelarut sahaja. Kepekatan terakhir etanol dalam media kultur ialah 3 peratus (v/y). Pengasingan RNA. transkripsi terbalik dan tatasusunan PCR masa nyata yang terdiri daripada 84 gen yang terlibat dalam tindak balas antioksidan serta analisis data telah dilakukan seperti yang diterangkan sebelum ini. Tiga ulangan bebas bagi setiap rawatan sel telah dijalankan.
Analisis statistik.
Semua nilai dinyatakan sebagai min±SD bagi tiga eksperimen bebas melainkan dinyatakan sebaliknya. Kepentingan statistik penentuan aktiviti antioksidan dalam sistem bebas sel menggunakan ujian DPV dan DPPH serta dalam model selular yang diperolehi oleh ujian CAA telah diperiksa dengan ujian Tukey yang tidak berpasangan (p Kurang daripada atau sama dengan 0.{{ 6}}5). Keputusan genotoksisiti dan metilasi DNA global yang dianalisis oleh ujian komet telah diperiksa oleh ANOVA sehala dengan ujian post-hoc Dunnett. Analisis statistik ini dilakukan menggunakan pakej perisian Prism 4.0(GraphPad Software, Inc., USA). Kepentingan statistik perubahan dalam ekspresi gen antara sampel dan kawalan juga dinilai oleh ujian-t Pelajar yang tidak berpasangan untuk setiap gen yang diminati menggunakan Pusat Analisis Data GenGlobe (Qiagen, Amerika Syarikat). Tahap kepentingan statistik ditetapkan padap Kurang daripada atau sama dengan 0.05.
Artikel ini dipetik daripadawww.nature.com/scientificreports
