Induksi Kekebalan Mukosa Oleh Pentadbiran Pulmonari Nanozarah yang menyasarkan sel
Jul 05, 2023
ABSTRAK
Kami sebelum ini mendapati bahawa zarah nano yang dibina dengan antigen, benzalkonium klorida (BK) dan asid c-polyglutamic (c-PGA) menunjukkan induksi imun jenis Th1 dan Th2-yang tinggi selepas pentadbiran subkutaneus. Untuk profilaksis jangkitan pernafasan, bagaimanapun, imuniti mukosa harus diinduksi. Dalam kajian ini, kami menyiasat kesan pentadbiran paru-paru nanopartikel yang terdiri daripada ovalbumin (OVA) sebagai model antigen, BK, dan c-PGA pada induksi imuniti mukosa dalam paru-paru dan serum.
Kompleks ini diambil dengan kuat oleh sel RAW264.7 dan DC2.4. Selepas pentadbiran paru-paru, pengekalan paru-paru lebih lama untuk kompleks OVA / BK / c-PGA daripada untuk OVA sahaja. Imunoglobulin serum khusus OVA (Ig) G sangat diinduksi oleh kompleks. Tahap IgG dan IgA yang tinggi juga diinduksi dalam cecair lavage bronchoalveolar, dan dalam vivo, ketoksikan tidak diperhatikan. Kesimpulannya, kami secara berkesan dan selamat mendorong imuniti mukosa oleh pentadbiran paru-paru kompleks OVA/BK/c-PGA.
Dalam beberapa tahun kebelakangan ini, semakin banyak kajian menunjukkan bahawa imuniti mukosa memainkan peranan penting dalam sistem imun badan. Kekebalan mukosa merujuk kepada sistem imun berasaskan membran mukus dalam tubuh manusia, dan keupayaan pertahanannya ditujukan terutamanya untuk pencerobohan patogen dalam membran mukus manusia seperti saluran pernafasan, saluran penghadaman, dan saluran pembiakan.
Imuniti mukosa itu sendiri tidak menjadikan badan lebih kebal, tetapi ia boleh membantu badan kita menangani pencerobohan patogen asing dengan lebih berkesan. Dengan terus merangsang imuniti mukosa, badan kita menghasilkan lebih banyak antibodi, yang meningkatkan imuniti kita.
Jadi, bagaimanakah imuniti mukosa boleh dirangsang? Berikut adalah beberapa cadangan:
1. Dapatkan vitamin C yang mencukupi. Vitamin C ialah antioksidan semulajadi yang meningkatkan fungsi sel imun, yang membantu melawan jangkitan. Buah-buahan dan sayur-sayuran berdaun hijau seperti limau, oren, dan strawberi kaya dengan vitamin C.
2. Meningkatkan pengambilan bakteria asid laktik. Bakteria asid laktik boleh menggalakkan keseimbangan flora usus dan menghalang pertumbuhan bakteria berbahaya. Makanan bakteria asid laktik yang biasa termasuk yogurt, sauerkraut, kimchi, dll.
3. Amalkan bernafas dengan nafas dalam. Pernafasan dalam meningkatkan bekalan oksigen dan pengudaraan ke paru-paru, yang boleh membantu membuang patogen terkumpul dari paru-paru.
Ringkasnya, merangsang imuniti mukosa adalah cara penting untuk meningkatkan imuniti. Kita harus mencuba yang terbaik untuk meningkatkan imuniti mukosa melalui pemakanan dan tabiat hidup, untuk melindungi kesihatan kita. Dari sudut pandangan ini, kita perlu meningkatkan imuniti. Cistanche boleh meningkatkan imuniti dengan ketara kerana abu daging mengandungi pelbagai komponen aktif secara biologi, seperti polisakarida, dua cendawan, dan Huang Li, yang boleh merangsang sistem imun. Pelbagai jenis sel, meningkatkan aktiviti imun mereka.

Klik suplemen cistanche deserticola
1. Pengenalan
Jangkitan pernafasan akut hampir pasti merupakan punca utama kematian di kalangan kanak-kanak < 5 tahun di negara membangun (Williams et al., 2002). Beberapa vaksin, seperti vaksin influenza, pertusis, dan pneumokokus, telah dibangunkan untuk jangkitan pernafasan (White, 1988; Pittman, 1991; Chen et al., 2020). Kebanyakan vaksin tersebut diberikan melalui laluan intramuskular dan subkutan, yang boleh mendorong imunoglobulin serum (Ig)G secara berkesan. Walau bagaimanapun, laluan lain lebih berguna untuk merangsang imuniti mukosa untuk mencegah jangkitan pernafasan akut. Pentadbiran mukosa, seperti intranasal dan pulmonari, telah dilaporkan berkesan mendorong IgA mukosa dan mencegah jangkitan pernafasan (Giri et al., 2005; Ainai et al., 2017).
Sebaliknya, vaksin untuk pentadbiran intranasal dan pulmonari tidak seharusnya mengandungi bahan tambahan yang telah dilaporkan menyebabkan tindak balas keradangan dan ulser di tapak pentadbiran (Tamura et al., 1988; McKee et al., 2007). Satu lagi pendekatan untuk meningkatkan keberkesanan vaksin tanpa bahan pembantu ialah membangunkan sistem yang boleh menghantar vaksin secara berkesan ke dalam sel pembentang antigen mukosa (APC).
Dalam kajian terdahulu, kami membangunkan vektor penghantaran vaksin baru yang dibina dengan antigen, benzalkonium klorida (BK), dan asid c-polyglutamic (c-PGA). Kompleks yang terdiri daripada ovalbumin (OVA) sebagai antigen model, BK dan c-PGA (kompleks OVA/BK/c-PGA) secara berkesan menghantar OVA ke dalam sel dendritik dan meningkatkan induksi IgG serum khusus OVA selepas pentadbiran subkutan ke dalam tikus (Kurosaki et al. ., 2012). Kajian ini bertujuan untuk menyiasat kesan pentadbiran pulmonari kompleks OVA/BK/c-PGA terhadap induksi imuniti mukosa dalam paru-paru dan serum.
2. Bahan-bahan dan cara-cara
2.1. Bahan kimia
OVA telah dibeli daripada Sigma-Aldrich (St. Louis, MO, Amerika Syarikat). BK diperoleh daripada Nacalai Tesque, Inc. (Kyoto, Jepun). C-PGA disediakan oleh Yakult Pharmaceutical Industry Co., Ltd. (Tokyo, Jepun). OVA berlabel Fluorescein isothiocyanate (FITC-OVA) dan Alexa Fluor 647-berlabel OVA (Alexa647- OVA) diperoleh daripada Invitrogen (Carls, CA, USA). Fetal bovine serum (FBS) dibeli daripada Biological Industries Ltd. (Kibbutz Beit Haemek, Israel). OPTI-MEM I diperoleh daripada GIBCO BRL (Grand Island, NY, USA), dan larutan antibiotik pracampuran yang mengandungi penisilin, streptomisin dan L-glutamin diperoleh daripada Wako Pure Chemical Industries, Ltd. (Osaka, Jepun). Medium Helang Modified Dulbecco (DMEM) dan medium RPMI1640 diperoleh daripada Nissui Pharmaceutical Co., Ltd. (Tokyo, Jepun).
2.2. Penyediaan yang kompleks
Sebelum ini, kami membina kompleks OVA/BK/c-PGA pada nisbah berat 1:0.2:0.2 (Kurosaki et al., 2012). Untuk menyediakan kompleks OVA/BK, jumlah larutan BK yang sesuai (pH 5.0) yang dilarutkan dalam 5 peratus glukosa dicampur dengan larutan OVA (pH 7.0) yang dilarutkan dalam 5 peratus glukosa dan dibiarkan selama 15 minit pada suhu 4 C. Untuk menyalut kompleks OVA/BK dengan c-PGA, larutan c-PGA (pH 7.0) yang dilarutkan dalam 5 peratus glukosa telah ditambah kepada kompleks OVA/BK dan dibiarkan selama 15 minit lagi pada 4 C. Saiz zarah dan potensi f bagi setiap kompleks diukur dengan menggunakan Zetasiser Nano ZS (Malvern Instruments, Ltd., Malvern, UK).
2.3. sel
Talian sel makrofaj tikus RAW264.7 dan garisan sel dendritik DC2.4 telah digunakan. Sel RAW264.7 telah ditanam dalam DMEM ditambah dengan 10 peratus FBS dan antibiotik. Sel DC2.4 telah ditanam dalam medium RPMI1640 ditambah dengan 10 peratus FBS, antibiotik, 1 mM asid amino bukan penting dan 1 nM 2-mercaptoethanol. Sel-sel ini dinilai di bawah suasana lembap sebanyak 5 peratus CO2 di udara pada 37C.

2.4. Eksperimen pengambilan selular in vitro
Sel RAW264.7 dan sel DC2.4 disalut pada 24-plat perigi (Corning, NY, USA) pada ketumpatan 2.0 104 sel/telaga dan ditanam dalam 50{ {21}} mL medium kultur. Selepas 24-h prainkubasi, medium telah digantikan dengan medium OPTI-MEM I, dan sel telah diinkubasi dengan 5 mg FITC-OVA dan kompleks yang mengandungi 5 mg FITC-OVA selama 2 jam. Selepas pengeraman, sel tersebut dibasuh dengan PBS dan diperhatikan di bawah mikroskop pendarfluor (BIOREVO BZ-9000; Keyence Co., Osaka, Jepun). Selepas pemerhatian, sel-sel tersebut telah dilisiskan dalam 300 lL penimbal lisis (pH 7.8 dan 0.1 M Tris/HCl penimbal yang mengandungi 0.05 peratus Triton X-100 dan 2 mM EDTA). Lisat diletakkan ke dalam 96-plat telaga, dan pendarfluor FITC-OVA diukur pada panjang gelombang pancaran 530 nm dengan panjang gelombang pengujaan 480 nm, menggunakan pembaca plat mikro fluorometrik (Infinite-200Pro M-Plex, Tecan Japan Co., Ltd., Kanagawa, Jepun). Kandungan protein lysate ditentukan oleh ujian Bradford menggunakan BSA sebagai standard. Penyerapan diukur menggunakan pembaca plat mikro pada 570 nm. Pengambilan FITC-OVA ditunjukkan sebagai mg per mg protein.
2.5. Haiwan
Penjagaan haiwan dan prosedur eksperimen dilakukan oleh Garis Panduan untuk Eksperimen Haiwan Universiti Nagasaki dengan kelulusan daripada Jawatankuasa Penjagaan dan Penggunaan Haiwan Institusi. Tikus C57BL/6N jantan (5 minggu) telah dibeli dari Jepun SLC (Shizuoka, Jepun). Selepas diangkut, tikus dibenarkan menyesuaikan diri dengan persekitaran baru mereka selama 1 hari sebelum eksperimen. Pentadbiran pulmonari (40 mL) dilakukan dengan menggunakan penekan lidah dengan cahaya melalui pernafasan spontan pada tikus yang dibius melalui penyedutan isoflurane (Horiguchi et al., 2015).
2.6. Pengumpulan paru-paru kompleks
Untuk memeriksa pengumpulan OVA, 40 mg Alexa647-OVA dan kompleks yang mengandungi 40 mg Alexa647- OVA pada volum 40 mL setiap tetikus telah ditadbir ke dalam tikus melalui laluan paru-paru. Enam hari selepas pentadbiran, tikus dikorbankan dan paru-paru dibedah. Keamatan pendarfluor Alexa647-OVA dalam paru-paru tetikus diperhatikan dengan Sistem Lumina Xenogen IVIS ditambah dengan perisian Living Image untuk pemerolehan data (Xenogen, Co, Almeda, CA, USA). Selepas pemerhatian, paru-paru tersebut dihomogenkan dengan penimbal lisis dan homogenat disentrifugasi pada 15,000 rpm (Kubota-3500, Kubota Corporation, Tokyo, Jepun) selama 5 minit dan pendarfluor Alexa647 dalam supernatan tersebut telah ditentukan dengan pemimpin mikroplat pada pengujaan dan panjang gelombang pancaran masing-masing 640 dan 670 nm.
2.7. Imunisasi
Tikus telah diimunisasi dengan larutan glukosa 5 peratus, 40 mg OVA, kompleks kosong 8 mg BK dan 8 mg c-PGA (kenderaan), dan kompleks OVA/BK/c-PGA yang mengandungi 40 mg OVA melalui pemberian pulmonari, 4 kali setiap minggu. Dua minggu selepas imunisasi terakhir, cecair lavage bronchoalveolar (BALF) dan serum diperolehi. BALF dan serum digunakan untuk ujian imunosorben berkaitan enzim (ELISA).
2.8. Penentuan induksi antibodi khusus OVA
Untuk salutan OVA, 100 mL larutan OVA (10 mg/mL, dalam 1 M natrium hidrogen karbonat) telah ditambahkan pada setiap telaga plat ELISA (Thermo Fisher Scientific Inc., Waltham, MA, USA) dan diinkubasi semalaman pada suhu 4 C. Plat dibasuh tiga kali dengan garam penimbal fosfat yang mengandungi 0.05 peratus Tween-20 (PBST), 200 mL reagen penyekat N 102 (Nichiyu, Co., Ltd., Tokyo, Jepun ) ditambah untuk menyekat pengikatan tidak spesifik dan kemudian diinkubasi selama 6 jam pada suhu 4 C. Plat telah dibasuh dua kali dengan PBST. Kemudian, 100 mL aliquot 1000-kali ganda serum cair dan sampel BALF tidak cair ditambah ke dalam setiap telaga dan diinkubasi semalaman pada suhu 4 C. Selepas lima kali mencuci dengan PBST, 100 mL setiap lobak pedas peroksidase (HRP) – anti kambing terkonjugasi -tikus IgG, IgA, IgM, IgE, IgG1, IgG2a, IgG2b dan IgG3 (1:10,000) (Abcam, Cambridge, UK) – telah ditambahkan pada setiap perigi dan diinkubasi pada suhu bilik selama 1 jam dan kemudian dibasuh lima kali dengan PBST. Penyelesaian TMB One (Promega, WI, USA) telah digunakan dan disediakan mengikut arahan pengilang. Tindak balas kemudian dihentikan pada 15 minit dengan penambahan asid hidroklorik 1 N. Penyerapan dibaca pada 450 nm dengan menggunakan pembaca plat mikro.
2.9. Ketoksikan in vivo kompleks OVA/BK/c-PGA
Kompleks OVA dan OVA / BK / c-PGA diberikan kepada tikus melalui laluan pulmonari. BALF diperolehi 3 dan 24 jam selepas pentadbiran daripada tikus. Dua puluh empat jam selepas pentadbiran, paru-paru juga dibedah. Aktiviti dehidrogenase laktat (LDH) dalam BALF diukur menggunakan Kit Dehidrogenase Laktat QuantiChromTM (Sistem BioAssay, CA, Amerika Syarikat) mengikut arahan kilang. Sampel paru-paru telah ditetapkan dalam larutan penimbal fosfat paraformaldehid 4 peratus. Pembahagian dan pewarnaan hematoxylin-eosin (HE) telah diamanahkan kepada GenoStaff (Tokyo, Jepun). Bahagian paru-paru yang diwarnai HE telah diperhatikan dengan mikroskop pada pembesaran 20.
2.10. Analisis statistik
Kepentingan statistik perbezaan antara kedua-dua kumpulan dinilai dengan melaksanakan ujian-t Pelajar. Perbandingan berbilang antara kumpulan dilakukan dengan melakukan ujian Tukey. p-Values < .05 dianggap sebagai menunjukkan kepentingan statistik.
3. Keputusan
3.1. Sifat fizikokimia kompleks
Kami membina kompleks OVA/BK/c-PGA anionik pada nisbah berat 1:0.2:0.2. Kompleks bersalut c-PGA mempunyai saiz zarah kira-kira 105.4 nm dan potensi f kira-kira 35.5 mV.


3.2. Pengambilan sel kompleks
Sel RAW264.7 dan sel DC2.4 telah dirawat dengan kompleks FITC-OVA dan FITC-OVA/BK/c-PGA, dan pengambilan selular FITC-OVA telah divisualisasikan, seperti yang ditunjukkan dalam Rajah 1. FITC-OVA/BK/ Kompleks c-PGA sangat diambil oleh sel RAW264.7 dan sel DC2.4, dan pendarfluor hijau FITC-OVA yang kuat diperhatikan (Rajah 1 (A, B), masing-masing). Pada masa yang sama, sejumlah kecil FITC-OVA diperhatikan dalam kedua-dua sel yang dirawat dengan FITC-OVA.
Pengambilan selular FITC-OVA dikira dalam sel RAW264.7 dan sel DC2.4 (Rajah 1(C)). Kompleks FITC-OVA/BK/ c-PGA menunjukkan pengambilan yang lebih tinggi daripada FITC-OVA dalam kedua-dua sel (p <.01).
3.3. Pengumpulan paru-paru Alexa647-OVA selepas pentadbiran paru-paru
Kompleks Alexa647-OVA dan Alexa647-OVA/BK/c-PGA telah diberikan kepada tikus melalui laluan pulmonari untuk menentukan pengumpulan paru-paru Alexa647-OVA sebagai antigen. Pada 6 hari selepas pentadbiran, paru-paru telah dibedah, dan keamatan pendarfluor mereka divisualisasikan dengan menggunakan Sistem Lumina Xenogen IVIS. Imej pendarfluor ex-vivo ditunjukkan dalam Rajah 2(A). Keamatan pendarfluor yang tinggi diperhatikan di seluruh paru-paru 6 hari selepas pentadbiran paru-paru, walaupun tiada keamatan pendarfluor dalam limpa, jantung, buah pinggang, dan hati (data tidak ditunjukkan). Pengumpulan paru-paru adalah lebih tinggi untuk kompleks Alexa647-OVA/BK/c-PGA berbanding Alexa647-OVA pada hari ke-6. Seperti yang ditunjukkan dalam Rajah 2(B), pengumpulan paru-paru adalah lebih tinggi dengan ketara untuk Alexa 647-Kompleks OVA/BK/c-PGA daripada untuk Alexa647- OVA (p <.05).

3.4. Antibodi khusus OVA dalam serum selepas pentadbiran pulmonari kompleks
Penyelesaian glukosa 5 peratus, kompleks BK/c-PGA (kenderaan), OVA, dan kompleks OVA/BK/c-PGA diberikan melalui laluan pulmonari ke dalam tikus empat kali, dan kemudian serum IgG khusus OVA, IgA, IgM, dan IgE ditentukan oleh ELISA seperti yang ditunjukkan dalam Rajah 3. Pentadbiran paru-paru OVA dan kompleks OVA/BK/c-PGA meningkatkan tahap IgG pada tikus, walaupun IgG khusus OVA tidak dikesan pada tikus yang diberi 5 peratus glukosa dan kenderaan. Tambahan pula, pengeluaran IgG dan IgA adalah lebih tinggi dengan ketara selepas pentadbiran kompleks OVA/BK/c-PGA berbanding selepas pentadbiran OVA (p <.05 atau .01). Sebaliknya, IgM dan IgE khusus OVA tidak diinduksi oleh OVA atau kompleks OVA/BK/c-PGA.

3.5. Antibodi khusus OVA dalam BALF selepas pentadbiran pulmonari kompleks
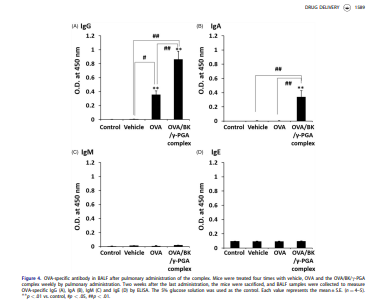
IgG, IgA, IgM, dan IgE khusus OVA dalam BALF juga ditentukan, seperti yang ditunjukkan dalam Rajah 4. Tahap IgG meningkat dengan ketara oleh OVA berbanding tahap selepas pentadbiran kawalan dan kenderaan (p <.05 atau .01). Namun begitu, kompleks OVA/BK/c-PGA meningkat dengan ketara bukan sahaja IgG tetapi juga IgA dalam BALF (p <.01). Walau bagaimanapun, IgM dan IgE khusus OVA tidak diinduksi oleh OVA atau kompleks OVA/BK/c-PGA.
3.6. Subtipe IgG dalam serum selepas pentadbiran pulmonari kompleks
Kesan induksi subtipe IgG khusus OVA, seperti IgG1, IgG2a, IgG2b, dan IgG3 dalam serum ditentukan seperti ditunjukkan dalam Rajah 5. Berbanding dengan kawalan dan kenderaan, OVA hanya meningkat dengan ketara IgG1 (p <.01). Tahap antibodi semua subtipe yang disebabkan oleh kompleks OVA/BK/c-PGA adalah lebih tinggi daripada tahap yang disebabkan oleh kawalan dan kenderaan (p <.05 atau .01).
3.7. Subtipe IgG dalam BALF selepas pentadbiran pulmonari kompleks
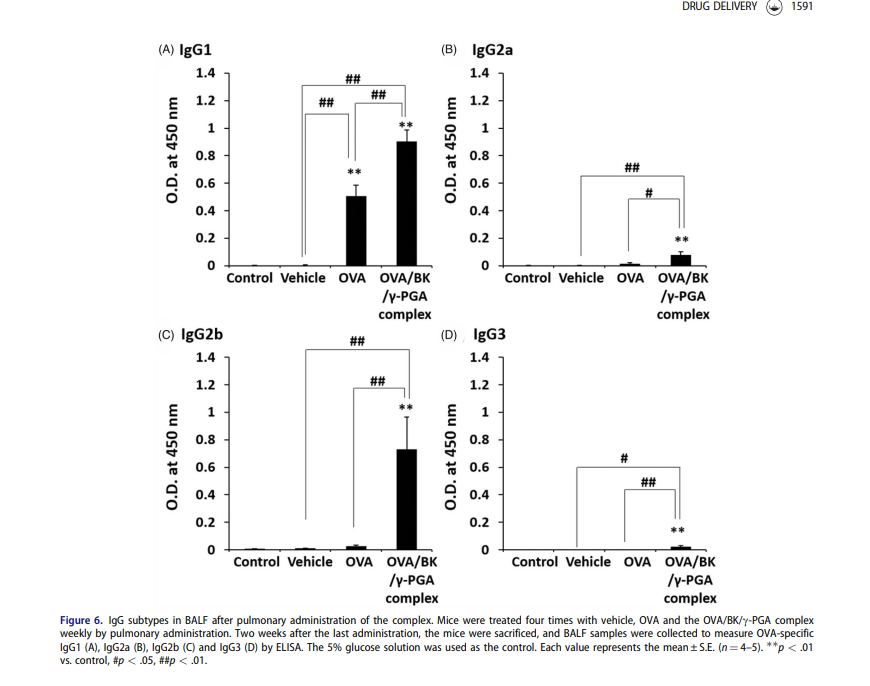
Subjenis IgG khusus OVA, seperti IgG1, IgG2a, IgG2b, dan IgG3 dalam BALF juga ditentukan, seperti yang ditunjukkan dalam Rajah 6. OVA meningkat dengan ketara hanya tahap IgG1 berbanding dengan yang disebabkan oleh kawalan dan kenderaan (p <.01) . Berbanding dengan kawalan, kenderaan dan OVA, kompleks OVA/BK/ c-PGA mendorong tahap antibodi yang lebih tinggi secara ketara bagi semua subjenis (p <.05 atau .01).
3.8. Ketoksikan in vivo kompleks OVA/BK/c-PGA
Tikus diberikan larutan glukosa 5 peratus, OVA, dan kompleks OVA/BK/c-PGA. Aktiviti LDH dalam BALF ditentukan 3 atau 24 jam selepas pentadbiran (Rajah 7). Pentadbiran kompleks OVA dan OVA/BK/c-PGA mempunyai sedikit kesan ke atas tahap LDH dalam BALF.
Dua puluh empat jam selepas pentadbiran, paru-paru telah dibedah daripada tikus tersebut untuk analisis histologi. Bahagian paru-paru yang diwarnai HE ditunjukkan dalam Rajah 8. Tiada keabnormalan histologi diperhatikan pada tikus yang dirawat dengan OVA dan kompleks OVA/BK/c-PGA.
4. Perbincangan
Paru-paru mengawal pernafasan dan terdedah kepada banyak patogen, seperti virus dan bakteria yang menyebabkan jangkitan pernafasan. Patogen tersebut menjangkiti melalui membran mukosa pulmonari, jadi imuniti mukosa mesti didorong untuk melindungi daripada jangkitan pernafasan. Mencegah jangkitan pernafasan, imuniti mukosa mempunyai peranan penting; Walau bagaimanapun, pentadbiran intradermal dan intramuskular vaksin tidak boleh merangsang imuniti mukosa dengan kuat (Ito et al., 2003; Amorij et al., 2007). Sistem imun mukosa yang mendorong rembesan IgA dibangunkan pada permukaan mukosa. Beberapa APC, seperti sel dendritik dan makrofaj, telah dilaporkan terletak di permukaan mukosa (Kopf et al., 2015). Tambahan pula, tisu limfoid berkaitan bronkus (BALT) terdapat dalam mukosa bronkiolar dan merupakan folikel limfoid yang mempunyai peranan penting dalam imuniti mukosa saluran pernafasan (Bienenstock, 1980). Pemberian vaksin secara paru-paru dijangka dapat merangsang sistem imun mukosa dengan berkesan. Oleh itu, kami membina kompleks OVA/BK/c-PGA untuk menilai kegunaannya sebagai vaksin yang diberikan melalui laluan pulmonari.
Rajah 4 menunjukkan kepekatan BALF antibodi khusus OVA selepas pentadbiran paru-paru OVA dan kompleks OVA/BK/c-PGA. Pentadbiran paru-paru OVA meningkatkan IgG tetapi mempunyai sedikit kesan pada IgA dalam BALF. Sebaliknya, kompleks OVA/BK/c-PGA secara signifikan menyebabkan rembesan IgA dalam BALF. Tambahan pula, induksi IgG serum adalah lebih tinggi selepas pentadbiran kompleks OVA/BK/ c-PGA berbanding selepas pentadbiran OVA (Rajah 3). Serum IgG adalah penting untuk mencegah keterukan sebarang jangkitan yang berlaku (Huber et al., 2006; Schroeder & Cavacini, 2010). Keputusan menunjukkan bahawa kompleks OVA/BK/c-PGA boleh mencegah jangkitan pernafasan oleh induksi IgA mukosa yang tinggi dan keterukan jangkitan pernafasan oleh induksi IgG serum yang tinggi. Tambahan pula, induksi IgE oleh kompleks OVA/BK/c-PGA tidak diperhatikan, dan keputusan ini menunjukkan sedikit risiko tindak balas alahan oleh kompleks OVA/BK/ c-PGA.
Kompleks OVA/BK/c-PGA juga boleh mendorong bukan sahaja IgG1 dan IgG2b tetapi juga IgG2a dan IgG3 (Rajah 5). IgG1 dan IgG2b dikenali sebagai imunoglobulin jenis Th2-yang mengantara tindak balas imun humoral, dan IgG2a dan IgG3 dikenali sebagai imunoglobulin jenis Th1-yang mengantara tindak balas imun selular (Firacative et al., 2018) . Oleh itu, kompleks OVA / BK / c-PGA boleh mendorong tindak balas imun humoral dan selular. Keputusan ini menunjukkan bahawa sistem ini boleh berguna untuk vaksin melawan jangkitan dan juga kanser. Kesan pencegahan, tindak balas sitokin jenis Th{15}} dan Th{16}}yang disebabkan oleh antigen dalam induksi BALT, populasi Treg dan IL{17}} yang boleh diinduksi hendaklah dinilai menggunakan antigen sebenar daripada jangkitan atau kanser pada masa hadapan pengajian.
Induksi kuat oleh kompleks OVA/BK/c-PGA bagi tindak balas imun mestilah disebabkan oleh pengekalan kompleks yang tinggi di dalam paru-paru dan penghantaran OVA yang berkesan ke dalam APC dalam mukosa paru-paru. Keputusan kami mengesahkan ini dengan menunjukkan bahawa 6 hari selepas pentadbiran, kompleks Alexa647-OVA/BK/c-PGA kekal di dalam paru-paru dan menunjukkan pendarfluor yang jauh lebih tinggi daripada Alexa647- OVA (Rajah 2). Pembentukan kompleks mungkin menghalang penyebaran OVA dan melindungi OVA daripada degradasi oleh protease dalam mukosa pulmonari. Tambahan pula, kompleks OVA/BK/c-PGA dapat menyampaikan OVA dengan berkesan ke dalam sel makrofaj RAW264.7 dan sel dendritik DC2.4 (Rajah 1). Keputusan tersebut menunjukkan bahawa kompleks OVA/BK/c-PGA akan diambil oleh APC alveolar dan mendorong tindak balas imun yang tinggi selepas pentadbiran pulmonari. Telah dilaporkan bahawa nanopartikel bersalut c-PGA telah diambil oleh laluan endositotik pengantara transpeptidase gamma-glutamyl (Du et al., 2015). Kami juga mengesahkan nanopartikel bersalut c-PGA telah diambil oleh laluan endositotik khusus c-PGA (Kurosaki et al., 2009). Kompleks OVA/BK/c-PGA mungkin diambil oleh APC dalam paru-paru melalui mekanisme yang sama. Walau bagaimanapun, masih tidak jelas sel mana yang bertanggungjawab untuk pengambilan OVA dan pembentangan antigen seterusnya dalam induksi imuniti khusus. Kajian lanjut mengenai mekanisme induksi imun yang terperinci perlu dilakukan pada masa hadapan.


Banyak bahan bantu telah dibangunkan untuk meningkatkan keberkesanan vaksin; bagaimanapun, bahan pembantu telah dilaporkan menyebabkan tindak balas keradangan di tapak suntikan (Tamura et al., 1988; McKee et al., 2007). Oleh itu, pemberian adjuvant pada paru-paru mungkin menyebabkan kesan sampingan yang teruk, seperti radang paru-paru. Selepas pentadbiran pulmonari kompleks OVA / BK / c-PGA, tahap LDH dalam BALF tidak meningkat (Rajah 7) dan keabnormalan histologi tidak diperhatikan dalam bahagian yang diwarnai HE (Rajah 8). Dilaporkan, c-PGA ialah polimer biokompatibel dan biodegradasi yang tidak menunjukkan tindak balas imuno-radang (Prodhomme et al., 2003; Ye et al., 2006). BK ialah sebatian ammonium kuaternari yang selamat yang telah digunakan secara meluas secara klinikal sebagai bahan tambahan antimikrob (Marple et al., 2004). Laporan ini juga menyokong keselamatan kompleks OVA/BK/c-PGA. Sebaliknya, tahap LDH yang lebih tinggi diperhatikan pada 3 jam selepas pentadbiran pulmonari daripada pada 24 jam, walaupun dalam kumpulan kawalan. Keputusan tersebut menunjukkan bahawa sedikit kerengsaan disebabkan oleh pemberian pulmonari. Kajian keselamatan lanjut diperlukan sebelum aplikasi klinikal kompleks OVA/BK/c-PGA.
Dalam kajian ini, kami menunjukkan induksi sistem imun mukosa yang tinggi oleh vektor penghantaran vaksin baru yang dibina dengan protein antigen, BK, dan c-PGA selepas pentadbiran paru-paru. Sistem ini boleh digunakan untuk vaksin terhadap pelbagai jangkitan pernafasan.

Kenyataan pendedahan
Tiada potensi konflik kepentingan dilaporkan oleh pengarang.
Pembiayaan
Kerja ini disokong oleh Japan Society for the Promotion of Science (JSPS) KAKENHI di bawah geran [JP20K12649 dan JP20K07156].
Rujukan
1.Ainai A, Suzuki T, Tamura SI, et al. (2017). Pentadbiran intranasal bagi seluruh vaksin virus influenza yang tidak aktif sebagai calon vaksin influenza yang menjanjikan. Immunol Viral 30:451–62.
2.Amorij JP, Saluja V, Petersen AH, et al. (2007). Penghantaran pulmonari vaksin subunit influenza yang distabilkan inulin yang disediakan dengan pengeringan semburan beku mendorong tindak balas imun sistemik, mukosa serta pengantaraan sel dalam tikus BALB/c. Vaksin 25:8707–17.
3.Bienenstock J. (1980). Tisu limfoid yang berkaitan dengan bronkus dan sumber sel yang mengandungi imunoglobulin dalam mukosa. Perspektif Kesihatan Persekitaran 35:39–42.
4.Chen JR, Liu YM, Tseng YC, et al. (2020). Vaksin influenza yang lebih baik: perspektif industri. J Biomed Sci 27:11.
5. Du X, Xiong L, Dai S, et al. (2015). Nanopartikel silika mesopori bersalut c-PGA dengan prodrug yang dilekatkan secara kovalen untuk pengambilan selular yang dipertingkatkan dan pelepasan responsif GSH intraselular. Adv Healthc Mater 4: 771–81.
6. Firacative C, Gressler AE, Schubert K, et al. (2018). Pengenalpastian antigen T helper (Th)1- dan Th2-yang berkaitan dengan cryptococcus neoformans dalam model murine jangkitan pulmonari. Sci Rep 8:14.
7. Giri PK, Sable SB, Verma I, et al. (2005). Penilaian perbandingan laluan imunisasi intranasal dan subkutaneus untuk pembangunan vaksin mukosa terhadap tuberkulosis eksperimen. FEMS Immunol Med Microbiol 45:87–93.
8. Horiguchi M, Oiso Y, Sakai H, et al. (2015). Pentadbiran pulmonari phosphoinositide 3-kinase inhibitor ialah rawatan kuratif untuk penyakit pulmonari obstruktif kronik melalui penjanaan semula alveolar. J Keluaran Kawalan 213:112–9.
9. Huber VC, McKeon RM, Brackin MN, et al. (2006). Sumbangan berbeza imunoglobulin G1 (IgG1) dan IgG2a yang disebabkan oleh vaksin kepada imuniti perlindungan terhadap influenza. Clin Vaccine Immunol 13: 981–90.
10. Ito R, Ozaki YA, Yoshikawa T, et al. (2003). Peranan antibodi anti-hemagglutinin IgA dan IgG di tapak berlainan saluran pernafasan tikus yang divaksin dalam mencegah radang paru-paru influenza yang boleh membawa maut. Vaksin 21:2362–71.
11.Kopf M, Schneider C, Nobs SP. (2015). Perkembangan dan fungsi makrofaj pemastautin paru-paru dan sel dendritik. Nat Immunol 16: 36–44.
12.Kurosaki T, Kitahara T, Fumoto S, et al. (2009). Kompleks ternari pDNA, polyethyleneimine, dan asid gamma-polyglutamic untuk sistem penghantaran gen. Biobahan 30:2846–53.
13.Kurosaki T, Kitahara T, Nakamura T, et al. (2012). Pembangunan vaksin kanser yang berkesan menggunakan sistem penyasaran protein antigen kepada APC. Pharm Res 29:483–9.
14. Marple B, Roland P, Benninger M. (2004). Kajian keselamatan benzalkonium klorida yang digunakan sebagai pengawet dalam larutan intranasal: gambaran keseluruhan data dan pendapat yang bercanggah. Otolaryngol Kepala Leher Surg 130: 131–41.
15.McKee AS, Munks MW, Marrack P. (2007). Bagaimanakah adjuvant berfungsi? Pertimbangan penting untuk adjuvant generasi baharu. Kekebalan 27: 687–90.
For more information:1950477648nn@gmail.com
